Struktur natrium asetat, sifat, sintesis, penggunaan

- 4621
- 174
- Ray Thiel
Dia Sodium asetat Itu adalah garam natrium asam asetat yang formula molekulnya c2H3SALAH SATU2Na. Ini terdiri dari bubuk putih lezat, pada dasarnya hadir dalam dua bentuk: anhidrat dan trihidrat. Keduanya sangat larut dalam air, pelarut universal; Tetapi tidak begitu larut dalam alkohol atau aseton.
Bentuk anhidra memiliki kepadatan, titik fusi dan didih dengan nilai yang lebih tinggi daripada yang disajikan oleh bentuk trihidrat natrium asetat. Ini karena molekul air mengganggu interaksi ion na+ dan ch3Mendekut-.
 Penampilan natrium asetat
Penampilan natrium asetat Sodium asetat stabil, terutama jika disimpan antara 2 dan 8 ºC; Tetapi rentan terhadap aksi agen pengoksidasi dan halogen yang kuat.
Itu dapat disiapkan dengan reaksi natrium bikarbonat dengan asam asetat. Juga, dengan reaksi asam asetat dengan natrium hidroksida. Kedua reaksi sederhana untuk rumit dan biaya ekonomi rendah; Yang pertama bahkan bisa dilakukan di rumah.
Garam ini adalah senyawa kecil beracun. Menghasilkan iritasi kulit, hanya setelah kontak yang sering dan terus menerus. Itu sedikit menjengkelkan mata tetapi bisa mengiritasi saluran udara. Tidak ada informasi tentang efek berbahaya dari konsumsi Anda.
Ini memiliki banyak kegunaan dan aplikasi, menyoroti fungsi redaman pH, bersama dengan asam asetat. Penyerap kejut asetat memiliki PKA = 4.7; yang memberikan efisiensi tinggi dalam regulasi pH dalam lingkungan asam dengan nilai pH antara 3 dan 6.
Karena toksisitasnya yang rendah dan sifat -sifatnya, ia telah banyak digunakan untuk meningkatkan rasa makanan, serta agen yang memberikan perlindungan terhadap dekomposisi mereka karena tindakan mereka terhadap mikroba.
[TOC]
Struktur natrium asetat
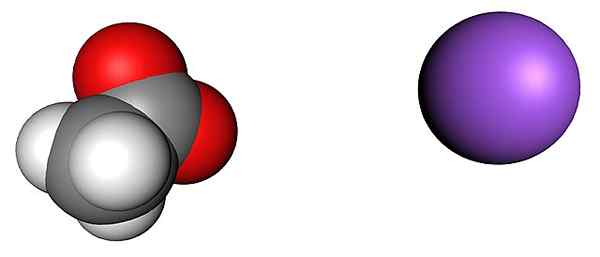 Ion asetat dan natrium. Sumber: SHU0309 [CC BY-SA 4.0 (https: // createveCommons.Org/lisensi/by-sa/4.0)]
Ion asetat dan natrium. Sumber: SHU0309 [CC BY-SA 4.0 (https: // createveCommons.Org/lisensi/by-sa/4.0)] Gambar atas menunjukkan ion yang membentuk kristal natrium asetat anhidrat (tanpa air). Bola ungu sesuai dengan na kation+, Dan ion molekuler di sebelah kirinya adalah asetat, cho3Mendekut-, Dengan atom oksigennya diwakili oleh bola merah.
Rekan -rekan ini, menurut chip ch3Jalur, berada dalam proporsi 1: 1; Untuk setiap cho3Mendekut-, Pasti ada kation+ tertarik dengan beban negatif dan sebaliknya. Dengan demikian, atraksi di antara mereka, dan tolakan antara beban yang sama, akhirnya menetapkan pola struktural yang mendefinisikan kristal, yang ekspresi minimalnya adalah sel kesatuan.
Sel kesatuan ini, seperti kaca secara keseluruhan, bervariasi tergantung pada disposisi ion di ruang angkasa; Itu tidak selalu sama, bahkan untuk sistem kristal yang sama. Misalnya, natrium asetat anhidrat dapat membentuk dua polimorf ortorombik, salah satunya diwakili di bawah ini:
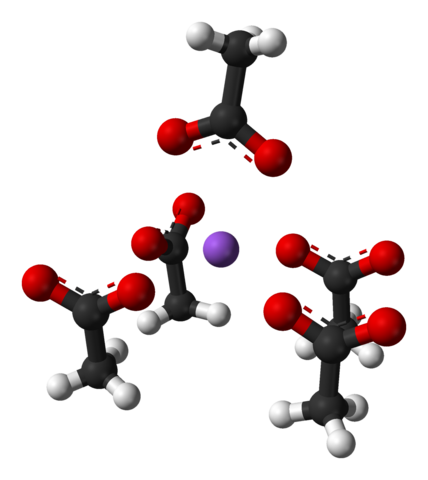 Sel kesatuan kristal orthorrombik natrium asetat. Sumber: Benjah-BMM27 [Domain Publik]
Sel kesatuan kristal orthorrombik natrium asetat. Sumber: Benjah-BMM27 [Domain Publik] Perhatikan pengaturan ion: empat ion cho3Mendekut- Mereka melampirkan na+ sedemikian rupa sehingga mereka "menggambar" piramida dasar persegi yang terdistorsi. Masing -masing Cho ini3Mendekut- pada gilirannya berinteraksi dengan NA lain+ bersebelahan.
Kristal terhidrasi
Sodium asetat memiliki banyak afinitas terhadap air; Sebenarnya itu lezat, yaitu, mempertahankan kelembaban sampai larut dalam hal yang sama. Semakin besar kelembaban, lebih cepat "meleleh". Ini karena begitu3Mendekut- Seperti na+ Mereka dapat melembabkan, mengelilingi diri mereka dengan molekul air yang memandu dipol mereka menuju beban mereka (NA+ Oh2, Ch3Mendekut- HOH).
Dapat melayani Anda: perak bromida (agbr): struktur, sifat dan penggunaanKetika garam ini disiapkan di laboratorium atau di rumah, itu adalah afinitas terhadap air sehingga bahkan pada suhu normal sudah diperoleh sebagai hidrat; ch3Pata · 3H2SALAH SATU. Kristal mereka berhenti menjadi ortorombik dan menjadi monoklinik, karena mereka sekarang menggabungkan tiga molekul air untuk setiap pasangan cho3Mendekut- dan na+.
Properti
Nama
-Sodium asetat.
-Sodium Ethanoate (IUPAC).
Masa molar
-Anhydrous: 82.03 g/mol.
-Trihidrasi: 136,03 g/mol.
Aspek
Bubuk putih lezat.
Bau
Menjadi cuka saat dia dipanaskan untuk dekomposisi.
Kepadatan
-Anhidro: 1, 528 g/cm3 pada 20 ºC.
-Trihidrasi: 1,45 g/cm3 pada 20 ºC.
Titik lebur
-Anhidro: 324 ºC (615 ºF, 597 K).
-Triohidrat: 58 ºC (136 ºF, 331 K).
Titik didih
-Anhidro: 881.4 ºC (1.618.5 ºF, 1.154.5 k).
-TriHydrate: 122 ºC (252 ºF, 395 K). Itu membusuk.
Kelarutan
Di dalam air
-Anhydro: 123,3 g/100 ml pada 20ºC.
-Trihidrasi: 46,4 g/100 ml pada 20 ºC.
Dalam metanol
16 g/100 g pada 15 ºC.
Dalam etanol
5.3 g/100 ml (trihidrat).
Di aseton
0,5 g/kg pada suhu 15 ° C.
Keasaman
PKA: 24 (20 ºC).
Basa
PKB: 9.25. Di sini terbukti bahwa natrium asetat adalah garam dasar karena harus memiliki PKB kurang dari pKa -nya.
Indeks refraksi (ηd)
1.464
Kapasitas kalori
-100.83 J/mol · k (anhidrat).
-229.9 J/mol · k (trihydrado).
titik pengapian
Lebih dari 250ºC.
Suhu diri sendiri
600 ºC.
ph
8,9 (solusi 0,1 m hingga 25 ºC).
Stabilitas
Stabil. Tidak sesuai dengan agen pengoksidasi yang kuat dan halogen. Kelembaban.
Reaksi
Sodium asetat dapat membentuk ester dengan bereaksi dengan rental halida; Misalnya, Bromoetano:
Ch3Poron +BRCH2Ch3 => Ch3Cooch2Ch3 + Nabr
Sodium asetat adalah dekarboksila untuk membentuk metana (pirolisis) di hadapan NaOH:
Ch3Poon +naoh => ch4 + Na2BERSAMA3
Reaksi dikatalisis oleh penjualan Cesio.
Perpaduan
Sodium asetat dapat diproduksi dengan biaya rendah di laboratorium dengan bereaksi natrium bikarbonat dengan asam asetat:
Nahco3 + Ch3Cooh => ch3Jalur +h2BERSAMA3
Reaksi ini disertai dengan keberadaan dalam larutan gelembung yang intens, karena dekomposisi asam karbonat dalam air dan karbon dioksida.
H2BERSAMA3 => H2Atau +co2
Secara industri, natrium asetat diproduksi oleh reaksi asam asetat dengan natrium hidroksida.
Ch3CoOH +naoh => ch3Jalur +h2SALAH SATU
Aplikasi
Kantong termal
Sodium asetat digunakan untuk pembuatan kantong termal.
Awalnya, kristal garam dilarutkan dalam volume air untuk persiapan larutan yang menjadi sangat jenuh.
Kemudian solusi pada suhu yang lebih besar dari 58 ºC dipanaskan, yang merupakan titik lelehnya. Larutan jenuh super pada suhu kamar dibiarkan dingin dan pembentukan kristal tidak diamati; Solusinya sudah lebih dari -chirp.
Dapat melayani Anda: tabel periodik, untuk apaTidak adanya kristal dijelaskan bahwa molekul cair terlalu berantakan dan tidak memiliki bimbingan untuk mencapai suhu kristalisasi. Cairan itu dalam keadaan metastabil, keadaan ketidakseimbangan.
Memberi. Dalam kasus kantong termal, perlekatan mekanis ditekan untuk mengaduk cairan dan memulai pembentukan kristal dan pemadatan larutan natrium asetat trihidrasi.
Ketika kristalisasi terjadi, suhu meningkat. Kristal natrium asetat trihidrasi memperoleh penampilan es, tetapi mereka panas, jadi disebut "es panas".
Industrialis
-Sodium asetat digunakan dalam industri tekstil sebagai mordan dalam proses pewarnaan jaringan
-Menetralkan limbah asam sulfat
-Ini telah digunakan dalam pemrosesan kapas untuk elaborasi kapas, dapat digunakan dalam pembersihan pribadi dan untuk tujuan medis
-Ini digunakan dalam acar logam, sebelum kromnya
-Berkolaborasi sehingga vulkanisasi kloroprene tidak terjadi dalam proses produksi karet sintetis
-Campur tangan dalam pemurnian glukosa
-Itu digunakan dalam penyamakan kulit.
Penggunaan medis
Sodium asetat adalah bagian dari senyawa yang digunakan untuk memasok elektrolit yang diberikan kepada pasien secara intravena.
Ini digunakan untuk memperbaiki kadar natrium pada pasien hiponathemik, juga dalam koreksi asidosis metabolik dan alkalinasi urin.
Solusi redaman pH
Ini digunakan sebagai regulator pH dalam banyak reaksi enzimatik yang terjadi antara pH 3 dan pH 6.
PH yang berbeda dari larutan buffer asetat dicapai dengan variasi konsentrasi asam asetat dan natrium asetat.
Misalnya, untuk mendapatkan pH 4,5 larutan buffer memiliki konsentrasi asam asetat 3,8 g/L dan konsentrasi natrium asetat anhidrat 3,0 g/L.
Konsentrasi larutan buffer asetat dapat ditingkatkan, meningkat dalam proporsi yang sama komponen dari larutan yang diperlukan untuk mendapatkan pH yang diinginkan.
Penyerap goncangan asetat/asetonitril digunakan dalam elektroforesis kapiler dalam pemisahan photoberberine.
Laboratorium Penelitian
-Sodium asetat adalah agen nukleofilik yang lemah yang digunakan dalam polimerisasi anionik β-lakton.
-Ini digunakan sebagai reagen dalam resonansi magnetik nuklir makromolekul biologis.
-Itu digunakan dalam ekstraksi sel sel. Sodium adalah kation yang berinteraksi dengan beban negatif fosfat yang ada dalam DNA, yang membantu dalam kondensasinya. Di hadapan etanol, DNA membentuk endapan yang kemudian dapat dipisahkan menjadi lapisan air.
Konservasi makanan
-Ini membantu mencegah pertumbuhan bakteri, selain mencegah pembentukan kelebihan keasaman yang menyebabkan penurunan makanan, sehingga mempertahankan pH tertentu.
-Sodium yang ada dalam asetat meningkatkan rasa makanan.
-Sodium asetat digunakan dalam persiapan acar sayuran: mentimun, wortel, bawang, dll. Selain itu, digunakan dalam konservasi daging.
Dapat melayani Anda: dimethlanylin: struktur, sifat, sintesis, penggunaanKonservasi beton
Beton rusak oleh aksi air yang memperpendek durasinya. Natrium asetat bertindak sebagai zat sealant beton yang tahan air untuk air, memperpanjang karakteristik awalnya.
Eksperimen Muda
Eksperimen 1
Eksperimen sederhana adalah sintesis natrium asetat melalui reaksi natrium bikarbonat dengan cuka (asam asetat 5%).
30 ml cuka ditempatkan dalam gelas kimia dan sekitar 3,5 g bikarbonat ditambahkan.
Dalam reaksi natrium dan bentuk asam karbonat terbentuk. Asam dipecah menjadi karbon dioksida dan air. Generasi karbon dioksida akan menghasilkan gelembung yang intens dalam larutan.
Untuk mengumpulkan natrium asetat, penguapan air disebabkan, memanaskan larutan.
Eksperimen 2
Eksperimen sederhana lainnya adalah pembentukan natrium trihidrat asetat.
Untuk melakukan ini, sekitar 20 g trihidrat natrium asetat dan ditempatkan di gelas, kemudian menambahkan 10 ml air, kemudian menambahkan 10 ml air. Solusinya dipanaskan hingga suhu yang lebih besar dari 58 ºC.
Natrium asetat benar -benar larut untuk memastikan bahwa solusinya supers jenuh. Sebelumnya, kapsul pietri ditempatkan di permukaan yang dingin.
Isi gelas dengan trihidrat asetat dalam kapsul Pietri perlahan -lahan dituangkan. Suhu cairan dalam kapsul mulai turun, bahkan di bawah titik leleh, tanpa mengamati kristalisasi atau pemadatan natrium asetat trihidrat.
Biasanya menghasilkan kristalisasi natrium asetat trihidrasi, sejumlah kecil garam ditambahkan untuk berfungsi sebagai inti kristalisasi. Di lain waktu ada gangguan kecil dari larutan, untuk memulai kristalisasi natrium asetat.
Kristal natrium asetat trihidrasi terlihat seperti es, tetapi jika disentuh akan diperhatikan bahwa mereka relatif panas. Karena alasan ini, garam disebut "es panas".
Toksisitas
Natrium asetat adalah senyawa beracun yang sangat kecil. Juga tidak diklasifikasikan sebagai sensitizer untuk kulit dan saluran udara.
Selain itu, natrium asetat tidak diklasifikasikan sebagai agen mutagenik pada kuman, karsinogen atau sel toksik untuk reproduksi.
Singkatnya, itu sedikit menjengkelkan mata. Saluran udara bisa jengkel setelah inhalasi mereka. Kontak yang sering dan konstan dengan kulit dapat menyebabkan iritasi.
Referensi
- Shiver & Atkins. (2008). Kimia anorganik. (Edisi keempat). MC Graw Hill.
- Worldofchemicals. (16 Januari 2017). Cara menyiapkan natrium asetat di rumah? Pulih dari: medium.com
- Pusat Nasional Informasi Bioteknologi. (2019). Sodium asetat. Database pubchem. CID = 517045. Pulih dari: pubchem.NCBI.Nlm.Nih.Pemerintah
- S. Cameron, k. M. Mannan dan m. SALAH SATU. Rahman. (1976). Struktur kristal natrium asetat trihidrat. Cryst Act. B32, 87.
- Wikipedia. (2019). Sodium asetat. Diperoleh dari: di.Wikipedia.org
- Helmestine, Anne Marie, PH.D. (24 Januari 2019). Buat es panas dari cuka dan soda kue. Pulih dari: thinkco.com
- Buku Kimia. (2017). Sodium asetat. Dipulihkan dari: Chemicalbook.com
- Wasserman Robin. (2019). Penggunaan natrium asetat. Pulih dari: livestrong.com
- CHANKBANK. (2019). Sodium asetat. Pulih dari: bankbank.Ac

