Karakteristik, Struktur, Fungsi Alanina, Biosintesis
- 4291
- 1013
- Dewey Runolfsdottir
Itu untuk gadis itu (Sayap) adalah salah satu dari 22 asam amino yang diketahui yang membentuk struktur protein dari semua organisme, dari bakteri ke pria. Seperti yang dapat disintesis oleh organisme, ini diklasifikasikan sebagai asam amino yang tidak penting.
Protein memiliki struktur dasar atau primer yang terdiri dari rantai asam amino yang disebut rantai polipeptida, dalam rantai tersebut masing -masing asam amino dibentuk oleh karbon sentral yang disebut karbon α.
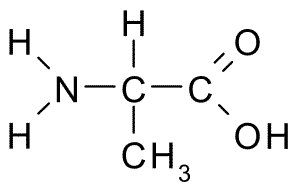
 Struktur Kimia Asam Amino Alanin (Sumber: Borb, Via Wikimedia Commons)
Struktur Kimia Asam Amino Alanin (Sumber: Borb, Via Wikimedia Commons) Karbon α bergabung dengan empat kelompok: gugus amino (-NH2), kelompok karboksil (-COH), atom hidrogen (-H) dan kelompok atau rantai samping (-r) yang mengidentifikasi setiap asam amino. Di rantai samping, karbon secara berurutan mengambil huruf ß, γ, δ dan ε.
Asam amino diklasifikasikan oleh polaritas rantai sampingnya dan dengan demikian ada asam amino polar hidrofobik dan hidrofilik yang, pada gilirannya, dapat netral, basa dan asam. Alanin adalah asam amino apolar hidrofobik dan merupakan asam amino paling sederhana setelah glisin dan yang paling berlimpah di sebagian besar protein.
Alanin dapat dibentuk di otot dan diangkut ke hati, di mana ia diperkenalkan ke rute glukoneogenik, yaitu, rute untuk pembentukan glukosa dari zat non -glukosida. Alanin juga dapat disintesis di hati melalui katabolisme triptofan dan urasil dan dapat terdegradasi untuk membentuk piruvat.
Berpartisipasi dalam sintesis tryptophan, piridoksin (vitamin B6) dan daging.
Ini digunakan sebagai suplemen makanan untuk meningkatkan kinerja olahraga dan secara alami ditemukan dalam daging sapi, babi dan ikan, serta susu dan turunannya dan telurnya. Beberapa kacang -kacangan, buah -buahan, dan kacang -kacangan juga kaya akan alanine.
[TOC]
Struktur
Sebelumnya dikomentari bahwa alanin, seperti semua asam amino, memiliki karbon α dengan empat kelompok yang disatukan untuk itu, menjadi kelompok r grup A A (-CH3).
Oleh karena itu, ke pH tubuh (sekitar 7.4) Karbon α dari alanin terkait dengan kelompok proton amino (-NH3+), dengan kelompok karboksil yang telah kehilangan proton (-co-), untuk hidrogen dan gugus metil (-CH3).
Sebagian besar asam amino terionisasi hingga pH 7.0 dan secara geometris mereka dapat memiliki isomer, yang dikenal sebagai enansiomer, yang merupakan gambar specular, seperti halnya tangan kanan dan kiri.
Dapat melayani Anda: histokimia: fondasi, pemrosesan, pewarnaanKemudian, semua asam amino dapat ditemukan sebagai "pasangan kiral" yang dilambangkan sebagai D atau L (Dextro dan Levo, masing -masing), sesuai dengan posisi atom di sekitar karbon α.
Namun, alanine, seperti kebanyakan asam amino.
Asam amino ini juga dapat ditemukan sebagai β-alanin, di mana gugus amino melekat pada karbon β-nya, yaitu karbon pertama dari rantai sampingnya.
Β-alanin ditemukan dalam asam pantotenat (vitamin B5) dan di beberapa peptida alami. D-alanin ditemukan di beberapa polipeptida yang merupakan bagian dari dinding beberapa sel bakteri.
Grup R (Metilo, Ch3)
Metil rantai samping alanin adalah hidrokarbon jenuh yang memberikan karakteristik hidrofobik apolar untuk asam amino ini. Karakteristik alanin ini sering terjadi pada asam amino lainnya dari kelompok ini seperti glisin, valin, leusin dan isoleusin.
Asam amino yang membentuk kelompok alifatik adalah asam amino netral kimia dan memainkan peran yang sangat penting dalam pembentukan dan pemeliharaan struktur protein tiga dimensi karena mereka memiliki kecenderungan untuk bereaksi satu sama lain tidak termasuk air.
Asam amino ini, termasuk alanin, mengandung jumlah kelompok terionisasi yang sama dengan beban yang berlawanan, sehingga mereka tidak memiliki beban bersih dan disebut "Zwitterions ".
Fungsi
Seperti yang paling diketahui asam amino, alanin digunakan dalam sintesis peptida dan protein secara umum, dan berpartisipasi dalam pembentukan struktur polipeptida dan dalam struktur tersier beberapa protein.
Fungsi penting lain dari alanine adalah untuk berpartisipasi secara tidak langsung dalam kontrol glikemia:
Ini dapat memunculkan piruvat dan sebaliknya, ini juga dapat mencapai hati dan menjadi glukosa melalui glukoneogenesis agar terlihat beredar atau digunakan dalam sintesis glikogen, seperlunya diperlukan.
Alanine berpartisipasi sebagai pengangkut amonium dari otot ke hati, karena dapat disintesis dengan aminasi dari piruvat, mengangkut hati dan ada transaminasi dengan transaminasi.
Ini terjadi secara bersamaan dengan transformasi α-zotoglutarate menjadi glutamat, yang dapat memasuki siklus urea dan menjadi piruvat.
Fungsi lainnya
Asam amino ini sangat diperlukan untuk sintesis tryptophan dan piridoksin. Meskipun secara kimiawi sangat sedikit reaktif, alanin dapat memiliki pengakuan substrat dan pengakuan regulasi enzimatik.
Dapat melayani Anda: kelompok pargapilikalSalah satu fungsi β-alanin adalah suplemen makanan, karena digunakan sebagai bantuan ergogenik dari latihan ini. Asupan β-alanin meningkatkan konsentrasi berdaging (dipéptide yang dibentuk oleh β-alanin dan histidin) pada otot rangka, bertindak sebagai "penyangga".
Biasanya, berdaging tidak berkontribusi secara signifikan terhadap kapasitas buffer total sel otot dan ini disebabkan oleh konsentrasi yang rendah. Pemberian β-alanin meningkatkan konsentrasi ini dan oleh karena itu kapasitas buffer, sehingga meningkatkan resistensi dengan mengurangi kelelahan.
Biosintesis
Sintesis alanin yang paling penting dalam tubuh manusia terjadi dengan aminasi reduktif asam piruvat. Reaksi ini membutuhkan langkah enzimatik tunggal.
Piruvat menyediakan kerangka karbon dan glutamat menyediakan kelompok amino yang ditransfer ke piruvat. Enzim yang mengkatalisasi reaksi reversibel ini adalah transaminase alanin.
Sebagai hasil dari reaksi ini, alanin dan α-cetoglutarate diproduksi. Alanin kemudian dapat hadir dalam glukoneogenesis, glikolisis dan dalam siklus Krebs.
Sumber Alanin lain berasal dari degradasi triptofan menjadi asetil-CoA. Pada rute ini, ketika enzim quinureninase menghidrolisis di quinurenine 3-hydroxi dibentuk 3-hidroksi antranilate dan alanin. Alanine dilepaskan dan antranilate 3-hidroksi mengikuti rute metabolisme.
Degradasi urasil adalah sumber lain dari alanine. Dalam hal ini ada β-alanine yang dapat mengikuti beberapa jalur metabolisme, salah satunya adalah menjadi asetil-CoA.
Degradasi
Proses Umum Degradasi Asam Amino
Asam amino tidak disimpan sebagai karbohidrat dan lemak, sehingga yang dilepaskan selama degradasi protein harus digunakan kembali untuk sintesis protein baru dan nukleotida.
Di sisi lain, asam amino dapat terdegradasi dan kerangka berkarbonasi dapat digunakan dalam reaksi katabolik atau anabolik.
Ketika asam amino terdegradasi, bentuk amonia nitrogen berlebih, yang merupakan zat beracun yang harus dihilangkan dan langkah pertama degradasi asam amino adalah eliminasi nitrogen.
Pada mamalia, degradasi ini terjadi di hati; Di sana, semua asam amino yang berlebihan dan tidak dapat digunakan terdegradasi.
Degradasi alanine
Degradasi alanin terjadi dengan konversi alanin menjadi piruvat. Reaksi ini dikatalisis oleh transaminase alanin dan membutuhkan adanya α-zotoglutarate sebagai akseptor dari kelompok amino dan pembentukan glutamat berikutnya; Itu adalah reaksi yang dapat dibalikkan.
Dapat melayani Anda: faktor virulensiReaksi pembentukan alanin ini dari piruvat dan degradasi alanin untuk membentuk piruvat adalah bagian dari siklus yang melibatkan otot dan hati rangka.
Hati mengambil glukosa ke otot dan otot, melalui glikolisis, mengubah glukosa menjadi piruvat untuk menghasilkan ATP; Piruvat ini dapat memasuki sintesis alanin, yang dapat dituangkan ke dalam torrent peredaran darah dan kembali ke hati yang membuatnya lagi piruvat, yang memasuki glukoneogenesis untuk membentuk glukosa.
Jika perlu siklus diulangi. Di hati, produksi piruvat dari alanine menghasilkan ion amonium yang melihat glutamin dan glutamat dan mereka memasuki siklus urea. Kemudian urea dihilangkan dengan urin.
Alanin, glisin, sistein, serin, dan treonin adalah asam amino glikogenik karena degradasinya dapat memunculkan piruvat, α-zetoglutarat, succinyl-coA, menjadi fumarat atau oksalasat, semua prekursor glukoneogenik dari glukosa atau oksalasetat, semua glukoneogenik dari glukosa dari glukosa atau oksalasetat, glukoneogenik dari glukosa dari glukosa dari glukosa atau oksalasetat dari glukoneogenik dari glukoneogenik dari glukoneik dari glukoneik atau.
Makanan Kaya di Alanina
Sumber utama asam amino adalah daging tanpa lemak, ikan, kerang, telur dan produk susu, namun, alanine juga ditemukan di banyak makanan yang berasal dari tanaman. Contoh makanan yang kaya di Alanina adalah:
- Daging seperti sapi, babi, domba, ayam, kalkun, kelinci, ikan; Telur, susu dan turunan.
- Buah kering seperti hazelnut, kacang -kacangan, chestnut, almond dan kacang adalah sumber Alanina.
- Kelapa, alpukat, asparagus, terong, singkong atau singkong, bit, wortel dan ubi jalar.
- Legum seperti jagung, kacang dan kacang polong.
- Sereal seperti nasi, gandum, gandum, kakao, gandum dan gandum hitam.
Referensi
- Caruso, J., Charles, J., Unruh, k., Giebel, r., Learmonth, l., & Potter, W. (2012). Efek ergogenik β-alanin dan karnosin: Diusulkan penelitian di masa depan untuk mengukur efficacy. Nutrisi, 4(7), 585-601.
- Gille, c., Bölling, c., Hoppe, a., Bulik, s., Hoffmann, s., Hübner, k.,… Holzhütter, h. G. (2010). Hepatonet1: Rekonstruksi metabolisme komprehensif hepatosit manusia untuk analisis fisiologi hati. Biologi Sistem Molekuler, 6(411), 1-13.
- Mathews, c., Van Holde, K., & Ahern, k. (2000). Biokimia (Edisi ke -3.). San Francisco, California: Pearson.
- Murray, r., Bender, d., Botham, k., Kennelly, hlm., Rodwell, v., & Weil, p. (2009). Biokimia Illustrated Harper (Edisi ke -28.). McGraw-Hill Medical.
- Nelson, d. L., & Cox, m. M. (2009). Prinsip -prinsip biokimia lehninger. Edisi Omega (Edisi ke -5.).

