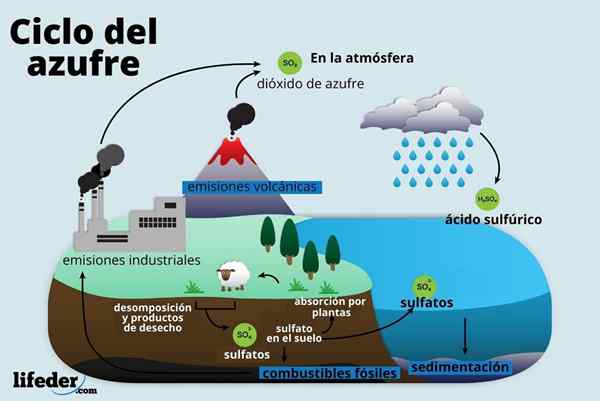
Siklus belerang
- 4725
- 1369
- Frederick Pfeffer
Apa siklus belerang?
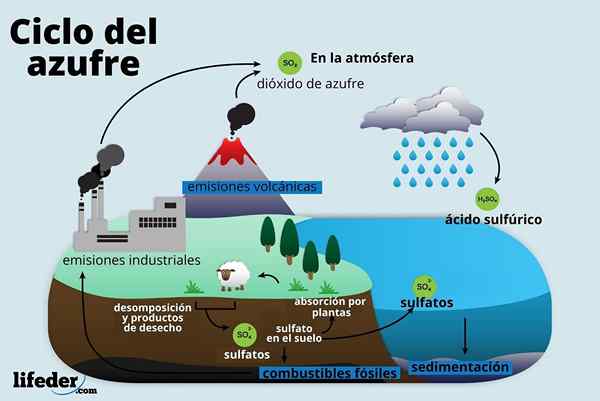
Dia Siklus belerang Ini adalah proses sirkulasi elemen kimia ini di planet bumi. Proses ini diekspresikan dalam serangkaian tahapan atau fase yang mencakup biosfer, litosfer, atmosfer dan hidrosfer.
Dengan demikian, partikel sulfur di bumi melewati tanah dan batu, udara, air dan makhluk hidup. Gerakan ini terus diulang, bergerak dari satu lingkungan ke lingkungan lainnya.
Belerang adalah elemen kuning dan bau yang tidak menyenangkan, yang reservoir terbesarnya berada di litosfer. Ini ditemukan terutama dalam endapan bahan bakar fosil seperti batubara dan minyak, dibubarkan di perairan samudera dan menjadi bagian dari makhluk hidup.
Siklus sulfur sangat penting, karena elemen kimia ini memainkan peran penting untuk kehidupan, baik mendukung atau mengancam makhluk hidup, tergantung pada zat yang terbentuk dan dari mana asalnya.
Menjadi bagian dari asam amino esensial, enzim dan klorofil, belerang sangat penting untuk keberadaan organisme hidup. Pada saat yang sama dengan polutan, itu adalah bagian dari hujan asam dan dapat menjadi faktor negatif seumur hidup.
Karakteristik siklus belerang
Sulfur
Elemen kimia ini adalah non-logam, diwakili dengan huruf "S", kuning, kuning kehijauan, oranye, coklat-kuning atau abu-abu. Selain itu, rapuh, lembut, dengan kecerahan sutra atau resin dan bau yang tidak menyenangkan. Saat belerang terbakar, menghasilkan nyala api biru dan membebaskan belerang anhidrida yang merupakan gas beracun.
Siklus biogeokimia
Siklus belerang adalah siklus biogeokimia, yaitu bahwa elemen ini beredar antara organisme hidup dan lingkungan. Ini juga merupakan siklus jenis gas, karena membentuk gas, memiliki fase penting di atmosfer.
Pada gilirannya, dalam proses ini perubahan kimia terjadi, karena dapat dikombinasikan dengan oksigen dan senyawa lainnya. Siklus ini menjamin ketersediaan belerang, memberikan kesinambungan untuk kehidupan di planet ini, karena elemen ini adalah makronutrien.
Seperti siklus biogeokimia lainnya, sulfur memiliki endapan, aliran dan komposisi dan perubahan fase. Dalam hal ini, endapan belerang utama berada di litosfer, terutama dalam bahan bakar fosil seperti batubara dan minyak.
Demikian pula, ada serangkaian aliran yang melintas di berbagai arah antara atmosfer, tanah, air dan makhluk hidup. Belerang ditemukan dalam aliran dalam berbagai keadaan gas, padat dan terlarut dalam air.
Dapat melayani Anda: 10 bioma Meksiko dan karakteristiknyaDemikian pula, sulfur mengasumsikan bentuk kimia yang berbeda, misalnya kalsium sulfat (case4) dan magnesium sulfat (MGSO4). Bentuk lain adalah belerang dioksida (jadi2), asam sulfat (h2Sw4), karbon sulfida (CS2), hidrogen sulfida (h2S) dan ion sulfat terlarut (jadi42-).
Tahap siklus belerang
Fase atau tahapan di mana belerang lewat dalam siklusnya, tidak mengikuti urutan yang ketat. Yaitu, belerang dapat melewati dari tanah ke organisme hidup dan dari ini lagi ke tanah.
Itu juga dapat melewati dari lantai ke udara dan lagi ke tanah atau udara ke air, dari sini ke organisme hidup dan lagi ke tanah.
Fase litologis: di bebatuan dan tanah
 Roca dengan belerang
Roca dengan belerang Sulfur mineral ditemukan di batu -batu kaya di elemen ini, seperti batubara mineral. Juga endapan plester (kalsium sulfat), saat membusuk, dapat menghasilkan endapan belerang di tanah.
Minyak adalah senyawa lain yang disimpan dalam lapisan geologis dan mengandung belerang. Demikian pula, dalam magma atau endapan batuan yang meleleh di dalam bumi, belerang berlimpah.
Belerang mencapai tanah karena dekomposisi makhluk hidup, hujan asam atau sedimentasi sulfur mineral. Di sisi lain, ia meninggalkan tanah dengan tiga jalur mendasar: aktivitas gunung berapi, ekstraksi alami oleh makhluk hidup atau ekstraksi manusia.
Gunung berapi mengeluarkan gas -gas kaya sulfur seperti sulfur dioksida dan juga lava, yang di antara komponen lainnya mengandung mineral ini. Selain itu, bakteri dan tanaman menyerap senyawa yang kaya akan nutrisi tanah.
Di sisi lain, manusia mengekstrak senyawa dengan belerang untuk menghasilkan energi atau menggunakannya di industri. Aktivitas ini menghasilkan gas limbah yang mengandung unsur ini, yang melewati atmosfer. Misalnya, batubara dan minyak adalah senyawa kaya belerang yang diekstraksi dari bumi.
Fase Atmosfer: Di Udara
 Letusan Gunung Berapi Krakatoa
Letusan Gunung Berapi Krakatoa Belerang mencapai atmosfer karena2). Gas ini tidak berwarna, mengiritasi dan menembus bau.
Dapat melayani Anda: Leopold Matrix: Apa itu, untuk apa, keuntungan, contohSelain itu, sulfur dioksida muncul dari sumber buatan seperti tanaman termoelektrik, pipa knalpot mobil dan pabrik. Saat kontak dengan uap air di awan, SO2 menghasilkan asam sulfat yang mengembun dalam tetesan air dan endapan.
Dengan demikian jatuh larut dalam air hujan atau salju, mencapai tanah atau badan air (sungai, danau, lautan). Sulfur juga dimasukkan ke dalam atmosfer sebagai hidrogen sulfida dengan aktivitas bakteri baik di tanah maupun air.
Fase Biologis: Dalam Organisme Hidup
Sulfur memasuki fase biologis ketika dimasukkan ke dalam rantai makanan, yang terjadi ketika diserap oleh bakteri dan tanaman baik di tanah maupun di dalam air. Itu diserap sebagai ion sulfat yang dilarutkan dalam air dan kemudian diubah menjadi sulfida dengan reduksi.
Setelah diserap, menjadi protein yang membentuk tubuh bakteri dan tanaman. Ini pada gilirannya dikonsumsi oleh organisme lain, yang mendapatkan belerang yang mereka butuhkan untuk nutrisi mereka.
Misalnya, tanaman menyerap belerang, hewan herbivora mengkonsumsi tanaman dan ini pada gilirannya dikonsumsi oleh karnivora. Dimana sulfur bepergian ke seluruh jaringan makanan.

Saat hewan mengusir tinja mereka, sisa -sisa protein dan senyawa lainnya ada belerang. Demikian pula, kematian makhluk hidup adalah cara untuk mengembalikan belerang ke tanah atau (dalam kasus organisme air) ke air.
Saat sekarat, organisme dekomponen menggabungkan belerang dalam bentuk hidrogen sulfida lagi. Kemudian, sulfida mengoksidasi dan membentuk sulfat lagi, yang dapat diserap oleh tanaman.
Ada juga bakteri yang memproses dekomposisi bahan organik di rawa dan melepaskan hidrogen sulfida di udara. Karenanya bau khas area berawa.
Fase hidrologi: sungai, danau, lahan basah, dan lautan
Belerang mencapai tubuh air yang diseret oleh air limpasan yang mencucinya dari tanah. Demikian pula, itu bisa jatuh langsung dari udara dalam bentuk hujan asam.
Itu dapat melayani Anda: ekosistem air dari Meksiko timur lautIni juga dimasukkan ke lautan dari kedalaman laut melalui sumber hidrotermal yang terendam, yang mengeluarkan senyawa yang kaya sulfur.
 Sumber hidrotermal dengan belerang
Sumber hidrotermal dengan belerang Begitu dalam air, digunakan sebagai sumber energi oleh bakteri pemrosesan sulfur dan diserap oleh elemen plankton. Dengan cara ini, itu menembus jaringan makanan, karena bakteri dan plankton dikonsumsi oleh makhluk laut lainnya.
Pentingnya siklus belerang
Siklus belerang sangat penting, karena menjamin daur ulang dan ketersediaan elemen mendasar ini untuk makhluk hidup.
Biologis
Belerang adalah bagian dari asam amino yang merupakan konstituen protein, seperti metionin, sistein dan sistin yang mensintesis tanaman. Serta senyawa fundamental lainnya untuk metabolisme semua makhluk hidup, seperti koenzim.
Demikian pula, belerang adalah bagian dari produksi klorofil yang merupakan senyawa yang memungkinkan untuk mengubah energi matahari menjadi makanan.
Ekonomis
Sulfur unsur memiliki nilai ekonomi yang besar, karena digunakan dalam pembuatan berbagai produk penggunaan industri dan domestik. Di antaranya asam sulfat yang digunakan dalam baterai untuk kendaraan bermotor.
Ini juga digunakan dalam pembuatan bubuk mesiu, dalam pemutihan kertas dan di vulkanisasi ban.
Dampak lingkungan
Senyawa belerang, seperti sulfur dioksida dan sulfur trioksida, yang memancarkan industri, termoelektrik dan kendaraan, adalah polutan. Senyawa ini saat melembabkan di atmosfer membentuk asam sulfat dan asam sulfur yang mengendap sebagai hujan asam.
Proses ini menghasilkan pengasaman badan air dan secara negatif mempengaruhi kehidupan.
Referensi
- Berg, J. M., Stryer, l., & Tymoczko, J. L. (2007). Biokimia. Saya terbalik.
- Calow, hlm. (Ed.) (1998). Ensiklopedia Ekologi dan Manajemen Lingkungan.
- Campbell, m. K., & Farrell, s. SALAH SATU. (2011). Biokimia. Thomson. Brooks/Cole.
- Christopher R. Dan fielding, c.R. (1993). Tinjauan Sedimentologi Sungai. Geologi Sedimen.
- Margalef, r. (1974). Ekologi. Edisi Omega.
- Miller, g. Dan Tyler, J.R. (1992). Ekologi dan Lingkungan. Grup Editorial Iberoamérica.KE. dari c.V.
- Odum, e.P. dan Warrett, G.W. (2006). Dasar -dasar Ekologi. Edisi Kelima. Thomson.