Asam Benzoat (C6H5COOH)
- 3317
- 222
- Jessie Harvey
 Asam Benzoat adalah asam karboksilat aromatik
Asam Benzoat adalah asam karboksilat aromatik Apa itu asam benzoat?
Dia Asam benzoat Itu adalah asam aromatik paling sederhana dari semuanya, memiliki formula molekul C6H5Cooh. Di alam ditemukan di banyak tanaman, terutama dalam buah -buahan seperti aprikot dan blueberry. Ini juga terjadi pada bakteri sebagai produk sampingan dari metabolisme fenilalanin asam amino.
Ini dihasilkan di usus oleh pemrosesan bakteri (oksidatif) dari polifenol yang ada dalam beberapa makanan.
C6H5COOH, tidak seperti banyak asam, senyawa padat, terdiri dari kristal cahaya, putih dan filiform, yang mengeluarkan aroma almond dan karakteristik.
Salah satu kemampuan utama asam benzoat adalah menghambat pertumbuhan ragi, jamur dan beberapa bakteri, sehingga digunakan sebagai pengawet makanan.
Meskipun ini bukan senyawa beracun, ia memiliki beberapa tindakan berbahaya bagi kesehatan. Oleh karena itu, WHO merekomendasikan dosis asupan maksimum 5 mg/kg berat badan/hari, setara dengan asupan harian 300 mg asam benzoat.
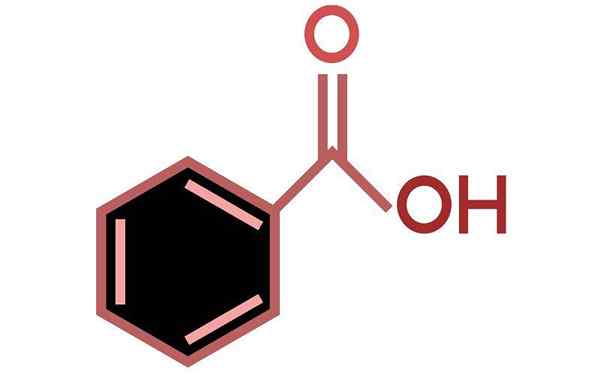
Struktur asam benzoat
 Struktur asam benzoat. Sumber: Wikimedia Commons
Struktur asam benzoat. Sumber: Wikimedia Commons Gambar superior mewakili struktur asam benzoat dalam model bar dan bola.
Jika jumlah bola hitam dihitung, akan diverifikasi bahwa ada enam dari mereka, yaitu, enam atom karbon, dua bola merah sesuai dengan dua atom oksigen dari gugus karboksil, -cooh, dan akhirnya, bola putihnya adalah atom hidrogen.
Di sebelah kiri Anda memiliki cincin aromatik, yang aromatiknya diilustrasikan dengan garis -garis terputus di tengah cincin. Dan di sebelah kanan, kelompok -COOH, yang bertanggung jawab atas sifat asam dari senyawa ini.
Terutama, c6H5COOH memiliki struktur datar, karena semua atomnya (kecuali untuk hidrogen) memiliki hibridisasi SP2.
Di sisi lain, kelompok -COOH, sangat polar, memungkinkan dipol permanen untuk ada dalam struktur.
Fakta ini menghasilkan C6H5COOH dapat berinteraksi dengan dirinya sendiri melalui pasukan dipol-dipolo. Khususnya, dengan jembatan hidrogen khusus.
Jika kelompok -COOH diamati, akan ditemukan bahwa oksigen dari C = O dapat menerima jembatan hidrogen, sedangkan oksigen O -H menyumbangkannya.
Jembatan kristal dan hidrogen
Asam benzoat dapat membentuk dua jembatan hidrogen: menerima dan menerima satu secara bersamaan. Oleh karena itu, ia membentuk dímeros, yaitu molekulnya "terkait" dengan yang lain.
Ini adalah pasangan atau dimer, c6H5COOH-HOOCC6H5, dasar struktural yang mendefinisikan padatan yang dihasilkan dari perencanaannya di luar angkasa.
Dapat melayani Anda: elemen diatomikSifat fisik dan kimia asam benzoat
Nama Kimia
Asam:
-Benzoikum
-Benzenocarboxylic
-Dracyl
-Carboxibenzene
-Benzenophoremical
Formula molekul
C7H6SALAH SATU2 atau c6H5Cooh
Berat molekul
122.123 g/mol.
Deskripsi Fisik
Padat atau dalam bentuk kristal, biasanya putih, tetapi dapat menghadirkan warna krem jika memiliki kotoran tertentu. Kristal -kristalnya adalah skema atau berbentuk jarum.
Bau
Baunya seperti almond dan bagus.
Rasa
Hambar atau sedikit pahit. Batas deteksi rasa adalah 85 ppm.
Titik didih
480º F A 760 mmHg (249 ºC).
Titik lebur
252.3º F (121.5-123.5 ºC).
titik pengapian
250º F (121 ºC).
Sublimasi
Dapat mensublimasikan dari 100 ºC.
Kelarutan air
3.4 g/l a 25 ºC.
Kelarutan dalam pelarut organik
- 1 g asam benzoat larut dalam volume yang sama dengan: 2,3 mL alkohol dingin, 4,5 mL kloroform, 3 mL eter, 3 mL aseton, 30 ml karbon tetraklorida, 10 mL benzena, 30 mL karbon disulfida, dan 2,3 ml minyak treem.
- Ini juga larut dalam oli yang mudah menguap dan tetap.
- Itu sedikit larut dalam eter minyak.
- Kelarutannya di heksano adalah 0,9 g/L, dalam metanol 71,5 g/L, dan dalam toluena 10,6 g/L.
Kepadatan
1.316 g/ml pada 82.4º F, dan 1.2659 g/ml pada 15 ° C.
Kepadatan uap
4,21 (dengan hubungan udara diambil sebagai referensi = 1)
Tekanan uap
1 mmHg pada 205º F dan 7,0 x 10-4 mmHg pada 25 ºC.
Stabilitas
Solusi dengan konsentrasi 0,1% dalam air stabil selama setidaknya 8 minggu.
Penguraian
Ini membusuk dengan menghangatkan, memancarkan asap dan asap yang menjengkelkan.
Zat yang lengket dan kental
1.26 cpoise pada 130 ºC.
Panas pembakaran
3227 kJ / mol.
Panas penguapan
534 kJ /mol pada 249 ºC.
ph
Sekitar 4 di air.
Tegangan permukaan
31 N/M A 130 ºC.
PKA
4.19 hingga 25 ºC.
Indeks bias
1.504-1.5397 (ηd) pada 20 ºC.
Reaksi
- Kontak dengan pangkalan (NaOH, KOH, dll.) Membentuk penjualan benzoat. Misalnya, jika Anda bereaksi dengan naOH, bentuk natrium benzoat, c6H5Jalur.
- Bereaksi dengan alkohol untuk membentuk ester. Misalnya, reaksinya terhadap etil alkohol berasal dari etil ester. Beberapa ester asam benzoat memenuhi fungsi sebagai plasticizer.
- Bereaksi dengan fosfor pentachloride, PCL5, Untuk membentuk klorida benzoil, asam halida. Benzoil chloride dapat bereaksi dengan amonium (NH3) atau amina seperti methylamine (cho3NH2) Untuk membentuk benzamide.
- Reaksi asam benzoat dengan asam sulfat menghasilkan sulfonasi cincin aromatik. Grup fungsional -jadi3H menggantikan atom hidrogen di posisi target cincin.
Itu dapat melayani Anda: revolusi kimia pertama- Ini dapat bereaksi dengan asam nitrat, dengan penggunaan asam sulfat sebagai katalis, membentuk asam meta-nitrobenzoat.
- Di hadapan katalis, seperti besi klorida, FECL3, Asam benzoat bereaksi dengan halogen. Misalnya, ia bereaksi dengan klorin untuk pembentukan asam meta-chlorobenzoic.
Produksi
Beberapa metode produksi senyawa ini:
- Sebagian besar asam benzoat terjadi secara industri dengan mengoksidasi toluena dengan oksigen yang ada di udara. Proses ini dikatalisis oleh bensin kobalt, pada suhu 140-160 ºC dan pada tekanan 0,2-0,3 MPa.
- Toluena dapat terklorinasi untuk menghasilkan benzotriklorida, yang kemudian dihidrolisis dengan asam benzoat.
- Hidrolisis benzonitril dan benzamida, dalam media asam atau alkali, dapat menyebabkan asam benzoat dan basa terkonjugasi.
- Benzyl alkohol dalam oksidasi yang dimediasi oleh kalium permanganat, dalam media berair, menghasilkan asam benzoat. Reaksi terjadi dengan pemanasan atau distilasi refluks. Setelah proses selesai, campuran disaring untuk menghilangkan mangan dioksida, sedangkan supernatan didinginkan untuk mendapatkan asam benzoat.
- Senyawa benzocticloride bereaksi dengan kalsium hidroksida, menggunakan garam besi atau besi sebagai katalis, awalnya membentuk kalsium benzoat, Ca (C (C (C (C (C (C (C (C6H5Mendekut)2. Kemudian garam ini, dengan reaksi dengan asam klorida, diubah menjadi asam benzoat.
Penggunaan asam benzoat
Industrialis
- Ini digunakan dalam produksi fenol dengan dekarboksilasi oksidatif asam benzoat pada suhu 300-400 ºC, karena fenol dapat digunakan dalam sintesis nilon.
- Dari itu glikol benzoat, prekursor kimia dari ester dietilen glikol dan ester trietilen glikol, zat yang digunakan sebagai plasticizer. Mungkin aplikasi plasticizer yang paling penting adalah formulasi perekat. Beberapa ester rantai panjang digunakan untuk melunakkan plastik seperti PVC.
- Ini digunakan sebagai aktivator polimerisasi karet. Selain itu, ini adalah perantara dalam pembuatan resin alquidic, serta aditif untuk aplikasi dalam pemulihan minyak mentah.
- Selain itu, digunakan dalam elaborasi resin, pewarna, serat, pestisida dan sebagai agen pemodifikasi resin poliamida untuk produksi poliester. Ini digunakan untuk pemeliharaan aroma tembakau.
Dapat melayani Anda: garam biner- Ini adalah prekursor klorida Benzoil, yang merupakan bahan awal untuk sintesis senyawa seperti benzil benzoat, digunakan dalam penjabaran rasa buatan dan serangga serangga.
Obat
- Ini adalah komponen dari Whitfield Oint. Salep ini terdiri dari 6% asam benzoat dan asam salisilat 3%.
- Ini adalah bahan dari tingtur benzoine, digunakan sebagai menghirup antiseptik topikal dan dekongestan. Itu digunakan sebagai ekspekoran, analgesik dan antiseptik sampai awal abad ke -20.
- Asam benzoat telah digunakan dalam terapi eksperimental pasien dengan penyakit akumulasi nitrogen residual.
Konservasi makanan
- Asam benzoat dan garamnya digunakan dalam konservasi makanan. Senyawa ini mampu menghambat pertumbuhan jamur, ragi dan bakteri, melalui mekanisme yang bergantung pada pH.
Tidak nyaman
Dapat bereaksi dengan asam askorbat (vitamin C) hadir dalam beberapa minuman, menghasilkan benzena, senyawa karsinogen. Karena itu, senyawa lain sedang dicari dengan kemampuan untuk menghemat makanan yang tidak menghadirkan masalah asam benzoat.
Yang lain
- Ini digunakan dalam kemasan aktif, hadir dalam ionomer. Dari mereka, asam benzoat dilepaskan, mampu menghambat pertumbuhan spesies genera Penicillium Dan Aspergillus Dalam media mikroba.
- Ini digunakan sebagai agen pengawet aroma jus buah dan parfum.
- Asam benzoat digunakan sebagai herbisida selektif untuk mengendalikan gulma dengan lebar dan rumput dalam kacang kedelai, mentimun, melon, kacang dan tanaman ornamen kayu.
Toksisitas
- Kontak dengan kulit dan mata itu dapat menghasilkan kemerahan. Dengan inhalasi dapat menyebabkan iritasi pada pernapasan dan batuk. Asupan sejumlah besar asam benzoat dapat menyebabkan gangguan pencernaan, mampu mencapai hati dan kerusakan ginjal.
- Asam benzoat dan benzoat dapat melepaskan histamin yang dapat menyebabkan reaksi alergi dan iritasi mata, kulit dan selaput lendir.
- Itu tidak memiliki efek kumulatif, mutagenik atau karsinogenik, karena dengan cepat diserap di usus, menghilangkan urin tanpa menumpuk di dalam tubuh.
- Dosis maksimum yang diizinkan menurut WHO adalah 5 mg/kg berat badan/hari, sekitar 300 mg/hari. Dosis toksisitas akut pada manusia: 500 mg/kg.
Referensi
- Asam benzoat. Dipulihkan dari Chemicalbook.com
- Asam benzoat. Pulih dari pubchem.NCBI.Nlm.Nih.Pemerintah
- Asam benzoat. Diterima dari.Wikipedia.org

