Karakteristik Senyawa Kuarter, Pelatihan, Contoh
- 4258
- 1183
- Frederick Pfeffer
Itu Senyawa Kuarter Mereka semua adalah mereka yang memiliki empat atom atau ion yang berbeda. Oleh karena itu, mereka bisa menjadi spesies molekuler atau ionik. Keragamannya mencakup kimia organik dan anorganik, menjadi kelompok yang sangat besar; Meskipun mungkin, tidak begitu banyak dibandingkan dengan senyawa biner atau terner.
Alasan bahwa jumlah Anda lebih kecil adalah karena keempat atom atau ion harus disatukan oleh afinitas kimianya. Tidak semua elemen kompatibel satu sama lain, dan bahkan lebih sedikit ketika dianggap sebagai kuartet; Tiba -tiba beberapa dari mereka lebih terkait satu sama lain daripada dengan pasangan lainnya.
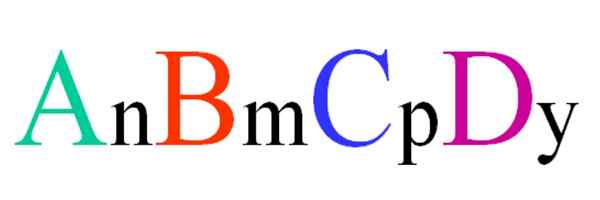 Formula umum dan acak untuk senyawa kuaterner. Sumber: Gabriel Bolívar.
Formula umum dan acak untuk senyawa kuaterner. Sumber: Gabriel Bolívar. Pertimbangkan senyawa kuaterner dari rumus acak ABCD. Subskrip n, m, p e y, adalah koefisien stoikiometri, yang pada gilirannya menunjukkan berapa proporsi masing -masing atom yang ada dalam kaitannya dengan yang lain.
Dengan demikian, formula ANBMCPDDan Itu akan valid jika memenuhi elektroneutralitas. Selain itu, senyawa seperti itu akan dimungkinkan jika keempat atomnya cukup dekat satu sama lain. Akan terlihat bahwa formula ini tidak berlaku untuk banyak senyawa, tetapi terutama untuk paduan atau mineral.
[TOC]
Karakteristik senyawa kuaterner
Bahan kimia
Senyawa kuaterner dapat berupa ionik atau kovalen, menunjukkan karakteristik yang diharapkan untuk sifatnya. Senyawa ionik ABCD diharapkan larut dalam air, alkohol atau pelarut kutub lainnya; Mereka harus memiliki titik mendidih dan fusi yang tinggi, dan menjadi pendorong listrik yang baik saat mereka bergabung.
Mengenai senyawa kovalen ABCD, sebagian besar terdiri dari senyawa organik nitrogen, teroksigenasi atau terhalogenasi; yaitu, formulanya akan menjadi cNHMSALAH SATUPNDan atau cNHMSALAH SATUPXDan, X menjadi atom halogen. Dari molekul -molekul ini, akan logis untuk berpikir bahwa mereka adalah kutub, mengingat tingginya elektronegatifitas o, n dan x.
Dapat melayani Anda: natrium klorida (NaCl)Senyawa ABCD murni kovalen dapat memiliki banyak kemungkinan tautan: A-B, B-C, D-A, dll., Tergantung pada afinitas dan kemampuan elektronik atom. Sedangkan dalam senyawa ABCD murni ionik, interaksinya adalah elektrostatik: a+B-C+D-, Misalnya.
Dalam kasus paduan, dianggap lebih sebagai campuran padat daripada senyawa dengan benar, ABCD terdiri dari atom netral dalam keadaan basal (secara teori).
Dari sisanya, senyawa ABCD bisa netral, asam atau basa, tergantung pada identitas atomnya.
Fisik
Secara fisik, ada kemungkinan bahwa ABCD tidak menjadi gas, karena empat atom yang berbeda selalu melibatkan massa molekul yang lebih besar atau merumuskan. Jika bukan cairan dengan titik didih yang tinggi, itu diharapkan menjadi padatan, yang dekomposisi harus menghasilkan banyak produk.
Sekali lagi, warnanya, bau, tekstur, kristal, dll., Mereka akan tunduk pada bagaimana mereka hidup berdampingan A, B, C dan D dalam senyawa, dan akan tergantung pada sinergi dan struktur mereka.
Tata nama
Sejauh ini masalah senyawa kuaterner telah ditangani dengan cara global dan tidak tepat. Mengesampingkan kimia organik (Amidas, benchilo klorida, garam amonium kuaterner, dll.), Dalam kimia anorganik ada contoh yang ditentukan dengan baik yang disebut okisal asam dan basa.
Oksisal asam
Oxisal asam adalah yang berasal dari netralisasi parsial oksoasid poliprotik. Dengan demikian, satu atau lebih hidrogennya digantikan oleh kation logam, dan hidrogen yang kurang tersisa memiliki, semakin sedikit asam.
Misalnya, asam fosfat, h3PO4, Hingga dua garam asam dapat diperoleh dari, untuk mengatakan, natrium. Ini adalah: nah2PO4 (Na+ menggantikan hidrogen yang setara dengan h+) dan na2HPO4.
Dapat melayani Anda: selenium: sejarah, sifat, struktur, mendapatkan, menggunakanMenurut nomenklatur tradisional, garam -garam ini dinamai serta oksisal (sama sekali tidak terlindungi), tetapi mendahului kata 'asam' dengan nama logam. Jadi, nah2PO4 Itu akan menjadi sodium dease fosfat, dan na2HPO4 Asam natrium fosfat (karena memiliki h memiliki.
Di sisi lain, nomenklatur stok lebih suka menggunakan kata 'hidrogen' yang 'asam'. Nah2PO4 Itu akan menjadi natrium dihidrogen, dan na2HPO4 Hidrogen natrium fosfat. Perhatikan bahwa garam -garam ini memiliki empat atom: na, h, p dan o.
Oxisal dasar
Oxisals dasar adalah yang mengandung anion oh dalam komposisinya-. Misalnya, pertimbangkan Salt Cano3Oh (ca2+ TIDAK3- Oh-). Untuk menamainya, itu akan cukup untuk memberikan kata 'dasar' untuk nama logam. Dengan demikian, namanya: Kalsium nitrat dasar. Dan bagaimana dengan cuio3Oh? Namanya adalah: Cupric Basic Yodato (Cu2+ Io3- Oh-).
Menurut nomenklatur stok, kata 'dasar' digantikan oleh hidroksida, diikuti dengan penggunaan skrip sebelum nama oxoanion.
Mengulangi contoh-contoh sebelumnya, nama mereka adalah untuk masing-masing: kalsium hidroksida-nitrat, dan tembaga hidroksida-andodat (ii); Mengingat bahwa logam valencia harus ditunjukkan dalam tanda kurung dan dengan angka Romawi.
Garam ganda
Pada garam ganda ada dua kation berbeda yang berinteraksi dengan jenis anion yang sama. Misalkan garam ganda: cu3Iman (PO4)3 (Cu2+ Keyakinan3+ PO43-). Ini adalah besi dan tembaga fosfat, tetapi nama yang paling tepat untuk merujuk pada ini adalah: triple copper (II) dan besi (iii) fosfat.
Garam terhidrasi
Ini adalah hidrat, dan satu -satunya perbedaan adalah bahwa pada akhir nama mereka jumlah formulat air ditentukan. Misalnya, MNCL2 Itu adalah mangan klorida (II).
Dapat melayani Anda: benzoine: struktur, sifat, penggunaan dan risikoHidratnya, MNCl2· 4h2O Disebut mangan klorida (ii) tetrahidrat. Perhatikan bahwa ada empat atom yang berbeda: MN, CL, H dan O.
Garam ganda dan terhidrasi yang terkenal adalah Mohr's, Faith (NH4)2(SW4)2· 6h2SALAH SATU. Namanya: Double Iron Sulfate (II) dan hexahidrat amonium.
Pelatihan
Sekali lagi, fokus pada senyawa kuaterner anorganik, kami sebagian besar memiliki produk netralisasi parsial. Jika ini terjadi di hadapan beberapa oksida logam, garam ganda mungkin; Dan jika mediumnya sangat mendasar, oksisal dasar akan mengendap.
Dan jika di samping itu, di sisi lain, molekul air memiliki afinitas untuk logam, mereka akan langsung berkoordinasi dengannya atau dengan ion di sekitarnya, membentuk hidrat.
Di sisi paduan, empat logam atau logam yang berbeda harus dilas untuk pembuatan kapasitor, semikonduktor atau transistor.
Contoh
Akhirnya, daftar dengan berbagai contoh senyawa kuaterner ditunjukkan di bawah ini. Pembaca dapat menggunakannya untuk menguji pengetahuannya tentang nomenklatur:
- Pbco3(OH)2
- CR (HSO4)3
- Nahco3
- Znioh
- Cu2(OH)2Sw3
- Li2Kaso4
- Cuso4· 5h2SALAH SATU
- Agau (jadi4)2
- Kasus4· 2h2SALAH SATU
- FECL3· 6h2SALAH SATU
Referensi
- Shiver & Atkins. (2008). Kimia anorganik. (Edisi keempat). MC Graw Hill.
- Whitten, Davis, Peck & Stanley. (2008). Kimia. (Edisi ke -8.). Pembelajaran Cengage.
- Nomenklatur dan formulasi anorganik. [PDF]. Diperoleh dari: sumber daya.pendidikan.adalah
- Erika thalîa bagus. (2019). Garam ganda. Akademi. Pulih dari: akademi.Edu
- Wikipedia. (2019). Kation amonium kuaterner. Diperoleh dari: di.Wikipedia.org

