Referensi karakteristik elektroda, fungsi, contoh
- 4856
- 837
- Irvin Reichel
Dia elektroda referensi Ini adalah perangkat yang digunakan dalam analisis potensiometrik dan voltamétric untuk penentuan kuantitatif analit. Pentingnya adalah, seperti namanya, untuk berfungsi sebagai referensi untuk memperkirakan nilai sebenarnya dari potensi dalam reaksi semi -elektrokimia.
Potensi semi -media tergantung pada konsentrasi ion yang menarik, karena bereaksi dengan memenangkan atau kehilangan elektron. Dengan cara ini, dimungkinkan untuk menentukan konsentrasi mereka melalui potensi ini. Namun, nilainya tidak absolut tetapi terkait dengan elektroda hidrogen standar (dia dalam bahasa Inggris).
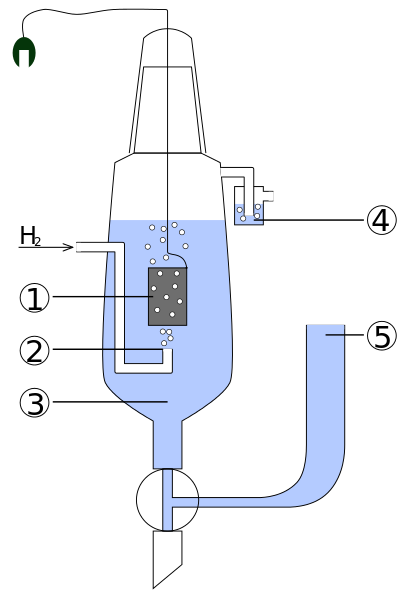
 Diagram bagian -bagian elektro hidrogen standar. Sumber: Standard_hydrogen_electrode.JPG: Kaverinderivevative Work: Henry Muelpfordt/CC BY-S (http: // CreativeCommons.Org/lisensi/by-sa/3.0/)
Diagram bagian -bagian elektro hidrogen standar. Sumber: Standard_hydrogen_electrode.JPG: Kaverinderivevative Work: Henry Muelpfordt/CC BY-S (http: // CreativeCommons.Org/lisensi/by-sa/3.0/) Dengan konvensi, potensial elektroda hidrogen sama dengan 0V. Masalahnya adalah bahwa elektroda ini sulit dimanipulasi, jadi mereka tidak praktis untuk memasangnya di semua analisis. Di sinilah elektroda referensi masuk, jauh lebih sederhana, dan yang potensinya berbeda dari 0V.
Beberapa elektroda referensi, seperti elektroda jenuh Calomel (ESC), dapat dibangun di laboratorium yang sama sebelum analisis dilakukan. Demikian juga, mereka diperoleh secara terbuka di pasar dengan spesifikasi yang tepat, dan risiko mencemari sampel analit minimal.
[TOC]
Karakteristik elektroda referensi
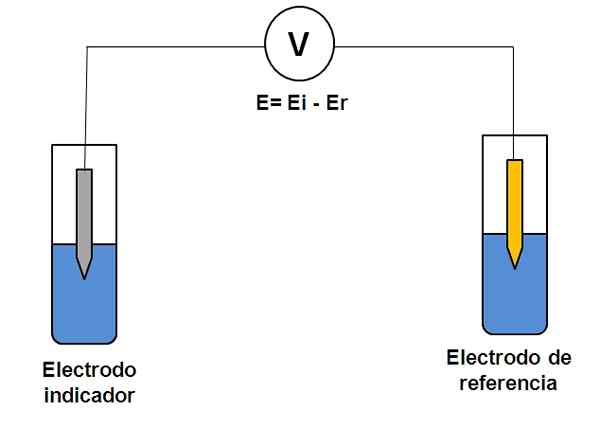 Representasi sederhana dari dua sistem elektroda dalam potensiometri. Sumber: Gabriel Bolívar.
Representasi sederhana dari dua sistem elektroda dalam potensiometri. Sumber: Gabriel Bolívar. Pertimbangkan sistem dua elektroda di atas. Salah satunya adalah indikator (abu -abu), di mana reaksi yang menarik terjadi, dan yang lainnya adalah referensi (emas). Sel elektrokimia ini akan memiliki potensi dan, yang akan sama dengan perbedaan potensi kedua elektroda (EI-E). Oleh karena itu, variasi E harus disebabkan oleh potensi elektroda indikator.
Dapat melayani Anda: kalium sianida (kcn): sifat, penggunaan, struktur, risiko,Dari atas disimpulkan bahwa elektroda referensi memiliki karakteristik berikut:
-Ini memiliki potensi yang stabil selama waktu dan dapat direproduksi. Yaitu, harus sama di mana pun di mana atau berapa kali pengukuran dilakukan.
-Komposisi kimianya konstan dan tidak sensitif, sehingga hampir tidak mengalami perubahan ketika berinteraksi dengan larutan analit atau merendam dirinya dalam media berair.
-Mudah dibangun dan dipasang, tidak seperti elektroda hidrogen standar, yang menuntut penggunaan tangki hidrogen dan berisiko ledakan ketika hidrogen bercampur dengan udara dengan udara.
Elektroda indikator adalah yang sensitif terhadap konsentrasi analit.
Fungsi elektroda referensi
Potensi elektroda referensi diukur terhadap elektroda hidrogen standar, sehingga nilainya berbeda dari 0V. Berkat elektroda hidrogen ini, konstruksi tabel potensial standar dan standar dimungkinkan, yang muncul dalam teks kimia untuk simfin reaksi redoks.
Namun, dalam praktiknya tidak memuat elektroda hidrogen di mana -mana. Sebaliknya, elektroda referensi digunakan, jauh lebih sederhana dan aman untuk dimanipulasi.
Karena potensinya konstan dan stabil, potensi pembacaan sel elektrokimia secara eksklusif disebabkan oleh elektroda indikator; yaitu, variasi konsentrasi analit yang dimaksud.
Dengan demikian, fungsi elektroda referensi adalah untuk menentukan potensi reaksi apa pun di salah satu semi -imit sistem elektrokimia. Jika potensi mereka tidak stabil, maka penentuan kuantitatif analit tidak akan dapat diandalkan. Setiap analisis potensiometrik atau voltametrik harus menentukan elektroda referensi mana yang mereka gunakan untuk melaporkan hasilnya.
Itu dapat melayani Anda: asam brom (hbro2): sifat fisik dan kimia, dan penggunaanContoh elektroda referensi
Ada beberapa elektroda referensi yang tersedia di pasaran. Beberapa digunakan untuk penentuan yang sangat spesifik. Namun, ada dua elektroda di antara semuanya yang menonjol berkat kesederhanaan dan kepraktisannya: elektroda calomel, dan perak-perak-klorida, keduanya sangat berulang dalam banyak analisis potensiometri dan voltamletrik.
Elektroda Calomel
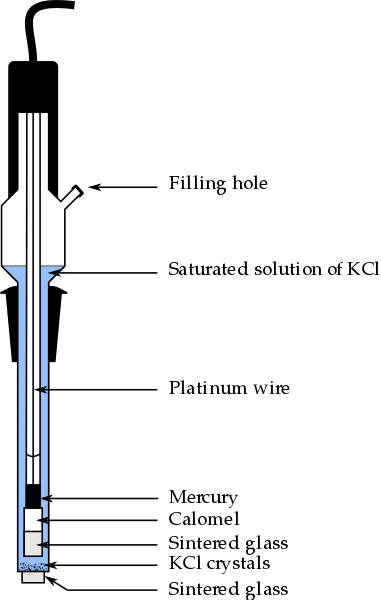 Bagian dari elektroda calomel, salah satu elektroda referensi yang paling banyak digunakan dalam kimia analitik. Sumber: Bachi-Bouzouk melalui Wikipedia.
Bagian dari elektroda calomel, salah satu elektroda referensi yang paling banyak digunakan dalam kimia analitik. Sumber: Bachi-Bouzouk melalui Wikipedia. Pada gambar atas bagian konvensional elektroda kalomel jenuh ditampilkan, ECS. Dikatakan bahwa itu jenuh karena mengandung larutan jenuh KCl (biru), yang juga menyajikan unveunds dari kcl.
Kolom internal, dilalui dengan kawat platinum, diisi dengan merkuri, yang pada gilirannya menghubungi pasta calomel, Hg2Cl2 o Merkurius klorida (I), dan larutan jenuh KCl. Dengan demikian, dalam elektroda ini konsentrasi ion CL adalah penting-, karena nilainya memodifikasi potensi elektroda.
Reaksi yang terjadi adalah sebagai berikut:
HG2Cl2(s) + 2e- ⇌ 2hg (l) + 2cl-
Dan memiliki eº dari 0.241 v.
Di ujung bawah ECS ada goreng berpori, yang diletakkan dalam kontak listrik dengan larutan analit dan memungkinkan pertukaran ion yang dikendalikan-. Kalau tidak, akan ada kontaminasi klorida dalam sampel, dan juga elektroda akan kehilangan larutan KCl jenuh yang berharga.
Elektroda ini digunakan untuk pengukuran pH dan secara umum analit mana pun yang konsentrasinya dapat ditentukan dalam media berair.
Itu dapat melayani Anda: alkohol termal: struktur, sifat, risiko dan penggunaanElektroda perak perak
 Elektro perak perak. Sumber: Tenofalltrades (Talk) (Unggah). / Area publik
Elektro perak perak. Sumber: Tenofalltrades (Talk) (Unggah). / Area publik Mirip dengan elektroda calomel, elektroda perak perak terdiri dari kawat perak yang ditutupi dengan perak klorida, dan juga terendam dalam larutan yang jenuh oleh campuran KCL dan AgCl.
Semua bagiannya dilindungi dalam tabung plastik, yang memiliki lubang berpori yang melaluinya ia menetapkan kontak listrik dengan larutan.
Reaksi yang mendefinisikan potensinya, eº = 0.197 V, adalah sebagai berikut:
Agcl (S) + E- ⇌ Ag (S)+Cl-
Elektroda ini menyajikan penggunaan dan preferensi yang lebih besar daripada Calomel, yang disebabkan oleh dampak negatif merkuri terhadap lingkungan. Di sisi lain, elektroda perak yang padat perak lebih sederhana, aman dan murah untuk dibangun di laboratorium.
Kami mengatakan kemudian bahwa elektroda garpu perak menggantikan Calomel di banyak aplikasinya (derajat potensiometrik, uji korosi, analisis elektrokimia, dll.).
Ini juga merupakan salah satu pilihan yang disukai dalam biologi dan kedokteran, terutama untuk elektrokardiografi dan elektroensefalografi, karena perak atau garamnya adalah zat yang relatif beracun bagi tubuh.
Referensi
- Hari, r., & Underwood, a. (1965). Kimia analitik kuantitatif. (Edisi kelima.). Pearson Prentice Hall.
- Skoog d.KE., Barat d.M. (1986). Analisis instrumental. (Ed kedua.). Inter -American., Meksiko.
- Wikipedia. (2020). Referensi elektroda. Diperoleh dari: di.Wikipedia.org
- Elsevier b.V. (2020). Referensi elektroda. Ilmiah. Diperoleh dari: Scientedirect.com
- Libretteks Kimia. (9 Juni 2020). Elektroda referensi. Pulih dari: chem.Librettexts.org
- « Lokasi Mercusuar Alexandria, Sejarah, Deskripsi, Reruntuhan
- Emily Dickinson Biografi, Prestasi, Pekerjaan, Frasa »

