Fase tersebar
- 1589
- 304
- Ray Thiel
 Sumber: Gabriel Bolívar
Sumber: Gabriel Bolívar Apa fase tersebar?
Itu fase tersebar Itu adalah salah satu yang lebih rendah proporsi dalam dispersi dan terdiri dari agregat partikel yang sangat kecil. Sementara itu, fase yang paling melimpah dan kontinu di mana partikel -partikel berbaring disebut fase dispersing. Contohnya adalah air dengan gula, di mana fase yang tersebar adalah gula dan air yang menyebar.
Dispersi diklasifikasikan sesuai dengan ukuran partikel yang membentuk fase terdispersi, mampu membedakan tiga jenis dispersi: dispersi kasar, solusi koloid dan solusi sejati.
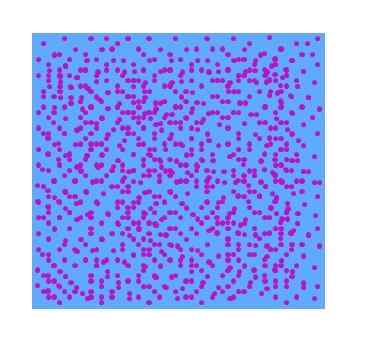
Dalam gambar superior, fase hipotetis yang tersebar dari partikel ungu dalam air dapat terlihat. Akibatnya, gelas yang penuh dengan dispersi ini tidak akan menunjukkan transparansi ke cahaya yang terlihat; Artinya, itu akan terlihat seperti yogurt cair ungu. Jenis dispersi bervariasi tergantung pada ukuran partikel tersebut.
Saat mereka "hebat" (10-7 m) Ada pembicaraan tentang dispersi kasar, dan dapat sedimen dengan aksi gravitasi; solusi koloid, jika ukurannya berkisar antara 10-9 M dan 10-6 M, yang membuat mereka hanya terlihat dengan ultramicroscope atau mikroskop elektronik; dan solusi sejati, jika ukurannya kurang dari 10-9 M, bisa melintasi selaput.
Solusi sejati, oleh karena itu, adalah semua yang populer diketahui, seperti cuka atau air manis.
Karakteristik fase tersebar
Solusi merupakan kasus penyebaran tertentu, ini menjadi sangat menarik bagi pengetahuan tentang fisioquimica makhluk hidup. Sebagian besar zat biologis, baik intraseluler maupun ekstraseluler, ditemukan dalam bentuk dispersi panggilan.
Gerakan Brown dan Efek Tyndall
Partikel -partikel dari fase tersebar dari larutan koloid memiliki ukuran kecil yang menghambat sedimentasi mereka. Selain itu, partikel terus bergerak dalam gerakan acak, bertabrakan satu sama lain, yang juga membuat sedimentasi sulit. Jenis gerakan ini dikenal sebagai Brown.
Dapat melayani Anda: kaca unguKarena ukuran yang relatif besar dari partikel fase terdispersi, solusi koloid memiliki penampilan yang keruh atau bahkan buram. Ini karena cahaya tersebar ketika koloid menyeberang, sebuah fenomena yang dikenal sebagai efek Tyndall.
Heterogenitas
Sistem koloid adalah sistem yang tidak homogen, karena fase terdispersi terdiri dari partikel dengan diameter antara 10-9 M dan 10-6 M. Sedangkan partikel solusi berukuran lebih kecil, biasanya kurang dari 10-9 M.
Partikel -partikel dari fase terdispersi dari larutan koloid dapat melintasi kertas filter dan filter tanah liat. Tetapi mereka tidak dapat melintasi membran dialisis seperti selofan, endotelium kapiler dan colodion.
Dalam beberapa kasus, partikel yang membentuk fase terdispersi adalah protein. Ketika mereka berada dalam fase air, protein terlipat, meninggalkan bagian hidrofilik di luar untuk interaksi yang lebih besar dengan air, melalui gaya ion-dipolo atau dengan pembentukan jembatan hidrogen.
Protein membentuk sistem reticular di dalam sel, mampu mengambil bagian dari dispersan. Selain itu, permukaan protein berfungsi untuk bergabung dengan molekul kecil yang memberikan muatan listrik superfisial, yang membatasi interaksi antara molekul protein, mencegahnya membentuk gumpalan yang menyebabkan sedimentasi.
Stabilitas
Koloid diklasifikasikan sesuai dengan daya tarik antara fase yang tersebar dan fase penyebaran. Jika fase penyebarannya cair, sistem koloid diklasifikasikan sebagai Suns. Ini dibagi lagi menjadi deliphilos dan liofob.
Itu bisa melayani Anda: kalium klorat (kclo3)Koloid liofil dapat membentuk solusi yang benar dan stabil secara termodinamik. Di sisi lain, koloid liofob dapat membentuk dua fase, karena mereka tidak stabil, meskipun stabil dari sudut pandang kinetik. Ini memungkinkan mereka untuk tetap dalam keadaan tersebar untuk waktu yang lama.
Contoh fase tersebar
Baik fase penyebaran dan fase yang tersebar dapat terjadi dalam tiga keadaan fisik materi, yaitu: padat, cair atau gas.
Biasanya, fase kontinu atau menyebar adalah dalam keadaan cair, tetapi koloid yang komponennya ditemukan di negara bagian lain dari agregasi materi dapat ditemukan.
Kemungkinan kombinasi fase dispersing dan fase tersebar dalam keadaan fisik ini adalah sembilan.
Masing -masing akan dijelaskan dengan beberapa contoh masing -masing.
- Solusi solid: Ketika fase penyebaran padat, dapat dikombinasikan dengan fase terdispersi dalam keadaan padat, membentuk solusi padat yang disebut SO.
Ini adalah contoh dari interaksi ini: banyak paduan baja dengan logam lain, beberapa permata berwarna -warni, karet yang diperkuat, porselen dan plastik berpigmen.
- Emulsi solid: Fase dispersing keadaan padat dapat dikombinasikan dengan fase terdispersi cair, membentuk emulsi padat yang disebut SO. Mereka adalah contoh interaksi ini: keju, mentega, dan jeli.
- Busa padat: Fase dispersing sebagai padatan dapat dikombinasikan dengan fase terdispersi dalam keadaan gas, yang merupakan busa padat yang disebut SO. Contoh interaksi ini adalah spons, karet, batu apung dan busa karet.
- Sol dan gel: Fase penyebaran dalam keadaan cair dikombinasikan dengan fase terdispersi dalam keadaan padat, membentuk matahari dan gel. Contoh interaksi ini adalah susu magnesia, lukisan, lumpur dan pudin.
Dapat melayani Anda: solusi peredam kejut- Emulsi: Fase penyebaran dalam keadaan cair dikombinasikan dengan fase terdispersi juga dalam keadaan cair, menghasilkan emulsi yang disebut SO. Contoh interaksi ini adalah susu, krim wajah, saus salad dan mayones.
- Busa: Fase penyebaran dalam keadaan cair dikombinasikan dengan fase terdispersi dalam keadaan gas, membentuk busa. Contoh interaksi ini adalah krim cukur, krim kocok dan busa bir.
- Aerosol padat: Fase penyebaran dalam keadaan gas dikombinasikan dengan fase terdispersi dalam keadaan padat, menyebabkan aerosol padat yang disebut SO. Contoh interaksi ini adalah asap, virus, bahan sel -sel di udara, bahan yang dipancarkan oleh pipa knalpot mobil.
- Aerosol cair: Fase penyebaran dalam keadaan gas dapat dikombinasikan dengan fase terdispersi dalam keadaan cair, yang merupakan semprotan cair yang disebut SO. Contoh interaksi ini adalah kabut, kabut dan embun.
- Solusi sejati: Fase penyebaran dalam keadaan gas dapat dikombinasikan dengan fase gas dalam keadaan gas, membentuk campuran gas yang merupakan solusi yang benar dan bukan sistem koloidal. Contoh interaksi ini adalah udara dan gas pencahayaan.
Referensi
- Whitten, Davis, Peck & Stanley. Kimia (8.ª ed.). Pembelajaran Cengage.
- Toppr (s.F.). Klasifikasi koloid. Pulih dari: toppr.com
- Jiménez Vargas, J dan Macarulla. J. M. (1984). Fisika Fisiologis, Edisi Keenam. Inter -American Editorial.
- Madhusha. Perbedaan antara fase disperseed dan dispersi medum. Pulih dari: pediaa.com

