Kalsium fosfat (CA3 (PO4) 2)

- 4593
- 1153
- Herbert Fritsch
Dia kalsium fosfat Ini adalah garam anorganik dan tersier yang formula kimianya CA3(Po4)2. Formula menetapkan bahwa komposisi garam ini adalah 3: 2 untuk kalsium dan fosfat, masing -masing. Ini dapat dilihat langsung di gambar bawah, di mana kation ditampilkan2+ dan anion po43-. Untuk setiap tiga CA2+ Ada dua PO43- berinteraksi dengan mereka.
Di sisi lain, kalsium fosfat mengacu pada serangkaian garam yang bervariasi tergantung pada rasio CA/P, serta tingkat hidrasi dan pH. Faktanya, ada banyak jenis kalsium fosfat yang ada dan dapat disintesis. Namun, mengikuti surat itu, nomenklatur, kalsium fosfat hanya menyinggung tricycal, yang disebutkan di atas.
 Proporsi dan ion dalam fosfat trisikcal. Sumber: Richard-59 [CC BY-SA 3.0 (https: // createveCommons.Org/lisensi/by-sa/3.0)], dari Wikimedia Commons
Proporsi dan ion dalam fosfat trisikcal. Sumber: Richard-59 [CC BY-SA 3.0 (https: // createveCommons.Org/lisensi/by-sa/3.0)], dari Wikimedia Commons Semua kalsium fosfat, termasuk CA3(Po4)2, Mereka adalah padatan putih dengan nada abu -abu sedikit. Mereka bisa granular, halus, kristal, dan memiliki ukuran partikel yang ada di sekitar mikrometer; Dan bahkan nanopartikel fosfat ini telah disiapkan, yang dengannya bahan biokompatibel untuk tulang dirancang.
Biokompatibilitas ini karena garam ini ditemukan di gigi dan dalam akun pendek di jaringan tulang mamalia. Misalnya, hidroksiapatit adalah kalsium fosfat kristal, yang pada gilirannya berinteraksi dengan fase amorf dari garam yang sama.
Ini berarti bahwa ada fosfat dari kalssio amorf dan kristal. Untuk alasan itu tidak mengherankan keragaman dan banyak opsi saat mensintesis bahan berdasarkan kalsium fosfat; Bahan -bahan yang propertinya setiap hari adalah peneliti yang lebih tertarik di seluruh dunia untuk fokus pada pemulihan tulang.
Struktur kalsium fosfat
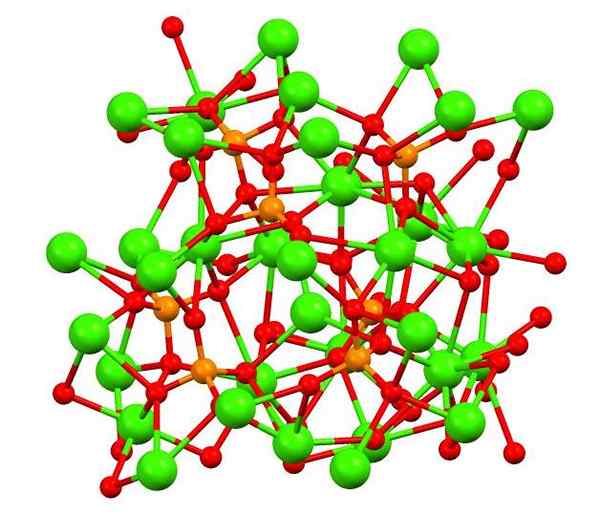 Kalsium fosfat dalam mineral Whitlockita. Sumber: Smokefoot [CC BY-SA 4.0 (https: // createveCommons.Org/lisensi/by-sa/4.0)], dari Wikimedia Commons
Kalsium fosfat dalam mineral Whitlockita. Sumber: Smokefoot [CC BY-SA 4.0 (https: // createveCommons.Org/lisensi/by-sa/4.0)], dari Wikimedia Commons Gambar atas menunjukkan struktur kalibi tribasic fosfat dalam mineral Whitlockita yang aneh, yang dapat mengandung magnesium dan besi sebagai pengotor.
Meskipun pada pandangan pertama mungkin tampak kompleks, perlu untuk mengklarifikasi bahwa model ini mengasumsikan interaksi kovalen antara atom oksigen fosfat dan pusat logam kalsium.
Dapat melayani Anda: beryllium hydride (beh2)Namun, sebagai representasi, ini valid, interaksi adalah elektrostatik; yaitu kation2+ rasakan ketertarikan untuk PO43- (AC2+- O-po33-). Dengan pemikiran ini, dapat dipahami mengapa dalam gambar kalsium (bola hijau) dikelilingi oleh atom oksigen bermuatan negatif (bidang merah).
Ketika ada begitu banyak ion, pengaturan atau pola simetris tidak terlihat terlihat. Ca3(Po4)2 mengadopsi pada suhu rendah (t<1000°C) una celda unitaria correspondiente a un sistema cristalino romboédrico; a este polimorfo se le conoce con el nombre de β-Ca3(Po4)2 (β-TCP, untuk akronimnya dalam bahasa Inggris).
Pada suhu tinggi, di sisi lain, itu menjadi α-Ca polimorf3(Po4)2 (α-TCP), yang sel unitnya sesuai dengan sistem kristal monoklinik. Pada suhu yang bahkan lebih tinggi, polimorf α'-Ca juga dapat terbentuk3(Po4)2, yang merupakan struktur kristal heksagonal.
Kalsium fosfat amorf
Struktur kristal untuk kalsium fosfat telah disebutkan, yang diharapkan dari garam. Namun, ini mampu ditampilkan.
Ketika ini terjadi, dikatakan bahwa kalsium fosfat memiliki struktur amorf (ACP, Kalsium fosfat amorf). Beberapa penulis menunjuk pada jenis struktur ini sebagai bertanggung jawab atas sifat biologis CA3(Po4)2 Dalam jaringan tulang, perbaikan dan biomimetisasi dimungkinkan.
Sisa keluarga
Kalsium fosfat sebenarnya adalah keluarga senyawa anorganik, yang pada gilirannya dapat berinteraksi dengan matriks organik.
Fosfat lain diperoleh "cukup" mengubah anion yang menyertai kalsium (PO43-, HPO42-, H2PO4-, Oh-), seperti jenis kotoran di padatan. Dengan demikian, hingga sebelas kalsium atau lebih fosfat, masing -masing dengan struktur dan sifatnya sendiri, dapat berasal secara alami atau artifisial.
Beberapa fosfat dan struktur kimianya masing -masing dan formula akan disebutkan di bawah ini:
-Hidrogen dihydrado kalsium fosfat, cahpo4∙ 2H2O: Monoklinik.
Dapat melayani Anda: amonium oksalat-Dihydrogen monohidrasi kalsium fosfat, CA (H2PO4)2∙ h2O: Triclinic.
-Anhydrous Dease Phosphate, CA (H2PO4)2: Triclinic.
-Hidrogen octacalcic phosphate (OCP), CA8H2(Po4)6: Triclinic. Ini adalah prekursor dalam sintesis hidroksiapatit.
-Hydroxyapatite, CA5(Po4)3OH: Heksagonal.
Sifat fisik dan kimia
Nama
-Kalsium fosfat
-Tricalcium fosfat
-Diposfat trikcal
Berat molekul
310.74 g/mol.
Deskripsi Fisik
Itu adalah padatan putih.
Rasa
Hambar.
Titik lebur
1670 ºK (1391 ºC).
Kelarutan
-Praktis tidak larut dalam air.
-Tidak larut dalam etanol.
-Larut dalam asam klorida dan asam nitrat encer.
Kepadatan
3.14 g/cm3.
Indeks bias
1.629
Entalpi pelatihan standar
4126 kkal/mol.
Suhu penyimpanan
2-8 ºC.
ph
6-8 dalam suspensi berair 50 g/L kalsium fosfat.
Pelatihan
Kalsium dan hidrogen nitrat amonium fosfat
Ada banyak metode untuk memproduksi atau membentuk kalsium fosfat. Salah satunya terdiri dari campuran dua garam, CA (tidak3)2∙ 4H2Atau, dan (nh4)2HPO4, sebelumnya dilarutkan dalam alkohol dan air absolut, masing -masing. Satu garam berkontribusi kalsium, dan yang lainnya fosfat.
Dari campuran ini, ACP mengendap, yang kemudian mengalami pemanasan dalam oven pada suhu 800 ° C dan selama 2 jam. Sebagai hasil dari prosedur ini, β-CA diperoleh3(Po4)2. Mengontrol suhu, agitasi, dan waktu kontak dengan hati -hati, pembentukan nanokristal dapat terjadi.
Untuk membentuk polimorf α-Ca3(Po4)2 Perlu memanaskan fosfat di atas 1000 ° C. Pemanasan ini dilakukan dengan adanya ion logam lainnya, yang menstabilkan polimorf ini cukup sehingga dapat digunakan pada suhu kamar; yaitu, tetap dalam keadaan target yang stabil.
Kalsium hidroksida dan asam fosfat
Kalsium fosfat juga dapat dibentuk dengan mencampur kalsium hidroksida dan larutan asam fosfat, terjadi netralisasi asam-basa asam. Setelah setengah hari pematangan dalam roh induk, dan penyaringan, mencuci, mengeringkan dan menyaring, debu granular fosfat amorf, ACP diperoleh.
Produk reaksi ACP ini dari suhu tinggi, berubah menurut persamaan kimia berikut:
2ca9(HPO4) (Po4)5(Oh) => 2ca9(P2SALAH SATU7)0,5(Po4)5(Oh) + h2O (A t = 446.60 ° C)
2ca9(P2SALAH SATU7)0,5(Po4)5(Oh) => 3ca3(Po4)2 + 0,5 jam2O (A t = 748.56 ° C)
Dapat melayani Anda: selenium: sejarah, sifat, struktur, mendapatkan, menggunakanDengan cara ini β-CA diperoleh3(Po4)2, Polimorf Anda yang paling umum dan stabil.
Aplikasi
Di jaringan tulang
Ca3(Po4)2 Ini adalah konstituen anorganik utama dari abu tulang. Ini adalah komponen transplantasi penggantian tulang, ini dijelaskan oleh kesamaan kimianya dengan mineral yang ada di tulang.
Biomaterial kalsium fosfat digunakan untuk memperbaiki cacat tulang dan dalam menutupi prostesis logam. Kalsium fosfat disimpan pada mereka, mengisolasi mereka dari lingkungan dan memperlambat proses korosi titanium.
Semen Bioceramic
Kalsium fosfat semen (CPC) adalah bioceramic lain yang digunakan dalam perbaikan jaringan tulang. Diuraikan dengan mencampur debu dari berbagai jenis kalsium fosfat dengan air, membentuk pasta. Pasta dapat disuntikkan atau disesuaikan dengan cacat tulang atau rongga.
Semen dibentuk, secara bertahap diserap kembali dan digantikan oleh tulang yang baru terbentuk.
Dokter
-Ca3(Po4)2 Ini adalah garam dasar, jadi digunakan sebagai antasid untuk menetralkan kelebihan keasaman lambung dan meningkatkan pH. Pada pasta gigi memasok sumber kalsium dan fosfat untuk memfasilitasi proses remineralisasi gigi dan hemostasis tulang.
-Ini juga digunakan sebagai suplemen gizi, meskipun cara paling ekonomis untuk memasok kalsium adalah dengan menggunakan karbonat dan sitratnya.
-Kalsium fosfat dapat digunakan dalam pengobatan tethany, hipokalsemia laten dan terapi pemeliharaan. Selain itu, ini berguna dalam suplementasi kalsium selama kehamilan dan menyusui.
-Ini digunakan dalam pengobatan kontaminasi dengan radioaktif radioaktif (RA-226) dan strontium (SR-90). Kalsium fosfat menghalangi penyerapan isotopo radioaktif di saluran pencernaan, sehingga membatasi kerusakan yang disebabkan oleh mereka.
Yang lain
-Kalsium fosfat digunakan sebagai pakan untuk burung. Selain itu, digunakan dalam pasta gigi dalam kontrol tartar.
-Ini digunakan sebagai zat anti -gendera, misalnya untuk mencegah garam meja menjadi compacte.
-Ini berfungsi sebagai agen pemutihan tepung. Sementara itu, dalam mentega cochino mencegah warna yang tidak diinginkan dan meningkatkan kondisi penggorengan.
Referensi
- Kalsium fosfat. Pulih dari: pubchem.NCBI.Nlm.Nih.Pemerintah
- Kalsium fosfat. Sains Direct. Diperoleh dari: Scientedirect.com

