Struktur, sifat dan penggunaan magnesium hidrida
- 4673
- 1131
- Miss Wm Hudson
Dia Magnesium hidrida (MGH2 dari formula molekul), ini adalah senyawa kimia dengan kandungan berat hidrogen dari 7.66%, dan ditemukan di alam sebagai padatan kristal putih. Ini terutama digunakan untuk menyiapkan zat kimia lainnya, meskipun juga telah dipelajari sebagai potensi penyimpanan rata -rata untuk hidrogen.
Itu milik keluarga hidror saline (atau ionik), yang ditentukan oleh ion yang dimuat secara negatif. Hidrida ini dianggap yang terbentuk dari logam alkali dan logam alkali yang menakutkan, tetapi dalam kasus magnesium (dan berilium) mereka memiliki serikat kovalen, selain ionik yang menjadi ciri keluarga hidros ini.
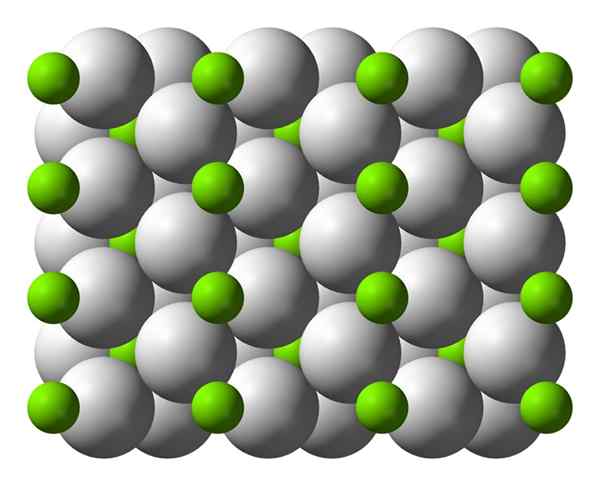
 Model sel magnesium hidrida kesatuan, MGH2.
Model sel magnesium hidrida kesatuan, MGH2. [TOC]
Persiapan dan formula
Magnesium hidrida terbentuk melalui hidrogenasi langsung magnesium logam (Mg) dalam kondisi tekanan dan suhu tinggi (200 atmosfer, 500 ° C) dengan katalis MGI2. Reaksi Anda setara dengan:
Mg+h2→ MGH2
Produksi MGH juga telah diselidiki2 pada suhu yang lebih rendah dengan penggunaan magnesium nanokristalin yang diproduksi di pabrik bola.
Ada juga metode persiapan lain, tetapi mereka mewakili reaksi kimia yang lebih kompleks (hidrogenasi magnesium-antrasena; reaksi antara dietilmagnesium dengan lithium-aluminium hidrida; dan sebagai produk dari kompleks MGH kompleks MGH2).
Struktur kimia
 Struktur kristal magnesium hidrida
Struktur kristal magnesium hidrida Atom ini memiliki struktur rutilo pada suhu kamar, dengan struktur kristal tetragonal. Ini memiliki setidaknya empat bentuk yang berbeda dalam kondisi tekanan tinggi, dan struktur non-lembar telah diamati dengan defisiensi hidrogen; Yang terakhir hanya disajikan dalam jumlah partikel yang sangat kecil saat membentuk.
Seperti disebutkan di atas, tautan yang ada dalam struktur rutilo memiliki sifat kovalen sebagian alih -alih murni ionik, seperti hidro saline lainnya.
Ini menyebabkan atom magnesium memiliki bentuk bulat, benar -benar terionisasi, tetapi ion hidrida adalah struktur yang memanjang.
Sifat magnesium hidrida
Properti fisik
- Penampilan: Kristal Putih.
- Massa Molar: 26.3209 g/mol
- Kepadatan: 1.45 g/cm3
- Titik fusi: 285 ° C dipecah
- Kelarutan: dalam air itu rusak.
Senyawa kimia ini memiliki berat molekul 26.321 g/mol, kepadatan 1.45 g/cm³ dan memiliki titik fusi 327 ºC.
Sifat kimia
- Prekursor untuk pembuatan bahan kimia lainnya.
- Penyimpanan hidrogen, sebagai sumber energi yang memungkinkan.
- Agen reduksi dalam sintesis organik.
Penting untuk menunjukkan bahwa senyawa ini tidak dapat dibawa ke keadaan cair, dan ketika diambil atau titik lelehnya atau diperkenalkan dalam air, ia membusuk. Hidrida ini tidak larut dalam eter.
Ini adalah zat yang sangat reaktif dan sangat mudah terbakar, dan juga piroforik, yaitu, dapat meradang secara spontan di udara. Ketiga kondisi ini mewakili risiko keamanan yang akan disebutkan di bagian terakhir artikel ini.
Penggunaan/Aplikasi
Penyimpanan hidrogen
Magnesium hidrida bereaksi dengan mudah dengan air untuk membentuk gas hidrogen, melalui reaksi kimia berikut:
MGH2+2h2O → 2H2+Mg (oh)2
Selain itu, zat ini terurai pada suhu 287 ºC dan 1 tekanan batang, sebagai berikut:
MGH2→ mg+h2
Oleh karena itu, penggunaan magnesium hidrida sebagai sarana penyimpanan hidrogen untuk penggunaannya dan transportasi telah diusulkan.
Hidrogenasi dan dehidrogenasi sejumlah magnesium logam dinaikkan sebagai cara transportasi.
Reaksi hidrogenasi dan dehidrogenasi
Meskipun suhu dekomposisi magnesium hidrida merupakan batasan untuk digunakan, metode telah dinaikkan untuk meningkatkan kinetika reaksi hidrogenasi dan dehidrogenasi. Salah satunya adalah dengan pengurangan ukuran partikel magnesium dengan penggunaan pabrik bola.
Dapat melayani Anda: sistem tidak homogenLumpur
Selain itu, suatu sistem telah dinaikkan yang menghasilkan magnesium hidrida berbentuk lumpur (lebih mudah dikelola dan pasti dalam debu atau partikel padat lainnya), yang akan direaksikan dengan air untuk mendapatkan hidrogen yang diinginkan.
Diperkirakan bahwa lumpur yang ditentukan sebelumnya akan dibentuk oleh hidrida yang ditumbuk halus, dilindungi dengan lapisan pelindung minyak dan ditangguhkan dalam agen yang tersebar untuk memastikan bahwa ia mempertahankan konsistensi tanpa kehilangan material, dan bahwa ia tidak menyerap kelembaban lingkungan.
Lumpur ini memiliki keuntungan yang dapat dipompa melalui diesel, bensin atau pompa air umum, membuat proposal ekonomi ini selain efisien.
Sel bahan bakar
Magnesium hidrida dapat diimplementasikan dalam produksi sel bahan bakar canggih, dan juga dalam penciptaan baterai dan penyimpanan energi.
Transportasi dan energi
Selama dekade terakhir, penggunaan hidrogen telah dianggap sebagai sumber energi. Implementasi hidrogen sebagai bahan bakar, membutuhkan menemukan sistem penyimpanan yang aman dan reversibel dan dengan kapasitas volumetrik tinggi (jumlah hidrogen per unit volume) dan gravimetri (jumlah hidrogen per unit massa).
Alkilasi
Alco3R) senyawa organik dalam media dasar, di mana ada adanya kelompok -OH dalam konsentrasi rendah dan suhu lebih tinggi dari titik leleh hidrida.
Dalam hal ini hidrogen hadir dalam magnesium hidrida (MGH2), Mereka bergabung dengan grup -OH yang membentuk air. Magnesium bebas dapat menerima halogen yang sering menyertai molekul alquilis yang dimaksudkan untuk menyatukan rantai hidrokarbon.
Risiko
Reaksi air
Seperti yang telah disebutkan, magnesium hidrida adalah zat yang bereaksi dengan sangat mudah dan keras dengan air, menghadirkan kemampuan untuk mengeksploitasi dalam konsentrasi utama.
Dapat melayani Anda: Garam Dasar: Formula, Properti, Nomenklatur, ContohIni terjadi karena reaksi eksotermiknya menghasilkan panas yang cukup untuk memicu gas hidrogen yang dilepaskan dalam reaksi dekomposisi, yang mengarah ke reaksi berantai yang cukup berbahaya.
Itu piroforis
Magnesium hidrida juga piroforik, yang berarti dapat menyalakan api secara spontan di hadapan udara lembab, dan membentuk oksida magnesium dan air.
Penghirupannya dalam keadaan padat atau kontak dengan uapnya tidak dianjurkan: zat dalam keadaan alami dan produk dekomposisi dapat menyebabkan cedera serius atau bahkan kematian.
Ini dapat menghasilkan solusi korosif yang bersentuhan dengan air dan kontaminasi. Kontak kulit dan mata tidak dianjurkan, dan juga menimbulkan iritasi pada selaput lendir.
Belum ditunjukkan bahwa magnesium hidrida dapat menghasilkan efek kesehatan kronis, seperti kanker, cacat reproduksi atau konsekuensi fisik atau mental lainnya, tetapi penggunaan peralatan perlindungan saat memanipulasi itu direkomendasikan (terutama respirator atau topeng, dengan karakter bubuk halus).
Saat bekerja dengan zat ini, kelembaban udara pada tingkat rendah harus dipertahankan, matikan semua sumber pengapian dan mengangkutnya dalam drum atau wadah lainnya.
Anda harus selalu menghindari bekerja dengan konsentrasi besar zat ini ketika dapat dihindari, karena kemungkinan ledakan menurun secara signifikan.
Jika tumpahan magnesium hidrida disajikan, area kerja harus diisolasi dan debu dengan alat vakum harus diisolasi. Anda tidak boleh menggunakan metode penyapuan kering; meningkatkan kemungkinan beberapa reaksi dengan hidrida.
Referensi
- Zumdahl, s. S. (1998). Encyclopedia Britannica. Diambil dari Britannica.com.
- Pubchem. (2005). Pubchem Open Chemistry Database. Diambil dari pubchem.NCBI.Nlm.Nih.Pemerintah.
- Safe Hydrogen, L. (2006). Kongres Mobil Hijau. Diambil dari GreencarConress.com.
- Bahan Kimia, c. (N.D.). Cameo Chemicals. Diambil dari cameochemical.NOAA.Pemerintah.
- Layanan, n. J. (1987). Departemen Kesehatan dan Layanan Senior New Jersey. Diambil dari NJ.Pemerintah.
- « Kelahiran Sungai Kuning, Tur, Mulut, Flora
- Dekolonisasi dalam sejarah, penyebab dan konsekuensi Asia »

