Logam
- 4991
- 347
- Domingo Gutkowski
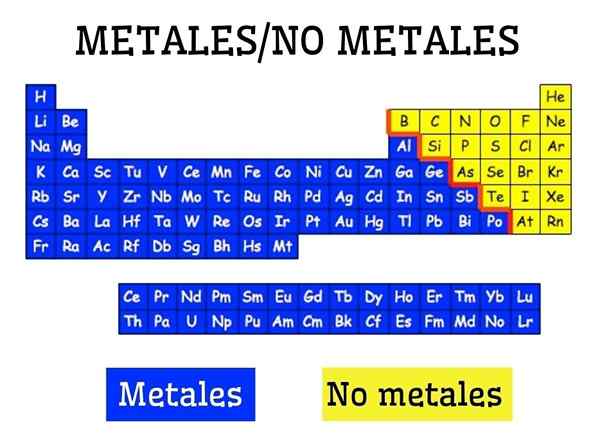
 Logam dan non -logam dalam tabel periodik elemen
Logam dan non -logam dalam tabel periodik elemen Apa itu logam?
Logam dibentuk oleh sekelompok elemen yang terletak di sisi kiri, dengan pengecualian hidrogen non -logam, dari tabel periodik. Logam merupakan sekitar 75 % elemen kimia, sehingga dapat dinyatakan bahwa sebagian besar alam adalah logam.
Logam yang awalnya dituntut oleh pria dalam prasejarah adalah sebagai berikut: emas, perak, tembaga, timah, timah dan besi. Ini karena fakta bahwa mereka asli atau kemudahan pemrosesan mereka untuk melakukan objek utilitas.
Tampaknya masalah sihir dari banyak batu dan mineral dapat diekstraksi tubuh berkilau dan perak (dengan pengecualian penting dan luar biasa). Begitulah kasus bauksit dan aluminium, yang tanah liatnya terurai logam ini dalam piring atau kertas perak diperoleh.
Logam adalah kerangka industri; Pengkabelan, reaktor, unit, wadah, semuanya dengan cara tertentu terdiri dari logam dan paduannya.
Dengan logam koin pertama, senjata, alat, baju besi dibuat, dan kemudian digunakan dalam pembuatan kendaraan, sepeda, kapal, pesawat terbang, komputer, di antara benda -benda yang sangat diperlukan dalam kehidupan modern.
Sejarah
Usia tembaga
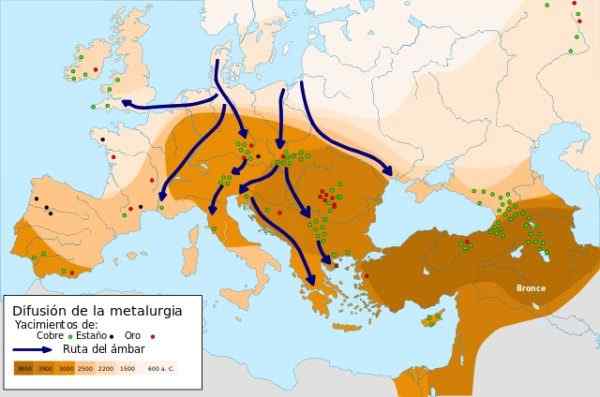 Ekspansi Metalurgi - Sumber: Difusi Metalurgi.SVG di bawah Lisensi 4 Creative Commons Attribution-Compartyrigual 4 4.0 Internasional
Ekspansi Metalurgi - Sumber: Difusi Metalurgi.SVG di bawah Lisensi 4 Creative Commons Attribution-Compartyrigual 4 4.0 Internasional Dalam 9000 a.C. Objek logam pertama tembaga yang ditempa di Timur Dekat dijabarkan, ketika pria itu menemukan bahwa ketika tembaga itu memalu ia meningkatkan kekuatan dan perlawanannya, menggunakannya untuk pembuatan pisau. Ini adalah usia tembaga.
Ditemukan bahwa tembaga dapat diperoleh melalui pemanasan mineral biru, seperti Corvellita dan Malachite (4000-3000.C.).
Periode Calcolithic adalah periode waktu yang mendahului Zaman Perunggu, sesuai dengan 5000-3000 hingga.C. Pria itu mulai bereksperimen dengan fusi dan pengecoran tembaga, untuk mendapatkan tembaga yang ditempa dari tembaga oksida.
Zaman Perunggu (3000-1500 a.C.)
 Bahan Zaman Perunggu - Sumber: Gaguilella di bawah Lisensi Creative Commons -Shareigual 4 4.0 Internasional.
Bahan Zaman Perunggu - Sumber: Gaguilella di bawah Lisensi Creative Commons -Shareigual 4 4.0 Internasional. Pria itu secara tidak sengaja memulai elaborasi paduan, awalnya tembaga dan arsenik, dan kemudian dengan tembaga dan timah untuk mendapatkan perunggu di Timur Dekat.
Artikel perunggu, yang sesuai dengan waktu ini, memiliki 87 % tembaga, 11 % timah dan sejumlah kecil zat besi, arsenik, nikel, timah dan antimonis.
Zaman Besi (700 a.C.)
Pria itu menggunakan pengalamannya dalam produksi tembaga palsu untuk produksi besi tempa di Timur Dekat. Dalam periode waktu yang sama ada granulasi debu Etrusco, Italia.
Produksi baja pertama yang diketahui, paduan besi dan karbon, memanifestasikan dirinya dalam potongan logam di situs arkeologi di Anatolia (1800 hingga.C.)
Dapat melayani Anda: gravimetri: analisis gravimetri, metode, penggunaan dan contohMenuju 1122 d.C., Pada tanggal dan tempat yang tidak diketahui, besi cor diperkenalkan. Pada 1440 d.C. Bell hebat Beijing diproduksi, Cina. Hampir tiga abad kemudian, pada 1709 D.C., Besi cor diproduksi menggunakan Coke sebagai bahan yang mudah terbakar.
Pada 1779 besi cor di Inggris digunakan sebagai bahan arsitektur. Pada tahun 1855, Henry Bessenir menggunakan Arrabio sebagai bahan baku untuk mendapatkan baja lunak. The English Clark and Wood (1872) mematenkan paduan, saat ini dianggap sebagai stainless steel.
Sifat fisik logam
 Perunggu lonceng kuno ini menunjukkan kegunaan logam untuk tujuan hias atau agama. Sumber: Pxhere.
Perunggu lonceng kuno ini menunjukkan kegunaan logam untuk tujuan hias atau agama. Sumber: Pxhere. Di antara beberapa sifat fisik logam yang kami miliki:
-Logam brilian dan mampu memantulkan cahaya.
-Secara umum, mereka adalah konduktor listrik dan panas yang baik.
-Mereka memiliki titik fusi dan didih yang tinggi.
-Mereka dapat ditempa, yaitu, mereka dapat dipalu untuk menghasilkan lembaran tebal rendah.

-Mereka ulet, dengan mereka dapat membuat kabel atau serat dengan diameter sangat sedikit.
-Mereka disajikan dalam keadaan padat, dengan pengecualian merkuri bahwa pada suhu kamar dalam keadaan cair, dan gallium, yang meleleh hanya dengan mengencangkan di tangan di tangan. Pada gambar berikut Anda dapat melihat wadah merkuri:

-Mereka adalah tubuh buram, lembaran tipis mereka tidak disilangkan oleh cahaya.
-Mereka memiliki kekerasan besar, kecuali untuk natrium dan kalium yang dapat dipotong oleh pisau.
-Mereka memiliki kepadatan tinggi, menjadi osmium dan iridium tertinggi, dan lithium dengan kepadatan terendah.
Sifat kimia logam
Di antara beberapa sifat kimia logam yang kami miliki:
-Mereka cenderung kehilangan elektron dan membentuk kation logam, mN+, di mana n menunjukkan angka oksidasi, yang hanya untuk logam alkali dan alkalis bertepatan dengan bilangan valensinya.
-Elektronegativitasnya rendah.
-Mereka berlari dan mengalami kerusakan oksidasi.
-Mereka membentuk oksida dasar saat bereaksi dengan oksigen. Oksida ini bila dikombinasikan dengan air membentuk logam hidroksida. Oksida logam bereaksi dengan asam untuk membentuk garam dan air.
-Mereka adalah agen pereduksi yang baik, karena mereka menghasilkan elektron mereka.
Jenis logam
Logam diklasifikasikan sebagai yang berikut ini: alkali, alkali-trial, pasca-transisional, transisional dan apa yang disebut tanah jarang.
Logam Alkali

Mereka biasanya tidak menemukan diri mereka bebas di alam karena mereka mengoksidasi dengan mudah. Memiliki suborbital1 Di lapisan orbital eksternal, sehingga mereka memiliki keadaan oksidasi +1. Mereka adalah logam yang bereaksi secara eksotermis dengan air dan sangat berkurang.
Logam Alkali-Térreos
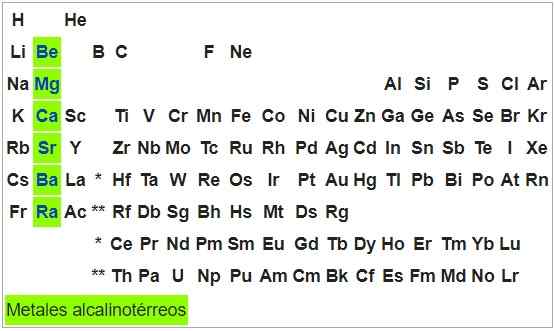
Mereka adalah logam yang dapat ditempa dan ulet. Atom -atom elemen grup ini memiliki konfigurasi S2, Jadi mereka dapat menghasilkan dua elektron dan status oksidasi mereka adalah +2. Dengan pengecualian berilium, mereka dapat dioksidasi untuk paparan udara.
Dapat melayani Anda: karbon alotropLogam posttransisi
Mereka adalah logam dari blok P yang disebut SO, yang terletak di antara logam transisi dan logam di tabel periodik.
Unsur -unsur kelompok 3 memiliki keadaan oksidasi +1 dan +3 sebagai yang paling umum, meskipun aluminium hanya menyajikan keadaan oksidasi +3. Ini juga merupakan bagian dari logam post -transisi yang terletak di Grup 14 dan 15.
Logam transisi d
Mereka membentuk kelompok antara elemen bentuk basa dan pengatur asam. Orbital atom D dan f tidak lengkap dan sedang diisi. Meskipun istilah logam transisi mengacu pada logam transisi d.
Logam transisi memiliki lebih dari satu keadaan oksidasi. Mereka memiliki fusi dan titik mendidih lebih tinggi dari kelompok logam lainnya. Logam transisi adalah kelompok logam yang sangat heterogen yang mencakup, antara lain, besi, kromium, perak, dll.
Tanah jarang
 Mineral Bumi Jarang
Mineral Bumi Jarang Kelompok logam ini terdiri dari unsur -unsur Scandio dan Ititrio dan unsur -unsur serangkaian lantanida dan aktinid. Istilah 'bumi jarang' mengacu pada fakta bahwa mereka tidak ditemukan di alam dalam keadaan murni dan dapat dilampirkan oleh asam.
Penggunaan/aplikasi logam
Logam Alkali
Lithium digunakan sebagai sarana perpindahan panas di beberapa reaktor nuklir. Ini digunakan dalam beberapa baterai kering dan akumulator dengan berat kecil. Klorida dan lithium bromida adalah senyawa higroskopis yang digunakan dalam proses pengeringan industri dan pendingin udara.
Sodium digunakan dalam metalurgi logam, seperti titanium dan zirkonium. Ini digunakan dalam pencahayaan publik dalam lampu busur natrium. Sodium chloride (NaCl) digunakan sebagai rasa makanan dan pelestarian daging.
Logam Alkalineter
Magnesium digunakan dalam fotografi sebagai lampu kilat dan kembang api. Barium adalah komponen paduan yang digunakan dalam busi karena kemudahan elemen untuk memancarkan elektron. Garam barium digunakan untuk membatasi kerusakan yang disebabkan oleh x -rays di pelat saluran pencernaan.
Kalsium digunakan untuk menghilangkan kotoran yang dilarutkan dalam logam cair dan dalam penghapusan gas residu dalam tabung vakum. Itu adalah bagian dari plester, bahan yang digunakan dalam konstruksi dan dalam pengobatan patah tulang.
Logam posttransisi
Aluminium karena logam ringan digunakan dalam konstruksi pesawat terbang dan kapal. Ini juga digunakan dalam elaborasi berbagai peralatan dapur. Ini digunakan sebagai bahan baku dalam pembuatan deodoran yang membatasi keringat.
Dapat melayani Anda: solusi persentaseGallium digunakan dalam transistor dan termometer untuk suhu tinggi. Isotop 67GA digunakan dalam pengobatan dalam pengobatan beberapa melanoma. Timbal digunakan dalam pembangunan baterai dan perlindungan terhadap radiasi pengion.
Logam Transisi
Tembaga digunakan dalam pipa pasokan air, di lemari es dan sistem pendingin udara. Ini juga digunakan sebagai bagian dari mekanisme disipasi panas komputer. Ini digunakan dalam konduksi arus listrik, dalam elektromagnet dan dalam warna kaca.
Nikel digunakan dalam elaborasi stainless steel, serta string gitar dan baterai isi ulang. Ini juga digunakan dalam galvanoplasti dalam perlindungan logam. Ini digunakan dalam paduan yang ditemukan di beberapa bagian kendaraan, seperti katup, bantalan dan rem.
Nikel telah digunakan, untuk waktu yang lama dalam elaborasi koin.
Seng digunakan dalam perlindungan logam korosi, dalam produksi kuningan. Seng oksida dan seng sulfat digunakan dalam pembuatan pelat yang digunakan di atap, selokan dan downspouts.
Kromium digunakan dalam perlindungan korosi logam dan persediaan bersinar. Ini digunakan sebagai katalis dalam reaksi sintesis amonia (NH3). Kromium oksida digunakan dalam perlindungan kayu.
Tanah jarang
Skandi ini digunakan dalam aluminium aluminium untuk komponen aerospace. Ini adalah aditif di lampu uap merkuri.
Lantano digunakan dalam refraksi tinggi dan kaca yang tahan alkalis. Selain itu, digunakan dalam pembuatan lensa kamera dan sebagai cairan katalis katalitik untuk kilang minyak.
Cerio digunakan sebagai agen kimia. Selain itu, ini digunakan untuk pasokan kaca kuning dan warna keramik, serta katalis untuk tungku mandiri.
Contoh elemen logam
Alkali
Sodium (NA), kalium (k), cesio (CS), lithium (Li) dan rubidium (RU).
Alkali-Terreos
Berilium (BE), magnesium (mg), kalsium (CA), strontium (MR), barium (BA) dan radio (RA).
Posttransitional
Aluminium (Al), Gallium (GA), India (dalam), Talio (TL), Tin (Sn) dan Lead (PB).
Transisi
Titanium (Ti), Vanadium (V), Chrome (CR), Mangan (MN), Besi (Faith), Cobalt (CO), Nikel (Ni), Tembaga (Cuinc), Zinc (Zn), Zirkonium (ZR), Niobio (nb), molybdenum (mo), paladio (pd), perak (ag), volframium (w), renio (re), osmio (os), iridido (IR),
Platinum (PT), Emas (AU) dan Merkurius (HG).
Tanah jarang
Scandio (SC), Itrio (Y), Lantano (LA), Cerio (CE), Praseodimio (PR), Neodymium (ND), Samarium (SM), Europio (UE), Gadolinio (GD), Holmio (HO), Erbio (ER), Tulio (TM), ITERBIO (YB) dan Luthacio (LU).
Referensi
- Whitten, Davis, Peck & Stanley. (2008). Kimia. (Edisi ke -8.). Pembelajaran Cengage.
- Shiver & Atkins. (2008). Kimia anorganik. (Edisi keempat). MC Graw Hill.
- Helmestine, Anne Marie, PH.D. (5 Oktober 2019). Logam versus non -logam. Pulih dari: thinkco.com
- Logam dan sifatnya-fisik dan kimianya. [PDF]. Pulih dari: csun.Edu
- Jonathan Master. (2019). 18 jenis logam (fakta dan penggunaan). Pulih dari: makeitfrommetal.com

