Radikal menyewa bagaimana mereka terbentuk, nomenklatur, contoh
- 4523
- 561
- Jessie Harvey
Itu Sewa Radikal Mereka adalah satu set molekul yang tidak stabil yang berasal dari hilangnya hidrogen alkana. Mereka ditandai dengan memiliki elektron yang hilang, sehingga mereka bereaksi dengan cepat untuk menyelesaikan oktet valencia atom tempat ia berada.
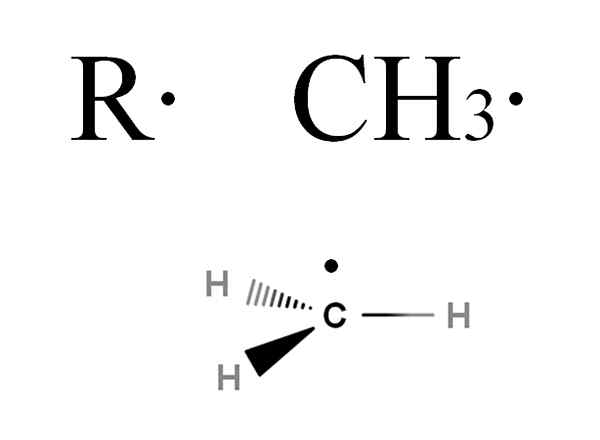
Radikal ini dilambangkan dengan huruf r, seperti halnya kelompok sewa, tetapi dengan perbedaan bahwa suatu titik ditambahkan, r ·. Poin ini menunjukkan keberadaan elektron menghilang. Misalnya, pertimbangkan gas metana, cho4. Alkana ini, kehilangan salah satu hidrogennya, akan diubah menjadi radikal metil, cho3· (Gambar di bawah).
 Formula umum alkil radikal dan metil radikal. Sumber: Gabriel Bolívar via Molview.
Formula umum alkil radikal dan metil radikal. Sumber: Gabriel Bolívar via Molview. Jika Anda ingin memperdalam sedikit tentang struktur radikal ch3·, Akan terlihat bahwa elektronnya yang hilang berada pada sudut tegak lurus terhadap tautan C-H; Artinya, terletak di orbital P murni. Oleh karena itu, cho3· Mengadopsi hibridisasi SP2, serta, secara umum, dengan alkil radikal lainnya.
Radikal ini adalah landasan reaksi berantai di mana alkana berpartisipasi, seperti halnya halogenasi mereka: klorinasi, bromasi, dll. Ada radikal pertama, ke -2 dan ke -3, serta vinil dan alilik, masing -masing dengan stabilitas masing -masing dan kemudahan pelatihan.
[TOC]
Bagaimana radikal membentuk alkil?
Reaksi "lebih sederhana" yang terbentuk radikal adalah halogenasi alkana. Untuk membentuk, reaksi berantai harus diberikan, yang hanya terjadi pada suhu tinggi (melebihi 250 ºC), atau di bawah insiden sinar ultraviolet pada suhu kamar.
Dapat melayani Anda: natrium sulfit (Na2SO3)Pertimbangkan klorinasi metana di bawah salah satu kondisi yang disebutkan di atas:
Cl2 → 2Cl ·
Energi yang disediakan sudah cukup untuk memecahkan tautan CL-Cl dari molekul klorin, terjadi istirahat homolitik; yaitu, setiap atom klorin tetap dengan salah satu elektron tautan. Oleh karena itu, dua radikal terbentuk.
Kemudian, cl radikal menyerang molekul metana:
Cl · + ch4 → hcl + ch3·
Dan metil radikal muncul. Ch3· Ini sangat tidak stabil, jadi akan segera bereaksi untuk memenangkan elektron tambahan yang akan muncul satu -satunya elektron:
Ch3· + Cl2 → Ch3Cl + cl ·
Yang terbentuk akan bereaksi dengan molekul metana lain dan siklus akan diulang lagi dan lagi. Saat metana habis, reaksi berikut akan terjadi yang akan mengakhiri reaksi berantai:
Cl · + · Cl → Cl2
Ch3· + · Cho3 → Ch3Ch3
Ch3· + · Cl → ch3Cl
Stabilitas relatif
Ch3
Metana bukan satu -satunya alkana yang "diradikalisasi" dengan klorinasi. Itu juga terjadi sama dengan etana, propana, butana, dan isomer lainnya. Namun, yang bervariasi adalah energi yang diperlukan yang harus disediakan sehingga radikal cl · dehidrogasi molekul alkana. Dalam kasus radikal metil, sangat tidak stabil dan, oleh karena itu, sulit dibentuk.
Jadi, cho radikal3Ch2· Ini lebih stabil dan mudah dibentuk daripada cho3·. Karena? Karena ch radikal3Ch2· Ini adalah primer, 1, yang berarti bahwa elektron yang hilang berada pada atom karbon yang terkait dengan karbon lain. Sementara itu, Cho3Segera terkait dengan atom hidrogen.
Dapat melayani Anda: fluoride: riwayat, sifat, struktur, memperoleh, risiko, penggunaanTentang apakah ini? Mengingat representasi sebelumnya, elektron yang hilang terletak di orbital P, tegak lurus terhadap tautan lainnya. Di ch3·, Atom hidrogen hampir tidak menyumbangkan kepadatan elektronik ke atom karbon, dalam upaya untuk mengimbangi kurangnya elektron lain.
1st
Di ch3Ch2·, Di sisi lain, karbon dengan elektron yang hilang terkait dengan dua hidrogen dan gugus metil. Akibatnya, karbon ini menerima kepadatan elektronik yang lebih besar, yang membantu menstabilkan elektron menghilang sedikit. Penjelasan yang sama berlaku untuk radikal alkynd pertama lainnya.
2nd
Dalam alquil sekunder atau ke -2 radikal, seperti radikal isopropil, (ch3)2C. Oleh karena itu, lebih stabil daripada radikal 1 dan metil.
3
Kami juga memiliki radikal alkynd tersier atau ke-3, seperti radikal ter-butyl radikal3)3C ·. Ini lebih stabil daripada yang pertama dan ke -2. Sekarang, ada tiga kelompok berkarbonasi yang berbeda dari atom hidrogen yang menstabilkan elektron yang hilang.
Allylic dan Vinyl
Perlu juga disebutkan radikal allylic, cho2= CH-CH2·, Dan vinil, cho2= Ch ·.
Alilic adalah yang paling stabil dari semuanya. Ini karena elektron yang hilang bahkan mampu pindah ke atom karbon dari ujung lainnya. Vínilico, di sisi lain, adalah yang paling tidak stabil dari semua, karena kelompok Cho2=, lebih banyak asam, menarik kepadatan elektronik ke arah dirinya sendiri alih -alih menyumbangkannya ke karbon dengan elektron menghilang.
Dapat melayani Anda: hydroxide timbal: struktur, sifat, penggunaan, risikoSingkatnya, stabilitas relatif radikal alkynd, dari tertinggi ke terendah, adalah: adalah:
Alilo> 3rd> 2nd> 1st> vinyl
Tata nama
Nomenklatur alkil radikal adalah sama dengan untuk remedie. Jadi, cho3Ch2· Disebut etil radikal; dan ch radikal3Ch2Ch2Ch3, N-butil.
Sewa Radikal Utama
Radikal alkil utama bertepatan dengan kelompok alkil: mereka adalah yang memiliki kurang dari enam atom karbon. Oleh karena itu, radikal berasal dari metana, etana, propana, butana dan pentano, adalah yang paling umum. Demikian juga, vinil radikal dan alilicos adalah bagian dari daftar ini.
Radikal alkynd lain yang lebih jarang ditemukan adalah yang berasal dari cycloalcanos, seperti cyclobutane, cyclobutane atau cyclopentano.
Pada gambar berikut beberapa radikal ini diwakili dengan huruf yang ditugaskan:
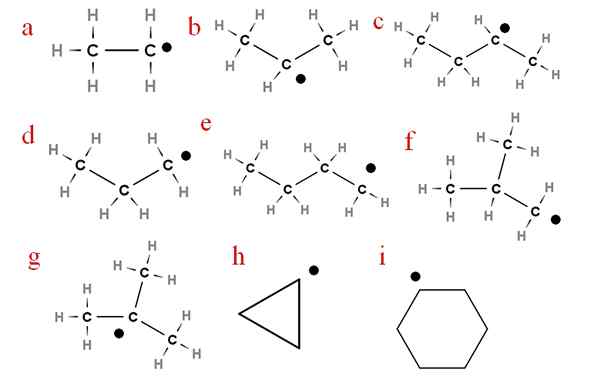 Sembilan radikal alchery terpenting. Sumber: Gabriel Bolívar.
Sembilan radikal alchery terpenting. Sumber: Gabriel Bolívar. Dimulai dengan huruf 'A', kami memiliki:
-A, etil radikal
-B, radikal isopropil
-C, radikal secbutyl
-D, propil radikal
-E, radikal N-butil
-F, radikal isobutil
-G, ter-butyl radical
-H, sikropilus radikal
-I, cyclohexil radikal
Masing -masing radikal ini mungkin atau mungkin tidak memiliki hidrogen mereka digantikan oleh kelompok lain, sehingga mereka sama -sama bervariasi sebagai alkana dan isomer strukturalnya.
Referensi
- Morrison, r. T. dan boyd, r, n. (1987). Kimia organik. Edisi ke -5. Editorial Addison-Wesley Inter-American.
- Carey f. (2008). Kimia organik. (Edisi Keenam). MC Graw Hill.
- Graham Solomons t.W., Craig b. Fryhle. (2011). Kimia organik. (Edisi ke -10.). Wiley Plus.
- Wikipedia. (2020). Alkil. Diperoleh dari: di.Wikipedia.org
- Libretteks Kimia. (5 Juni 2019). Struktur radikal alkil: hyperconjugation. Pulih dari: chem.Librettexts.org

