Struktur radio, sifat, penggunaan, mendapatkan
- 1517
- 342
- Frederick Pfeffer
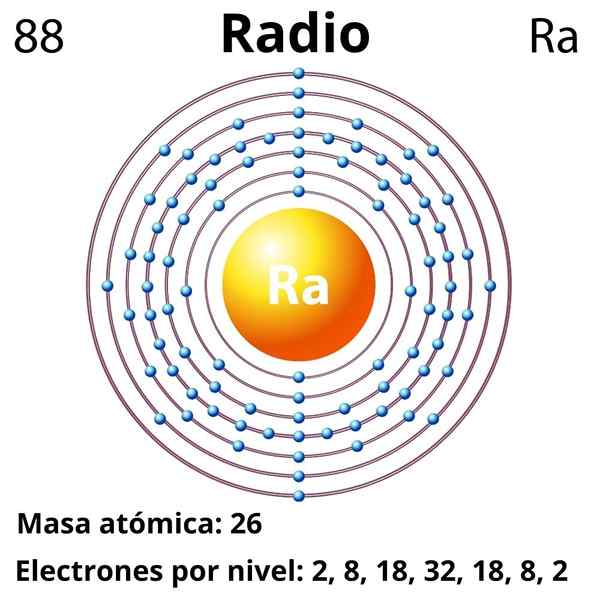
Dia radio Ini adalah elemen logam milik kelompok 2 dari tabel periodik, logam alkalinotherrous, yang simbol kimianya adalah RA. Ini adalah anggota terakhir dari grup ini, yang terletak di bawah barium, dan elemen radioaktif sebelumnya seperti thorium dan uranium; Namun, jari -jari itu sekitar satu juta kali lebih banyak radioaktif dan, oleh karena itu, lebih berbahaya daripada uranium itu sendiri.
Ini adalah elemen yang dikelilingi oleh cerita yang luar biasa dan tidak menguntungkan, semua sebagai akibat dari ketidaktahuan efek negatifnya pada kesehatan. Kecerahan kebiruan dari garam dan solusi berair mereka memikat para ilmuwan Pierre dan Marie Curie, yang menemukannya pada tahun 1898 menganalisis radiasi yang tidak dapat dijelaskan dan kuat dari sampel bijih Pechblenda, yang telah menghilangkan kandungan uranium dan uranium mereka dan kandungan uranium mereka dan kandungan uranium mereka dan kandungan uranium mereka dan kandungan uranium mereka dan kandungan uranium mereka dan kandungan uranium mereka dan kandungan uranium mereka dan kandungan uranium dan uranium mereka dan uranium telah menghilangkan uranium dan uranium mereka dan kandungan uranium mereka dan kandungan uranium mereka dan kandungan uranium dan uranium mereka dan kandungan uranium mereka dan kandungan uranium dan uranium telah menghilangkan uranium dan uranium mereka dan uranium mereka dan uranium telah menghilangkan kandungan uranium dan uranium mereka dan uranium mereka dan kandungan uranium dan uranium telah menghilangkan uranium dan uranium mereka Polonium.
 Ilustrasi oleh Marie Curie, penemu radio
Ilustrasi oleh Marie Curie, penemu radio Menghilangkan uranium dan polonium, curie dan menyimpulkan bahwa ada elemen lain yang ada di Pechblenda, yang bertanggung jawab atas radiasi yang kuat, yang dapat diukur dengan cerdik. Elemen baru ini secara kimiawi sangat mirip dengan barium; Namun, tidak seperti garis hijau spektralnya, garis -garisnya adalah warna carmine.
Dengan demikian, setelah memproses, memurnikan dan menganalisis berton -ton Pechblenda, mereka memperoleh 0.1 mg racl2. Pada saat itu, pada tahun 1902, mereka telah menentukan massa atom radio, yang namanya berasal dari kata Latin 'jari -jari', yang berarti 'ray'. Radio secara harfiah adalah elemen yang bersinar.
Delapan kemudian, pada tahun 1910, Marie Curie bersama dengan ahli kimia Prancis André Louis Debierne, berhasil mengisolasi jari -jari dalam bentuk logam mereka dengan elektrolisis racl2 menggunakan merkuri. Demam penelitian lahir, yang kemudian menjadi sensasi komersial, budaya dan obat yang mengkhawatirkan.
[TOC]
Struktur
Radio adalah logam yang atomnya sangat besar. Konsekuensi dari ini adalah bahwa kristal mereka sedikit padat (meskipun sedikit lebih dari bario), dan mengadopsi struktur kubik yang berpusat pada tubuh (BCC). Di luar struktur ini, tidak ada alotrop lain yang dilaporkan ke suhu atau tekanan lain.
Konfigurasi elektronik

Konfigurasi elektronik untuk radio adalah sebagai berikut:
[Rn] 7s2
Itu teroksidasi dengan kemudahan yang sangat besar untuk menjadi kation ra2+, yang isolektronik ke gas radon mulia. Oleh karena itu, semua senyawa jari -jari mengandung kation ra2+, membangun interaksi ionik yang dominan; Namun, diperkirakan ada kemungkinan bahwa, karena efek relativistik, dapat membentuk tautan dengan karakter kovalen luar biasa (RA-X).
Dapat melayani Anda: kalium benzoat: struktur, sifat, mendapatkan, penggunaanProperti Radio
 Sampel senyawa radio
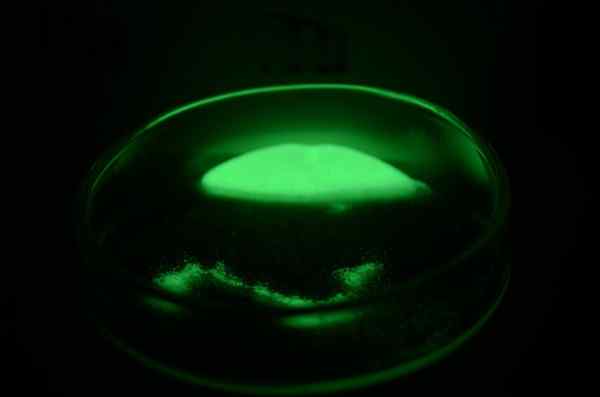
Sampel senyawa radio Penampilan fisik
Radio adalah logam putih perak, yang segera pewarna kuning dan gelap saat bereaksi dengan nitrogen dari udara untuk membentuk nitruro, ra3N2. Karena begitu sulit untuk dimanipulasi, ada beberapa karakteristik fisik jari -jari yang telah ditentukan secara langsung.
Nomor atom
88
Masa molar
226.03 g/mol
Titik lebur
Sekitar 700 ºC. Besarnya ini belum dapat ditentukan dengan tepat.
Titik didih
Radio mendidih antara 1100 dan 1700 ºC. Margin ketidakakuratan yang hebat ini mencerminkan, sekali lagi, komplikasi memanipulasi logam yang tidak stabil seperti itu.
Kepadatan
5.5 g/cm3
Panas fusi
8.5 kJ/mol
Panas penguapan
113 kJ/mol
Keadaan oksidasi
Radio memiliki keadaan oksidasi +2 tunggal.
Elektronegativitas
0.9. Nilai ini dengan setia sesuai dengan karakter elektropositif yang kuat dari jari -jari.
Energi ionisasi
Pertama: 509.3 kJ/mol
Kedua: 979 kJ/mol
Radioaktivitas
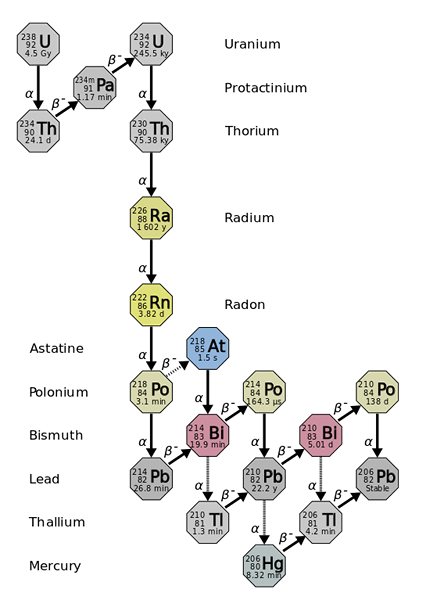 Radius berasal dari penurunan radioaktif dari elemen yang lebih berat dan lebih tidak stabil, seperti halnya isotop uranium-238. Sumber: Pengguna: Tosaka, CC oleh 3.0, via Wikimedia Commons
Radius berasal dari penurunan radioaktif dari elemen yang lebih berat dan lebih tidak stabil, seperti halnya isotop uranium-238. Sumber: Pengguna: Tosaka, CC oleh 3.0, via Wikimedia Commons Radiusnya sekitar satu juta kali lebih banyak radioaktif daripada uranium. Ini terutama karena fakta bahwa isotop lain diproduksi darinya, seperti 222RN (gambar superior), yang pada gilirannya meluruh dengan memancarkan partikel α untuk berubah menjadi isotop 218PO. Sampel radio karenanya mengeluarkan sejumlah besar partikel α dan β-, serta sinar γ.
Misalnya, gram radio, menderita 3.7 · 1010 Disintegrasi per detik, ukuran yang berfungsi untuk mendefinisikan unit CI, yang disebut curie. Energi ini cukup untuk memanaskan sampel 25 gram air 1 ° C per jam.
Jika rantai peluruhan diamati, akan terlihat bahwa isotop awal, 238U, Anda memiliki file T1/2 dari 4.5 Giga tahun (miliaran tahun); sementara itu sebaliknya, 226Ra memiliki a T1/2 1600 tahun, yang juga menghasilkan isotop dengan T1/2 hanya beberapa hari, menit dan detik.
Radioaktivitas radio dan senyawanya adalah pengion, jadi zat fluoresen, bahkan atom di sekitarnya, menyala di malam hari, menjadi mampu memicu reaksi peledak. Properti ini dikenal sebagai radioluminesensi.
Senyawa dan reaktivitas
Saat garam atau senyawa radio dipanaskan di lebih ringan mereka menembakkan api carmine. Padatan seperti itu biasanya putih atau tidak berwarna, tetapi berwarna kuning diwarnai dan akhirnya menjadi lebih gelap sebagai akibat dari radioaktivitas atom radio. Jika mereka memiliki kotoran barium, mereka dapat menunjukkan nada merah muda.
Dapat melayani Anda: reaksi substitusi gandaKimia radio sangat mirip dengan Bario, seolah-olah mereka adalah dua saudara yang tidak terpisahkan, Ra-Ba. Keduanya membentuk garam yang sama, tidak larut dalam air, dengan perbedaan bahwa jari -jari sedikit lebih tidak larut. Misalnya, radio sulfat, satin4, Lebih tidak larut daripada barium sulfat, baso4; Faktanya, itu adalah sulfat paling tidak larut yang pernah diketahui: 2.1 mg larut hanya dalam 1 liter air.
Di sisi lain, Radio Hydroxide, RA (OH)2, Itu adalah yang paling larut dan dasar dari semua hidroksida dari rekan -rekan mereka.
Dalam solusi, kation ra2+, Alih -alih berperilaku seperti asam Lewis, mereka adalah dasar, karena ukurannya yang besar membuat tidak mungkin bagi molekul.
Analogi kimia antara radio dan barium kembali ke logam ini sulit dipisahkan, karena garamnya secara copresipitate dengan yang dari barium.
Penggunaan/Aplikasi Radio
Jam tangan bercahaya
 Jam tangan bercahaya dan fosfor sangat diinginkan pada abad kesembilan belas, untuk daya tarik visual mereka dan untuk berisi radio yang terkenal dalam lukisan mereka. Sumber: Weapon95, CC BY-SA 3.0, via Wikimedia Commons
Jam tangan bercahaya dan fosfor sangat diinginkan pada abad kesembilan belas, untuk daya tarik visual mereka dan untuk berisi radio yang terkenal dalam lukisan mereka. Sumber: Weapon95, CC BY-SA 3.0, via Wikimedia Commons Penggunaan jari -jari yang paling populer dan kontroversial adalah digunakan sebagai aditif untuk lukisan jam tangan. Atom -atomnya dimasukkan ke dalam formulasi pucat seng sulfida, Zns, yang menyerap emisi radioaktif untuk melepaskan cahaya hijau dan fosfor. Cat itu diaplikasikan pada tangan jam (gambar superior).
Masalah penggunaan ini adalah dalam paparan radioaktif yang berkelanjutan yang mempengaruhi pengguna jam tangan ini; Atau lebih buruk lagi, kepada para pekerja yang melukisnya di pabrik.
Pada tahun 1924, beberapa karyawan yang bekerja di industri cat, yang kemudian dikenal sebagai Radio Girls (Radium Girls), mulai menderita kanker tulang, deformasi rahang dan kehilangan gigi mereka, karena mereka harus menjilat ujung kuas Anda untuk menjadi mampu menerapkan cat radioaktif pada jam.
Ini, ditambah ketidaktahuan jari -jari, dan sedikit etika tidak memaksakan langkah -langkah perlindungan yang menjamin keselamatan pekerja, berakhir dengan skandal hukum yang merevolusi undang -undang keamanan kerja kerja.
Dapat melayani Anda: sewa halogenuros: properti, mendapatkan, contohLukisan radio berhenti diproduksi pada tahun 1960; Meskipun hari ini ada beberapa spesimen koleksi yang memilikinya di permukaannya.
Radithor
 Botol Radithor dipamerkan di Museum Nasional Ilmu dan Sejarah Nuklir, New Mexico. Sumber: Sam LaRussa dari Amerika Serikat, CC BY-SA 2.0, via Wikimedia Commons
Botol Radithor dipamerkan di Museum Nasional Ilmu dan Sejarah Nuklir, New Mexico. Sumber: Sam LaRussa dari Amerika Serikat, CC BY-SA 2.0, via Wikimedia Commons Radithor adalah salah satu dari banyak produk farmasi dan kosmetik yang menyatakan efisiensi radio untuk melawan seribu dan satu orang sakit. Itu berisi kuantitas radio mikrometrik, yang harus menyembuhkan semua penyakit pencernaan dan endokrin. Namun, pada tahun 1932, setelah kematian Eden Byers, salah satu konsumen yang paling kuat, Radithor meninggalkan pasar.
Radioterapi
Tidak semua penggunaan radio adalah sensasional, pseudoscientific dan tidak bermoral (atau penjahat). Ada juga sangat bermanfaat bagi kesehatan, setidaknya sampai beberapa waktu. Garam Radio, Racl2 dan Rab2, Mereka digunakan dalam pengobatan kanker, khususnya kanker tulang.
Isotop 223Ra, saat bingung oleh ion kalsium dalam metabolisme, akhirnya menghancurkan sel kanker yang terletak di tulang.
Namun, banyak penggunaan terapeutik jari -jari telah digantikan oleh isotop yang lebih aman, ekonomi dan efisien, seperti 60CO dan 137CS.
Memperoleh
Radio adalah salah satu elemen yang produksinya langka: hanya sekitar 100 gram per tahun di seluruh dunia. Ton uranium oranye, seperti bijih Pechblenda (atau Uraninite) diproses mengikuti metode Curie, yang terdiri dalam mengolah sampel dengan natrium hidroksida, asam hidroklorat dan natrium karbonat, sehingga campuran radio dan barium sulfat, satin4-Baso4.
Campuran satin4-Baso4 Itu diubah menjadi klorida masing -masing, racl2-Bacl2, memisahkan kation ra2+ dengan kristalisasi fraksional dan akhirnya memurnikan teknik kromatografi ionik. Racl2 Itu dikurangi dengan elektrolisis, atau menguranginya dengan aluminium logam menjadi 1200 ºC.
Isotop
Semua isotop radio bersifat radioaktif. Empat dari mereka ada di alam sebagai produk dari peluruhan radioaktif atom 232Th, 235U dan 238ATAU.
Keempat isotop ini adalah: 223RA (T1/2= 11.4 hari), 224RA (T1/2= 3.64 hari), 226RA (T1/2= 1600 tahun) dan 228RA (5.75 tahun). Jelas, hampir semua atom radio terdiri dari campuran isotop 226Ra dan 228Ra, karena orang lain hancur dengan cepat.
Dia 226RA adalah yang paling stabil dari semua isotop radio, yang lainnya terlalu tidak stabil T1/2 Kurang dari dua jam.
Referensi
- Shiver & Atkins. (2008). Kimia anorganik. (edisi keempat). MC Graw Hill.
- Wikipedia. (2020). Radium. Diperoleh dari: di.Wikipedia.org
- Para editor Eeritlopaedia Britannica. (2020). Radium. Dipulihkan dari: Britannica.com
- Radioaktivitas. (S.F.). Radium: Inti radioaktif yang membuat sejarah. Pulih dari: radioaktivitas.UE.com
- Cantrill, v. (2018). Realitas radium. Nature Chem 10, 898. doi.org/10.1038/S41557-018-0114-8
- Elsevier b.V. (2020). Radium. Ilmiah. Diperoleh dari: Scientedirect.com
- « Faktor erosi angin, jenis, konsekuensi, contoh
- Geografi Semenanjung Italia, Negara, Flora, Fauna, Iklim »

