Solusi hipertonik
- 2140
- 415
- Joseph Nader PhD
Kami menjelaskan apa solusi hipertonik, karakteristiknya, apa gunanya, perbedaan dengan hipotonik dan memberikan beberapa contoh
Banyak yang akan terkejut mengetahui bahwa cara tanaman menyerap air melalui akarnya dan cara di mana jari -jari tangan keriput saat mandi di air laut, mereka terkait erat.
Kedua hal terjadi berkat keberadaan membran yang berfungsi sebagai filter, dan solusi hipertonik yang benar -benar menyedot air melalui itu. Tapi apa itu solusi hipertonik?
Dalam artikel ini, pertanyaan ini akan dijawab, dan karakteristik yang paling relevan dari solusi hipertonik juga akan disajikan, untuk apa mereka, bagaimana mereka dibedakan dari jenis solusi lain dan beberapa contoh yang sama.
Apa itu solusi hipertonik?
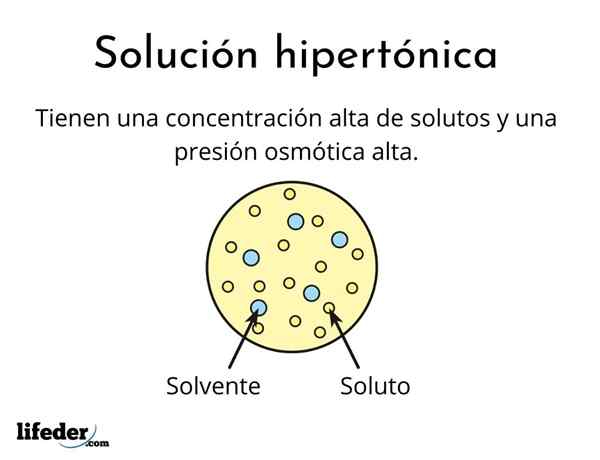
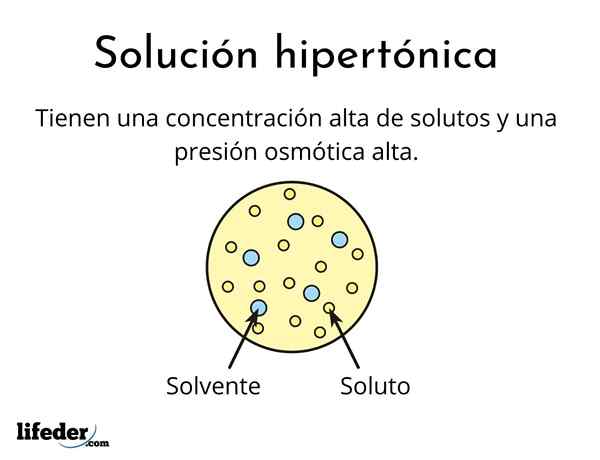
A solusi hipertonik Ini adalah salah satu yang mengandung konsentrasi total zat terlarut aktif osmolar lebih besar dari solusi referensi lain. Osmolally aktif berarti bahwa zat terlarut tidak dapat melintasi jenis membran khusus (mirip dengan kain) yang bertindak sebagai saringan atau filter, yaitu, biarkan air lewat, dan bukan pada partikel zat terlarut.
Konsentrasi zat terlarut yang tinggi ini menyebabkan solusi hipertonik memiliki tekanan osmotik yang tinggi. Tekanan inilah yang secara praktis menyedot air melalui membran, yang disebut osmosis.
Kata hipertonik berasal dari awalan Yunani hiper-, yang berarti "di, atau di atas" dan "nada", yang berarti ketegangan, atau tekanan, sehingga hipertonik secara harfiah berarti "bahwa ia memiliki tekanan atau ketegangan yang lebih besar".
Penting untuk diingat bahwa, dalam biologi dan kedokteran, asalkan ada pembicaraan tentang larutan hipertonik, itu mengacu pada solusi yang lebih terkonsentrasi daripada larutan yang terkandung dalam darah, yang disebut plasma darah darah.
Karakteristik solusi hipertonik
Solusi hipertonik memiliki beberapa karakteristik dasar:
Mereka dibentuk oleh pelarut dan setidaknya satu zat terlarut
Tidak ada solusi yang bisa hipertonik, meskipun begitu terkonsentrasi. Zat terlarut tidak dapat melintasi membran, sementara air harus dapat melewatinya tanpa masalah, jika tidak, tekanan osmotik tidak dihasilkan.
Mereka memiliki konsentrasi zat terlarut yang tinggi
Inilah yang membuat mereka solusi hipertonik. Seperti yang disebutkan beberapa saat yang lalu, solusi hipertonik lebih terkonsentrasi daripada darah.
Itu dapat melayani Anda: distilasi fraksional: proses, peralatan, aplikasi, contohMereka dapat memiliki komposisi yang berbeda
Larutan hipertonik dapat mengandung zat terlarut seperti garam, atau dapat mengandung campuran zat terlarut seperti garam dan gula, misalnya.
Soluto bisa ionik, netral, atau keduanya
Penjualan berisi ion dengan muatan listrik yang tidak membiarkannya melintasi membran, jadi mereka kecil. Solut lain tidak memiliki ion, tetapi mereka besar dan gemuk dan tidak pas melalui lubang.
Mereka memiliki tekanan osmotik yang tinggi
Seperti disebutkan di atas, solusi hipertonik memiliki tekanan osmotik lebih besar dari darah.
Mereka dapat mendehidrasi sel
Solusi Hipertonik Mengekstrak Air dari Sel Meninggalkannya Sebagai Kismis. Itulah sebabnya tangan dan kaki kita keriput saat kita mandi di pantai.
Untuk apa solusi hipertonik?
Solusi hipertonik memiliki banyak kegunaan dalam kehidupan sehari -hari, dan juga dalam kedokteran. Beberapa kegunaan yang paling umum adalah:
Mereka digunakan untuk menyimpan makanan
- Contoh: Persik dalam sirup tidak membusuk karena sirup memiliki banyak gula terlarut dan merupakan larutan yang sangat hipertonik. Dengan dehidrasi sel, solusi hipertonik tidak memungkinkan jamur dan bakteri dalam makanan, karena mereka mati kehausan. Ini memungkinkan makanan untuk bertahan lebih banyak.
Mereka berfungsi untuk mengurangi peradangan
- Contoh: Ketika seseorang mengalami kecelakaan dan mengenai kepala, ada berkali -kali peradangan di otak. Untuk menyembuhkan pasien, dokter menyuntikkan larutan larutan garam 7,5%. Solusi ini praktis menyedot air, mengurangi peradangan di otak.
Mereka berfungsi untuk menggantikan elektrolit.
- Contoh: Sodium adalah elektrolit yang perlu kita jalani, dan ketika seorang pasien memiliki sedikit natrium dalam darah, larutan salin 7,5% disuntikkan untuk mengisi kembali natrium yang hilang.
Mereka digunakan untuk makanan parenteral
- Contoh: Ketika orang tidak bisa makan melalui mulut atau melalui tabung, mereka memberi makan dalam larutan hipertonik yang mengandung jenis gula yang disebut glukosa.
Perbedaan dengan solusi hipotonik dan isotonik
Sama seperti ada solusi hipertonik, ada juga solusi hipotonik dan isotonik. Perbedaan antara solusi yang terakhir dan hipertonik adalah konsentrasinya. Solusi hipotonik adalah yang kurang terkonsentrasi dari darah, dan isotonik memiliki konsentrasi yang sama dengan darah.
Misalnya, air murni, karena tidak ada terlarut, adalah hipotonik, sedangkan air kelapa memiliki garam dan gula dengan konsentrasi yang hampir sama dengan darah, jadi isotonik.
Selain membedakan dengan konsentrasi, hyper, hypo dan solusi isotonik berbeda dalam cara mereka mempengaruhi sel.
Gambar berikut menunjukkan efek dari berbagai jenis solusi pada sel darah merah (sel -sel kecil yang membuat darah merah).
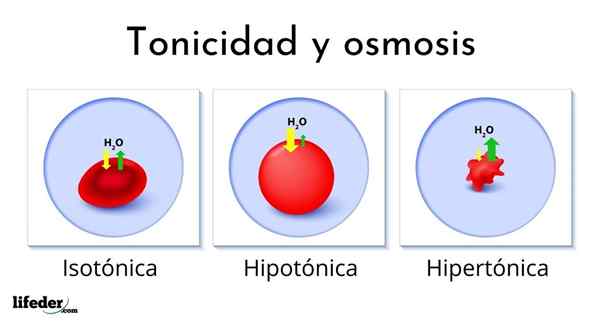
Jika sel darah merah diperkenalkan ke dalam larutan hipertonik, ia mengekstrak air, mendehidrasi dan membuat mereka berkerut sebagai umpan.
Di sisi lain, jika mereka diperkenalkan ke dalam larutan hipotonik, sel darah merah menyerap air dan membengkak, bahkan meledak seperti balon yang mengembang terlalu banyak. Akhirnya, jika mereka diperkenalkan ke dalam larutan isotonik, air di dalam dan di luar sel darah merah akan seimbang sehingga tidak ada yang terjadi.
Contoh solusi hipertonik
Sirup Gula
 Persik dalam sirup
Persik dalam sirup Sirup di mana buah persik dan buah -buahan lainnya diawetkan mengandung konsentrasi gula yang sangat tinggi, jadi ini adalah larutan hipertonik.
Air garam
Air garam adalah larutan air dan garam dengan konsentrasi sangat tinggi antara 3,5% dan 25%, yang dapat menjadi hampir 30 kali lebih terkonsentrasi daripada darah (yaitu, sangat hipertonik).
Cuka
Cuka yang umum adalah larutan hipertonik, karena memiliki konsentrasi antara 3% dan 5% asam asetat. Pengurangan cuka balsamic bahkan lebih terkonsentrasi.
Dapat melayani Anda: dimethylamine ((ch3) 2nh): struktur, sifat, penggunaan, risikoDarah pembuluh darah kita yang sama, setelah banyak berkeringat.
Saat berolahraga dan berkeringat, tubuh menghilangkan air dan garam, tetapi menghilangkan lebih banyak air daripada garam (keringat hipotonik) sehingga darah berkonsentrasi dan menjadi hipertonik.
Air laut
Air laut mengandung banyak garam terlarut, dengan konsentrasi total sekitar 3,5%, yang membuatnya hipertonik. Itulah sebabnya air laut mengerutkan jari kita.
Minuman manis
Minuman Cola dan minuman manis lainnya dapat mengandung hingga 10% gula, serta garam dan zat terlarut lainnya dengan konsentrasi yang lebih besar dari darah.
Larutan dekstrosa 5% dan 0,45% natrium klorida (D5 ½ ns)
Ini adalah contoh dari solusi hipertonik yang digunakan untuk memberi makan orang yang biasanya tidak bisa makan dari mulut.
25% Mannitol
Ini adalah solusi yang sering digunakan untuk mengobati guncangan di kepala. Itu empat kali lebih terkonsentrasi dari darah.
Solusi salin 7,5%
Ini adalah larutan garam yang cukup terkonsentrasi yang juga disuntikkan dengan beberapa pasien dengan penyakit tertentu di vena.
Jus komersial
Semua jus yang dibeli di supermarket dan yang tidak alami, memiliki konsentrasi gula yang sangat tinggi yang membuatnya hipertonik.
Referensi
- Sweeney J. Mengelola Hypernatremia. Perawatan. September 2010; 40 (9): 63.
- Air asin. Wikipedia. 2021. Diambil dari.Wikipedia.org/wiki/air garam.
- Air laut. Wikipedia. 2021. Diambil dari.Wikipedia.Org/wiki/air laut.
- Chavaltamrong B, Pidatcha P, Thavisri U. Elektrolit, gula, kalori, osmolaritas dan pH minuman dan air kelapa. Asia Tenggara J Trop Med Kesehatan Masyarakat. September 1982; 13 (3): 427-431.
- Dekstrosa 5% dan 0.45% injeksi natrium klorida, USP. FDA. 2006. Diambil dari AccessData.FDA.GOV/OBATSATFDA_DOCS/Label/2006/017607S123LBL.Pdf.
- Llorente G, Niño MC. Larutan saline hypertonic versus hypertonic di neuroanesthesia. Majalah Anestesiologi Kolombia. Januari-Maret 2015; 43 (1): 29-39.
- Saints MM, E. Pengobatan asidosis laktat rumen akut dengan larutan natrium klorida atau bikarbonat intravena kacau oleh air intrauminal. Penelitian dalam Sains Hewan. Februari 2020; 128: 24-34.
- Dini-G. E, Abreu-C. JD, López-M. DAN. Osmolalitas minuman konsumsi yang sering. Riset klinikal. Desember 2004; 45 (4).

