Penyebab Tegangan Permukaan, Contoh, Aplikasi dan Eksperimen

- 885
- 73
- Ernesto Mueller
Itu tegangan permukaan Itu adalah sifat fisik yang semua cairan hadir dan ditandai oleh resistensi bahwa permukaannya menentang peningkatan di daerah mereka. Ini sama dengan mengatakan bahwa permukaan ini akan mencari area yang paling tidak mungkin. Fenomena ini menjalin beberapa konsep kimia, seperti kohesi, adhesi dan kekuatan antar molekul.
Ketegangan permukaan bertanggung jawab untuk pembentukan lengkungan permukaan cairan dalam wadah tubular (silinder lulus, kolom, tabung reaksi, dll.). Ini bisa cekung (lembah melengkung) atau cembung (kubah melengkung). Banyak fenomena fisik dapat dijelaskan mengingat perubahan yang diderita oleh tegangan permukaan cairan.
 Bentuk bola yang diadopsi oleh tetesan air pada daun sebagian karena ketegangan permukaannya. Sumber: Foto yang Diambil oleh Pengguna Flickr Tanakawho [CC BY (https: // CreationCommons.Org/lisensi/oleh/2.0)]
Bentuk bola yang diadopsi oleh tetesan air pada daun sebagian karena ketegangan permukaannya. Sumber: Foto yang Diambil oleh Pengguna Flickr Tanakawho [CC BY (https: // CreationCommons.Org/lisensi/oleh/2.0)] Salah satu fenomena ini adalah tren yang dimiliki oleh molekul cairan dalam bentuk tetes, ketika mereka bersandar pada permukaan yang mengusirnya. Misalnya, air tetesan yang kita lihat di atas daun tidak bisa membasahinya karena bukitnya, permukaan hidrofobik.
Namun, ada saatnya gravitasi memberikan perannya dan penurunannya tumpah seperti kolom air. Fenomena serupa terjadi pada tetes bulat merkuri saat termometer tumpah.
Di sisi lain, tegangan air permukaan adalah yang paling penting dari semuanya, karena berkontribusi dan mengatur status tubuh mikroskopis dalam media berair, seperti sel dan membran lipid mereka. Selain itu, ketegangan ini bertanggung jawab atas air untuk menguap perlahan, dan beberapa tubuh terpadat yang dapat mengambang di permukaannya.
[TOC]
Penyebab Ketegangan Permukaan
Penjelasan tentang fenomena tegangan permukaan adalah pada tingkat molekuler. Molekul cairan berinteraksi satu sama lain, sehingga mereka kohesif dalam gerakan mereka yang tidak menentu. Molekul berinteraksi dengan tetangganya di sebelah dan yang ada di atas atau di bawahnya.
Namun, ini tidak terjadi sama dengan molekul permukaan cairan, yang bersentuhan dengan udara (atau gas lainnya), atau dengan padatan. Molekul permukaan tidak dapat kohesif dengan lingkungan eksternal.
Akibatnya, mereka tidak mengalami kekuatan apa pun yang menarik mereka; Hanya turun, dari tetangganya di media cair. Untuk menangkal ketidakseimbangan ini, molekul permukaan "diperas", karena hanya dengan begitu mereka berhasil mengatasi kekuatan yang mendorong mereka ke bawah.
Dapat melayani Anda: natrium silikat (na2sio3): struktur, sifat, penggunaan, risikoPermukaan kemudian dibuat di mana molekul berada dalam pembuangan yang lebih tegang. Jika suatu partikel ingin menembus cairan, ia harus terlebih dahulu melintasi penghalang molekul ini sebanding dengan tegangan permukaan cairan tersebut. Hal yang sama berlaku untuk partikel yang ingin melarikan diri ke lingkungan eksternal dari kedalaman cairan.
Oleh karena itu, permukaannya berperilaku seolah -olah itu adalah film elastis yang menunjukkan resistensi untuk berubah bentuk.
Unit
Tegangan permukaan biasanya diwakili dengan simbol γ, dan diekspresikan dalam unit N/M, kekuatan berdasarkan panjang. Namun, sebagian besar waktu unit Anda adalah Dyn/cm. Satu bisa menjadi yang lain melalui faktor konversi berikutnya:
1 dyn/cm = 0,001 n/m
Ketegangan air permukaan
Air adalah barat dan paling mengejutkan dari semua cairan. Ketegangan permukaannya, serta beberapa sifatnya, memiliki nilai tinggi yang luar biasa: 72 dyn/cm pada suhu kamar. Nilai ini dapat meningkat menjadi 75,64 dyn/cm, pada suhu 0 ºC; atau berkurang menjadi 58,85 ºC, pada suhu 100 ºC.
Pengamatan ini masuk akal jika dianggap bahwa penghalang molekul tegang bahkan lebih pada suhu yang dekat dengan titik beku, atau "melonggarkan" sedikit lebih di sekitar titik didih.
Air memiliki ketegangan permukaan yang hebat mengikuti jembatan hidrogennya. Jika ini terkenal di dalam cairan, mereka bahkan lebih di permukaan. Molekul air sangat terkait dengan membentuk interaksi dipol-dipolo tipe H2Oh oh.
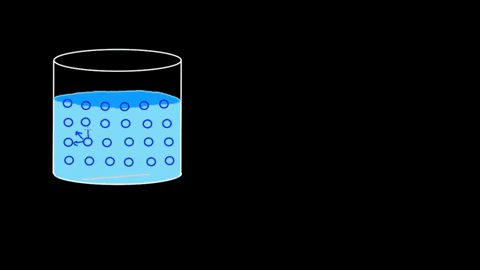 Molekul air saling menarik; Mereka dihubungkan oleh jembatan hidrogen
Molekul air saling menarik; Mereka dihubungkan oleh jembatan hidrogen Efisiensi interaksinya sedemikian rupa sehingga penghalang molekul berair bahkan dapat menopang beberapa tubuh sebelum mereka tenggelam. Di bagian aplikasi dan percobaan poin ini akan dilanjutkan.
Contoh lainnya
Semua cairan memiliki ketegangan permukaan, baik pada tingkat yang lebih rendah atau lebih besar dari air, atau jika mereka adalah zat atau solusi murni. Seberapa kuat dan tegang hambatan molekuler dari superfisial mereka, itu akan tergantung langsung pada interaksi antarmolekulnya, selain faktor struktural dan energi.
Gas kental
Misalnya, molekul gase dalam keadaan cair hanya berinteraksi satu sama lain melalui kekuatan dispersif di London. Ini setuju dengan fakta bahwa ketegangan superfisial mereka memiliki nilai rendah:
-Helium cair, 0,37 dyn/cm a -273 ºC
Ini dapat melayani Anda: Ammonium chloride (NH4CL)-Nitrogen cair, 8,85 dyn/cm a -196 ºC
-Oksigen cair, 13.2 dyn/cm a -182 ºC
Tegangan permukaan oksigen cair lebih besar dari helium karena molekulnya memiliki massa yang lebih besar.
Cairan apolar
Dari cairan apolar dan organik, mereka diharapkan memiliki ketegangan permukaan yang lebih tinggi daripada gas kental ini. Di antara beberapa dari mereka, kami memiliki yang berikut:
-Diet, 17 dyn/cm pada 20 ºC
-N-Hexano, 18.40 dyn/cm pada 20 ºC
-N-Octane, 21,80 Dyn/cm pada 20 ºC
-Toluene, 27.73 Dyn/cm pada 25 ºC
Tren serupa diamati untuk cairan ini: tegangan permukaan meningkat karena massa molekulnya meningkat. Namun N-Octane harus, menurut ini, memiliki tegangan permukaan terbesar dan bukan toluena. Di sini struktur dan geometri molekuler ikut bermain.
Toluena, rencana dan molekul anilar memiliki interaksi yang lebih efektif daripada N-oktan. Oleh karena itu, permukaan toluena adalah "tegang" dari permukaan N-oktan.
Cairan kutub
Menjadi dipol-dipol yang lebih kuat. Tapi tidak selalu demikian. Di antara beberapa contoh yang kami miliki:
-Asam asetat, 27,60 dyn/cm pada 20 ºC
-Aseton, 23,70 dyn/cm pada 20 ºC
-Darah, 55,89 dyn/cm pada 22 ° C
-Etanol, 22,27 Dyn/cm pada 20 ºC
-Gliserol, 63 dyn/cm pada 20 ºC
-Cair Sodium Chloride, 163 Dyn/Cm pada 650 ºC
-Solusi NaCl 6 M, 82,55 Dyn/cm pada 20 ºC
Sodium cair klorida diharapkan memiliki tegangan permukaan yang sangat besar: ini adalah cairan kental dan ionik.
Di sisi lain, merkuri adalah salah satu cairan dengan tegangan permukaan tertinggi: 487 dyn/cm. Di dalamnya, permukaannya terdiri dari atom merkuri yang sangat kohesif, jauh lebih banyak daripada molekul air.
Aplikasi
 Beberapa serangga menggunakan tegangan permukaan air untuk berjalan di atasnya. Sumber: Pixabay.
Beberapa serangga menggunakan tegangan permukaan air untuk berjalan di atasnya. Sumber: Pixabay. Ketegangan superfisial saja tidak memiliki aplikasi. Namun, ini tidak berarti bahwa itu tidak terlibat dalam beberapa fenomena harian, bahwa jika tidak ada, mereka tidak akan terjadi.
Misalnya, nyamuk dan serangga lainnya dapat berjalan melalui air. Ini karena kaki hidrofobik mereka mengusir air, pada saat yang sama bahwa massa kecil mereka memungkinkan mereka.

Ketegangan superfisial juga memenuhi peran dalam pembasahan cairan. Semakin besar ketegangannya yang dangkal, semakin sedikit kecenderungannya untuk bocor melalui pori -pori atau anak ayam bahan. Selain itu, mereka adalah sedikit cairan yang berguna untuk membersihkan permukaan.
Dapat melayani Anda: reaksi netralisasiDeterjen
Di sinilah deterjen bertindak, mengurangi tegangan permukaan air, dan membantunya menutupi permukaan yang lebih besar; Sambil meningkatkan tindakan degreaser Anda. Dengan mengurangi ketegangannya yang dangkal, ia mengakomodasi molekul udara, dengan mana gelembung terbentuk.
Emulsi
Di sisi lain, ketegangan yang lebih tinggi terkait dengan stabilisasi emulsi, sangat penting dalam perumusan rentang produk yang berbeda.
Eksperimen sederhana
 Klip logam mengambang karena ketegangan air permukaan. Sumber: Alvesgaspar [CC BY-S (https: // CreativeCommons.Org/lisensi/by-sa/3.0)]
Klip logam mengambang karena ketegangan air permukaan. Sumber: Alvesgaspar [CC BY-S (https: // CreativeCommons.Org/lisensi/by-sa/3.0)] Akhirnya, beberapa percobaan yang dapat dilakukan di ruang domestik apa pun akan dikutip.
Eksperimen Klip
Dalam gelas dengan air dingin, klip logam ditempatkan di permukaannya. Seperti yang terlihat pada gambar atas, klip akan tetap mengapung berkat ketegangan permukaan air. Tetapi jika sedikit lava loza ditambahkan ke kaca, tegangan permukaan akan berkurang secara dramatis dan klipnya akan tiba -tiba akan tenggelam.

Perahu Kertas
Jika kami memiliki kapal kertas atau palet kayu, dan jika Anda mencuci sedikit atau deterjen, itu ditambahkan di kepala swab, maka fenomena yang menarik akan terjadi: akan ada penolakan yang akan menyebarkannya ke arah tepi dari kaca. Kapal kertas dan palet kayu akan menjauh dari swab dioleskan dengan deterjen.

Eksperimen lain yang serupa dan lebih grafis adalah mengulangi operasi yang sama, tetapi dalam seember air yang disemprot dengan lada hitam. Partikel lada hitam akan bergerak menjauh dan permukaan akan berubah dari lada menjadi kristal, dengan tepi di tepi.
Referensi
- Whitten, Davis, Peck & Stanley. (2008). Kimia. (Edisi ke -8.). Pembelajaran Cengage.
- Wikipedia. (2020). Tegangan permukaan. Diperoleh dari: di.Wikipedia.org
- USGS. (S.F.). Tegangan permukaan dan air. Diperoleh dari: USGS.Pemerintah
- Jones, Andrew Zimmerman. (12 Februari 2020). Ketegangan Permukaan - Definisi dan Eksperimen. Pulih dari: thinkco.com
- Susanna Lauren. (15 November 2017). Mengapa Ketegangan Permukaan Penting? Biolin Scientific. Dipulihkan dari: blog.Biolinscientific.com
- Ilmu Pengasuhan Rookie. (7 November 2019). Apa itu tegangan permukaan | Eksperimen Sains Keren. Pulih dari: rookieparenting.com
- Jessica Mock. (2020). Eksperimen tegangan permukaan. Belajar. Pulih dari: belajar.com
- Anak itu harus melihat ini. (2020). Tujuh Eksperimen Ketegangan Permukaan - Gadis Fisika. Pulih dari: thekidshouldseethis.com

