Tioles
- 1616
- 113
- Ernesto Mueller
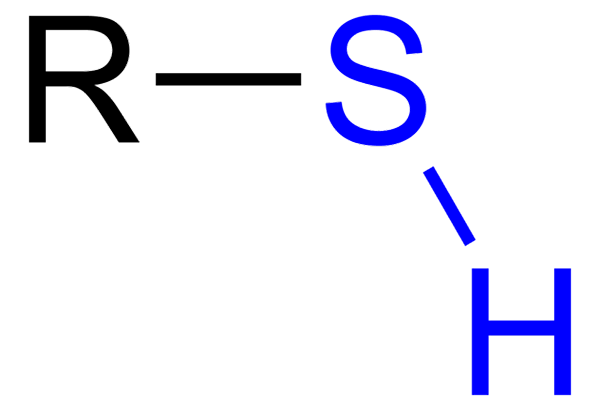
Itu Tioles Mereka adalah senyawa organik yang memiliki kelompok SH, yang disebut gugus tiol atau sulfihidrilo. Formulanya umum adalah RSH, mampu mewakili R ke sewa, aril atau kelompok kimia lainnya. Karakteristik khas thioles adalah bau bau yang kuat.
Beberapa thiol digunakan untuk memberikan bau gas yang mudah terbakar, untuk mendeteksi kebocoran gas -gas ini, yang memberikan karakteristik mereka dapat sangat bahaya. Tioles mirip dengan alkohol, karena mereka memiliki kelompok OH, sedangkan thioles a sh.
 Tiol dengan kelompok sulfhidrillo biru
Tiol dengan kelompok sulfhidrillo biru Namun, mereka pada gilirannya memiliki beberapa perbedaan: kelompok OH lebih polar daripada kelompok SH, dan belerang adalah atom yang lebih kecil dari oksigen dan lebih sedikit elektronegatif.
Ini menentukan bahwa molekul tiol tidak membentuk ikatan hidrogen atau air atau di antaranya. Oleh karena itu, kelarutan tiol dalam air rendah dan titik didihnya lebih rendah dari alkohol dengan rantai karbon yang sama.
Tiole sangat berguna dan sering dalam sistem biokimia, karena beberapa sesuai dengan biomolekul, seperti koenzim. Ikatan S-H-nya lebih asam daripada O-H, lebih mudah dipatahkan, dan juga lebih mudah untuk mengganti atau mengganti fragmen molekul lainnya dalam banyak sintesis organik sulfur.
[TOC]
Properti Tioles
 Aroma bau kaki bukit terutama terdiri dari tiol
Aroma bau kaki bukit terutama terdiri dari tiol Generalitas
Kelompok alkohol OH dan kelompok SH dari tiols memiliki serangkaian sifat fisik dan kimia untuk memiliki oksigen dan sulfur dengan kelompok kimia yang sama dari tabel periodik (melalui kelompok).
Loa Tioéters, Uniocetals dan Thioésters, yang analog dengan senyawa kimia yang dibentuk oleh alkohol, seperti eter, asetal dan ester. Namun, tautan S-H dan O-H menyajikan beberapa perbedaan yang akan tercermin dalam sifat tiol dan alkohol.
Bau
Karakteristik tiole berat molekul rendah adalah bau yang tidak menyenangkan, mirip dengan bawang putih dan bawang. Bau ini sangat besar sehingga bau manusia memiliki ambang satu bagian thiol untuk sepuluh miliar bagian udara.
Etanotiol ditambahkan ke gas alam sebagai tindakan pengaman, untuk mendeteksi apapun yang mudah terbakar tetapi toilet melarikan diri. Aroma thiol berkurang dengan meningkatkan jumlah karbon rantai mereka, karena volatilitas dan proporsi tiol sulfur berkurang.
Dapat melayani Anda: amonium fosfat: struktur, sifat, memperoleh, penggunaanTitik didih dan kelarutan
Tautan S-H dari Tioles memiliki momen dipol kurang dari tautan O-H dari alkohol. Selain itu, atom belerang lebih kecil dan lebih kecil elektronegativitas daripada atom oksigen.
Ini menentukan bahwa molekul tiol tidak dapat membentuk ikatan hidrogen dengan air atau di antaranya, menyebabkan perbedaan antara sifat fisik tiol dan alkohol. Misalnya: metanotiol (cho3Sh) memiliki titik mendidih 6 ºC, sedangkan metanol (cho3Oh) mendidih pada 65 ° C.
Oleh karena itu, pada suhu kamar (25 ºC) metanol adalah cairan dan metanotiol adalah gas.
Singkatnya: Thioles memiliki titik didih yang lebih rendah daripada alkohol yang disajikan. Untuk alasan yang sama, kelarutan tiol di dalam air dan pelarut kutub lainnya sangat rendah. Sementara itu, alkohol dengan berat molekul rendah sangat larut dalam air.
Reaktivitas
Tautan S-H lebih lemah dari ikatan O-H, jadi tautan S-H lebih mudah dipisahkan, membuat tiol asam kuat daripada alkohol. Kebanyakan alkohol memiliki PKA antara 16 dan 18, sementara thiol memiliki PKA sekitar 11.
Ini memungkinkan thioles-): Agen nukleofilik yang sangat kuat.
Kelompok SH dapat teroksidasi untuk membentuk tautan disulfida (-s-s-) yang ada dalam oksidasi glutathionik: tiol yang ada dalam sel dan memiliki fungsi antioksidan.
Bromo atau halogen lainnya, serta oksigen, dapat bertindak pada tiol untuk membentuk jembatan disulfur:
2 RSH +BR → R-S-S-R '+2 HBR
Senyawa RSSR dikenal sebagai sulfida dan alkiiles organik, R2S.
Di sisi lain, agen pengoksidasi yang kuat, seperti natrium hipoklorit dan hidrogen peroksida, dapat bertindak pada tiola untuk menyebabkan asam sulfonat:
Rsh +h2SALAH SATU2 → RSO3H +3 h2SALAH SATU
Tata nama
Nomenklatur IUPAC untuk Thioles sangat mirip dengan alkohol: nama alkano dari mana akhiran 'tiol' ditambahkan kepadanya.
Jadi, misalnya, thistan yang diturunkan stano disebut 1-butanotiol, ch3Ch2Ch2Ch2Sh, menunjukkan dengan angka posisi kelompok SH di karbon rantai.
Dapat melayani Anda: kation: pelatihan, perbedaan dengan anion dan contohDengan cara yang sama ada nomenklatur lain, sekali lagi, mirip dengan alkohol: kata 'alkohol' digantikan oleh 'Mercaptan' dalam nama alkohol. Misalnya, Cho3Sh, analog dengan metil alkohol, ch3Oh, disebut metil atau merkaptan mercaptan.
Contoh lain adalah Cho3Ch2Ch (sh) ch3, disebut 2-butanotiol, pedagang secbutilik, atau merchandise secbutil. Yaitu, penekanan ditempatkan pada identitas R dalam formula RSH. Oleh karena itu, norma nomenklatur lain untuk alkohol juga dipenuhi untuk tiol.
Dan akhirnya, ketika kelompok SH hadir dalam struktur yang lebih besar atau di mana kelompok yang paling penting mendominasi, sulfihidrilo atau awalan Mercapto digunakan.
Misalnya, senyawa ch3Ch2Ch (sh) Coch3 Itu disebut 3-mercapto-2-penon. Perhatikan bahwa SH memiliki prioritas yang lebih sedikit daripada kelompok teroksigenasi (kecuali untuk eter), sehingga angka kecil sesuai dengan itu.
Perpaduan
Metode sintesis tiol terdiri dari reaksi tiota dengan alkil halida, yang menghasilkan garam menengah isotiouron. Ini dihidrolisis oleh natrium hidroksida untuk mendapatkan tiol dan urea.
Ch3SH disiapkan secara industri dengan reaksi hidrogen sulfida dengan metanol, dengan adanya katalis asam:
Ch3Oh +h2S → CH3Sh +h2SALAH SATU
Dalam metode produksi lain, alkil halida bereaksi dengan natrium hidrosulfuro:
RX +NASH → RSH +NAX
Aplikasi
Penetapan enzim terkait dengan nanopartikel
Tioles digunakan sebagai jembatan untuk bergabung dengan kompleks nanopartikula-enzim ke elektroda emas. Sebagai contoh, thioles digunakan untuk fiksasi kompleks nanopartikel-uricasa, enzim yang mengintervensi dalam konversi asam urat menjadi allantoine.
Tiol -Tidak ada reaksi
Ini adalah reaksi organik antara TIOL dan alkena, menyebut reaksi "klik"; Bahwa di antara karakteristik lain, ini adalah reaksi kinerja tinggi, ruang lingkup luas, yang menciptakan produk yang dapat dihilangkan dengan produk dengan metode non -kromatografi, dan itu juga mudah dilakukan.
Reaksi thiol -tidak memiliki aplikasi dalam sintesis tioazúcar: gula hadir dalam salicinol, inhibitor α -glikosidase. Salicinol telah diisolasi dari tanaman yang digunakan di Sri Lanka dan India dalam pengobatan diabetes.
Selain itu, reaksi tiol -tidak digunakan dalam kimia karbohidrat, polimerisasi, kimia permukaan, kimia sintesis dan kimia peptida.
Dapat melayani Anda: titik beku: cara menghitungnya dan contohBau
 Gas dapur adalah toilet, tetapi berkat komposisinya dari thioles berat molekulnya ia memiliki bau yang khas
Gas dapur adalah toilet, tetapi berkat komposisinya dari thioles berat molekulnya ia memiliki bau yang khas Tiola alifatik dengan berat molekul rendah dimasukkan ke dalam gas alam sehingga bau kuatnya berfungsi sebagai peringatan di hadapan pelarian atau kebocoran gas.
Obat
Penicilamine (c5HsebelasTIDAK2S) Ini adalah obat yang digunakan dalam pengobatan penyakit Wilson dan rheumatoid arthritis.
Dan captopril (c9HlimabelasTIDAK3S), di sisi lain, digunakan dalam pengobatan hipertensi arteri dan penyakit jantung kongestif.
Keduanya adalah contoh thiol dengan aplikasi obat.
Biologis
Kelompok tiol ada, di antara senyawa lain dengan fungsi biologis, dalam sistein, koenzim A dan glutathione.
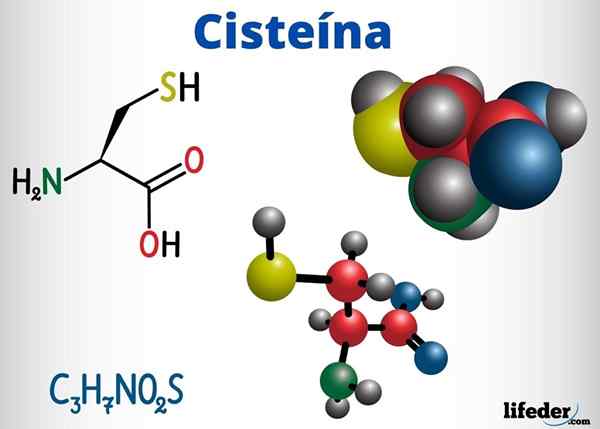
Sistein adalah asam amino yang mampu membentuk jembatan disulfur dalam rantai proteinnya, oleh karena itu, bertanggung jawab untuk struktur tersier protein. Ini juga dapat membentuk jembatan disulfur antara rantai protein yang berbeda, menyebabkan struktur kuat protein.
Cysteine terletak di pusat aktif dari berbagai enzim dan juga memiliki aksi antioksidan.
Glutathion adalah tindakan intraseluler antioksidan yang sangat penting, memberikan perlindungan pada sel dan makromolekul yang menyusunnya.
Koenzim A, di sisi lain, adalah tiol yang mengintervensi sintesis dan oksidasi asam lemak. Selain itu, koenzim di bawah bentuk asetilkoenzim A, mengintervensi pada awal siklus asam sitrat atau siklus Krebs.
Contoh
Akhirnya, beberapa nama thiol akan terdaftar disertai dengan rumus molekuler mereka:
-Asam Tioacetic (C2H4ANDA)
-Coenzyme A (cdua puluh satuH36N7SALAH SATU16P3S)
-Mengurangi glutation (c10H17N3SALAH SATU6S)
-Sistein (c3H7TIDAK2S)
-Mercaptanol (c2H6ANDA)
-Metanotiol (ch3SH)
-1-propanotiol (c3H7SH)
-Butanotiol (c4H 9SH)
-Tiofenol atau tiomerosa (c6H6S)
-Pomelo Mercaptano (c10H18S)
-Hexadecanotiol (c6H3. 4S)
-Penicillamine (c6HsebelasTIDAK2S)
-Captopril (c9HlimabelasTIDAK3S)
-Etanotiol (c2H6S)
-2-propenetiol (c3H6S)
-Α-lipoic atau lipoamide (c8H14SALAH SATU2S2). Itu adalah disulfida siklik.
Referensi
- Graham Solomons t.W., Craig b. Fryhle. (2011). Kimia organik. (10th Edisi.). Wiley Plus.
- Carey f. (2008). Kimia organik. (Edisi Keenam). MC Graw Hill.
- Morrison dan Boyd. (1987). Kimia organik. (Edisi Kelima). Addison-Wesley Iberoamericana.
- Wikipedia. (2020). Tiol. Diperoleh dari: di.Wikipedia.org
- Kata. Dietmar Kennepohl et al. (13 September 2020). Tiol dan sulfida. Libretteks Kimia. Pulih dari: chem.Librettexts.org
- Para editor Eeritlopaedia Britannica. (2020). Tiol. Dipulihkan dari: Britannica.com
- Nolan MD dan Scanlan EM (2020) Aplikasi Kimia Tiol-Ene untuk Ilmu Peptida. Depan. Chem. 8: 583272. Doi: 10.3389/fchem.2020.583272
- Kata. Carl c. Wamser. (1999). Bab 9: Alkohol dan Tiol. Diperoleh dari: web.PDX.Edu

