Sulfur oksida
- 661
- 6
- Miss Marion Graham
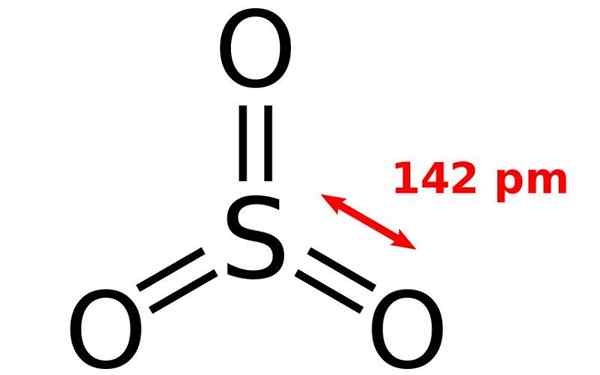
 Struktur kimia molekul sulfur oksida. Sumber: Joel Holdsworth, Wikimedia Commons
Struktur kimia molekul sulfur oksida. Sumber: Joel Holdsworth, Wikimedia Commons Apa itu sulfur oksida?
Dia sulfur oksida (Vi), juga dikenal sebagai sulfur atau sulfat anhidrida trioksida, adalah senyawa kimia dari formula S3, Itu, dalam kondisi normal, itu adalah padatan yang tidak berwarna dan berserat, dan pada 25 ° C dan 1 ATM adalah zat pencemar yang kuat, bertanggung jawab atas hujan asam.
Sulfur trioksida diproduksi oleh oksidasi sulfur oksid.
Namun, sampai sekarang, satu -satunya persiapan trioksida sulfur murni dari gas yang mengandung3 Diencerkan, ini telah menjadi proses pada skala pabrik percontohan yang menyiratkan kondensasi cryoscopic.
Prosedur yang biasa menyiratkan, sebaliknya, distilasi minyak. Panas yang dibutuhkan untuk distilasi minyak disuplai lebih nyaman dengan gas kontak panas dari tanaman asam sulfat terkait.
Ini dapat disiapkan di laboratorium dengan memanaskan asam sulfat merokok dan mengumpulkan sublimasi dalam penerima yang didinginkan. Jika uapnya terkondensasi di atas 27 ° C, bentuk gamma diperoleh sebagai cairan.
Jika uap dikondensasi di bawah 27 ° C dan di hadapan garis kelembaban, campuran dari tiga bentuk diperoleh. 3 bentuk dapat dipisahkan dengan distilasi fraksional.
Pembakaran bahan bakar fosil adalah penyebab penampilannya di atmosfer, ini menjadi penyebab antropogenik utama.
Sifat fisik dan kimia sulfur oksida
- Sulfur trioksida berbentuk seperti jarum putih yang menjadi asap di udara. Anda sering menemukan inhibitor untuk menghindari polimerisasi.
Dapat melayani Anda: renio: penemuan, sifat, struktur, penggunaan- Berat molekulnya adalah 80.066 g/mol, kepadatannya adalah 1,92 g/cm³ g/ml dan titik -titik perebusan masing -masing adalah 16,8 ° C dan 44,7 ° C.
- Senyawa ini dikombinasikan dengan air dengan gaya ledakan, membentuk asam sulfat karena keasamannya. Zat organik karboniza sulfur trioksida.
- Sulfur trioksida menyerap kelembaban dengan cepat, memancarkan asap putih padat. Larutan Trioksida Asam Sulfat disebut Asam Merokok Sulfat atau Minyak.
- Reaksi sulfur trioksida dan oksigen difluorida sangat kuat dan ledakan diproduksi jika reaksi dilakukan tanpa adanya pelarut.
- Reaksi kelebihan sulfur trioksida dengan tetrafluoroethylene menyebabkan dekomposisi peledak karbonil fluorida dan sulfur dioksida.
- Reaksi asam perklorat anhidrat dengan sulfur trioksida adalah kekerasan dan disertai dengan evolusi panas yang cukup besar. Trioksida sulfur cair bereaksi keras dengan nitril klorida, bahkan 75 ° C.
- Reaksi sulfur trioksida dan timbal oksida menyebabkan luminesensi putih. Kombinasi yodium, piridin, sulfur dan formamida trioksida mengembangkan gas pada tekanan setelah beberapa bulan.
Ini disebabkan oleh lambat pembentukan asam sulfat, air eksternal atau dehidrasi formamida hidrogen sianida.
Risiko
Sulfur trioksida adalah senyawa yang stabil, tidak sesuai dengan bahan organik, logam bubuk halus, pangkalan, air, sianida, dan berbagai macam bahan kimia lainnya.
Zat ini adalah oksidan yang kuat dan bereaksi keras dengan bahan dan penyelenggara yang mudah terbakar dan senyawa organik yang menyebabkan bahaya kebakaran dan ledakan.
Dapat melayani Anda: natrium oksalat (na2c2o4): struktur, sifat, penggunaan, risikoBereaksi keras dengan air basah dan udara untuk menghasilkan asam sulfat. Larutan dalam air adalah asam yang kuat, bereaksi keras dengan basa dan logam korosif, membentuk gas yang mudah terbakar / meledak.
Senyawa ini bersifat korosif untuk logam dan jaringan. Menyebabkan luka bakar di mata dan kulit. Konsumsi menyebabkan luka bakar yang parah di mulut, kerongkongan dan lambung. Uapnya sangat beracun dengan inhalasi.
Dalam hal kontak mata, Anda harus memverifikasi apakah lensa kontak digunakan dan segera menghapusnya. Mata harus dibilas dengan air mengalir setidaknya selama 15 menit, menjaga kelopak mata tetap terbuka. Air dingin dapat digunakan, tanpa mengoleskan salep mata.
Jika bahan kimianya bersentuhan dengan pakaian, simpan secepat mungkin, melindungi tangan dan tubuhnya sendiri. Tempatkan korban di bawah shower pengaman.
Jika bahan kimianya menumpuk di kulit korban yang terbuka, seperti tangan, kulit yang terkontaminasi dengan air mengalir dan sabun non -abasif dicuci dengan lembut dan hati -hati. Air dingin dapat digunakan. Jika iritasi tetap ada, cari perhatian medis. Cuci pakaian yang terkontaminasi sebelum menggunakannya lagi.
Dalam kasus inhalasi, korban harus diizinkan untuk berdiri di daerah berventilasi baik. Jika inhalasinya serius, korban harus dievakuasi ke area yang aman sesegera mungkin. Pakaian ketat longgar, seperti leher kemeja, ikat pinggang atau dasi.
Jika korban sulit bernafas, oksigen harus diberikan. Jika korban tidak bernapas, resusitasi mulut dibuat. Selalu mempertimbangkan bahwa itu bisa berbahaya bagi orang yang memberikan bantuan memberikan resusitasi mulut ke mulut ketika bahan inhalasi beracun, menular atau korosif.
Itu dapat melayani Anda: asam hipofisis (h3po2): sifat, penggunaan dan reagenDalam semua kasus, perhatian medis segera harus dicari.
Di sisi lain, polusi udara akibat sulfur oksida adalah masalah lingkungan yang penting, dengan jutaan ton sulfur dioksida dan trioksida yang dipancarkan ke atmosfer setiap tahun. Senyawa ini berbahaya bagi kehidupan tanaman dan hewan, serta untuk banyak bahan konstruksi.
Masalah besar lainnya yang perlu dipertimbangkan adalah hujan asam. Kedua sulfur oksida larut dalam air atmosfer tetes untuk membentuk larutan asam, yang bisa sangat berbahaya ketika jatuh dalam bentuk hujan.
Hujan asam dapat merusak hutan dan menyebabkan ikan mati di banyak danau. Ini juga korosif untuk logam, batu kapur dan bahan lainnya. Solusi yang mungkin untuk masalah ini mahal karena kesulitan menghilangkan belerang batubara dan minyak sebelum terbakar.
Aplikasi
- Sulfur trioksida adalah reagen penting dalam reaksi sulfonasi. Proses ini menyediakan deterjen, pewarna dan produk farmasi. Itu dihasilkan in situ dari asam sulfat atau digunakan sebagai larutan asam sulfat merokok.
- Sifat desinfektannya bertanggung jawab atas berabad -abad untuk digunakan untuk mendisinfeksi kubus anggur, membakar sulfur di dalamnya.
Referensi
- Sulfur trioksida. Pulih dari EBI.Ac.Inggris
- Lembar data keselamatan sulfur trioksida. Pulih dari sciencelab.com

