Boron oksida (B2O3) Apa itu, struktur, sifat, penggunaan
- 864
- 154
- Mr. Darrell Streich
Dia Boron oksida o Boric anhydride adalah senyawa anorganik yang formula kimianya B adalah B2SALAH SATU3. Menjadi elemen boron dan oksigen dari blok P dari tabel periodik, dan bahkan lebih banyak kepala kelompok masing -masing, perbedaan elektronegativitas di antara mereka tidak terlalu tinggi; Oleh karena itu, diharapkan bahwa B2SALAH SATU3 bersifat kovalen.
B2SALAH SATU3 Disiapkan dengan melarutkan boraks dalam asam sulfat pekat di dalam oven merger dan pada suhu 750ºC; Asam Borat Dehidrasi Termal, B (OH)3, pada suhu sekitar 300 ° C; atau juga dapat dibentuk sebagai produk dari reaksi diborano (b2H6) Dengan oksigen.
Boro oksida dapat memiliki penampilan kaca semi -transparan, atau kristal; Yang terakhir dengan menggiling dapat diperoleh dalam bentuk debu.
Meskipun tampaknya tidak terlihat pertama, B dipertimbangkan2SALAH SATU3 sebagai salah satu oksida anorganik paling kompleks; Tidak hanya dari sudut pandang struktural, tetapi juga karena sifat variabel yang diperoleh kaca dan keramik yang ditambahkan ke matriks mereka.
Struktur boro oksida
Persatuan bo3
B2SALAH SATU3 Ini adalah kovalen padat, jadi secara teori mereka tidak ada dalam struktur Ion B -nya3+ juga bukan2-, Tapi tautan B-O. Boron, menurut Teori Tautan Valencia (TEV), hanya dapat membentuk tiga tautan kovalen; Dalam hal ini, tiga tautan B-O. Sebagai konsekuensi dari ini, geometri yang diharapkan harus trigonal, bo3.
Molekul BO3 Ini adalah elektron yang buruk, terutama atom oksigen; Namun, beberapa dari mereka dapat berinteraksi satu sama lain untuk memasok kekurangan tersebut. Dengan demikian, segitiga bo3 Mereka bergabung dengan berbagi jembatan oksigen, dan didistribusikan di luar angkasa sebagai jaringan baris segitiga dengan pesawat mereka berorientasi dengan cara yang berbeda.
Dapat melayani Anda: solusi tak jenuhStruktur kristal
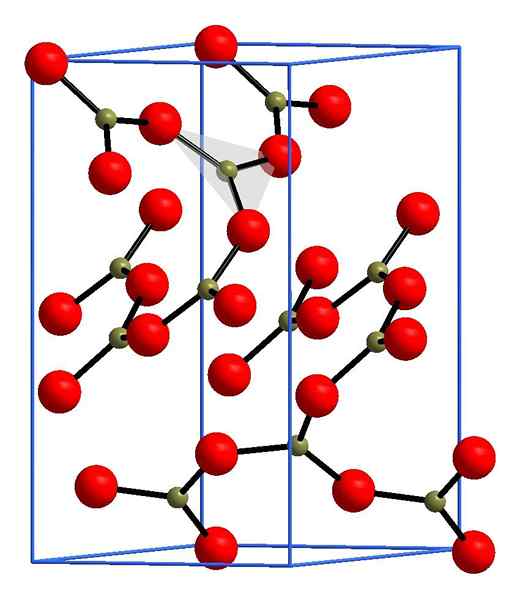
 Struktur boro oksida. Andif1, wikimedia commons.
Struktur boro oksida. Andif1, wikimedia commons. Pada gambar atas contoh baris ini dengan unit segitiga bo3. Jika diamati dengan hati -hati, tidak semua wajah dari rencana menunjuk ke pembaca, tetapi ke sisi lain. Orientasi wajah -wajah ini dapat bertanggung jawab atas bagaimana B didefinisikan2SALAH SATU3 pada suhu dan tekanan tertentu.
Ketika jaringan ini memiliki pola struktural rentang panjang, itu adalah padatan kristal, yang dapat dibangun dari sel satuannya. Di sinilah dikatakan bahwa B2SALAH SATU3 Ini memiliki dua polimorf kristal: α dan β.
Α-B2SALAH SATU3 Ini diproduksi dalam tekanan ambient (1 atm), dan dikatakan bahwa itu sangat tidak stabil; Faktanya, ini adalah salah satu alasan mengapa boron oksida mungkin merupakan senyawa kristalisasi yang sulit.
Polimorf lainnya, β-B2SALAH SATU3, Tekanan tinggi diperoleh dalam kisaran IPK; Oleh karena itu, kepadatannya harus lebih besar dari α-B2SALAH SATU3.
Struktur vitreous
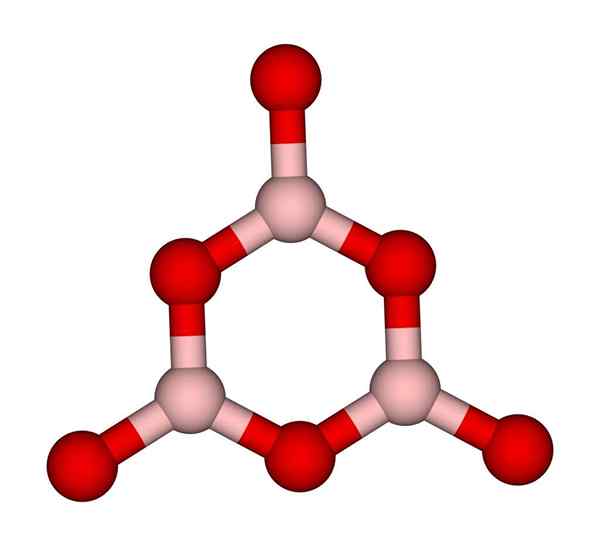 Cincin boroksol. Ccoil (bicara). Wikimedia Commons.
Cincin boroksol. Ccoil (bicara). Wikimedia Commons. Jaringan Bo3 secara alami cenderung mengadopsi struktur amorf; Inilah, yang tidak memiliki pola yang menggambarkan molekul atau ion dalam padatan. Dengan mensintesis b2SALAH SATU3 Bentuk dominannya adalah amorf dan bukan kristal; Dengan kata -kata yang benar: itu adalah solid yang lebih vitreus dari kristal.
Kemudian dikatakan bahwa b2SALAH SATU3 Itu vitreous atau amorf saat anak laki -laki Anda dari Bo3 Mereka berantakan. Tidak hanya ini, tetapi juga mengubah cara mereka bergabung. Alih -alih memesan dalam geometri trigonal, cincin boroksol (gambar superior) berakhir untuk membuat peneliti (gambar superior).
Dapat melayani Anda: 20 contoh energi kimiaPerhatikan perbedaan yang jelas antara unit segitiga dan heksagonal. Karakterisasi segitiga b2SALAH SATU3 kristal, dan heksagonal ke b2SALAH SATU3 seperti kaca. Cara lain untuk merujuk pada fase amorf ini adalah boron glass, atau dengan rumus: g-b2SALAH SATU3 ('G' berasal dari kata kaca, dalam bahasa Inggris).
Dengan demikian, jaringan G-B2SALAH SATU3 Mereka terdiri dari cincin boroksol dan bukan unit BO3. Namun, G-B2SALAH SATU3 dapat mengkristal ke α-B2SALAH SATU3, yang akan menyiratkan interkonversi cincin ke segitiga, dan juga menentukan tingkat kristalisasi yang dicapai.
Properti
Penampilan fisik
Itu adalah padatan yang tidak berwarna dan kaca. Dalam bentuk kristalnya putih.
Massa molekul
69.6182 g/mol.
Rasa
Sedikit pahit
Kepadatan
-Kristal: 2.46 g/ml.
-Vitreous: 1.80g/ml.
Titik lebur
Itu tidak memiliki titik fusi yang sepenuhnya didefinisikan, karena tergantung pada bagaimana kristal atau vitreous itu. Bentuk kristal murni meleleh ke 450ºC; Namun, bentuk vitreous meleleh ke dalam kisaran suhu yang mencakup 300 hingga 700ºC.
Titik didih
Sekali lagi, nilai yang dilaporkan tidak cocok dengan nilai ini. Rupanya cairan boron oksida (cair dari kristal atau gelasnya) mendidih pada 1860ºC.
Stabilitas
Itu harus tetap kering, karena menyerap kelembaban untuk berubah menjadi asam borat, B (OH)3.
Tata nama
Boro oksida dapat dinamai dengan cara lain, seperti:
-Diboro Trioxide (Nomenklatur Sistematik).
-Boron oksida (III) (nomenklatur stok).
-Oksida borik (nomenklatur tradisional).
Aplikasi
Beberapa penggunaan boron oksida adalah:
Sintesis Boro Trihalogenuros
Dari b2SALAH SATU3 dapat disintesis oleh trihalogenuros de boro, bx3 (X = f, cl y br). Senyawa ini adalah asam Lewis, dan dengan mereka dimungkinkan untuk memperkenalkan atom boron ke molekul tertentu untuk mendapatkan turunan lainnya dengan sifat baru.
Itu dapat melayani Anda: Ion Poliatomik: Daftar dan LatihanInsektisida
Campuran padat dengan asam borat, b2SALAH SATU3-B (oh)3, mewakili formula yang digunakan sebagai insektisida domestik.
Pelarut oksida logam: pembentukan kaca, keramik dan paduan boron
Boron oksida cair mampu melarutkan logam oksida. Dari campuran yang dihasilkan ini, setelah didinginkan, padatan yang terdiri dari boron dan logam diperoleh.
Tergantung pada jumlah b2SALAH SATU3 Digunakan, serta teknik, dan jenis oksida logam, beragam kaca (borosilikat), keramik (nitrida dan karbida boron), dan paduan dapat diperoleh (jika hanya logam yang digunakan).
Secara umum, kaca atau keramik memperoleh resistensi dan kekuatan yang lebih besar, dan juga daya tahan yang lebih besar. Dalam kasus kaca, mereka akhirnya digunakan untuk lensa optik dan teleskop, dan untuk perangkat elektronik.
Bahan pengikat
Dalam konstruksi oven pengecoran baja, batu bata refraktori dengan magnesium digunakan. Di dalamnya, boron oksida digunakan sebagai pengikat, membantu menjaga mereka tetap bersatu dengan kuat.
Referensi
- Oksida borik. Pulih dari: pubchem.NCBI.Nlm.Nih.Pemerintah
- Borix oksida. 20 Borax Tim Mule. Pulih dari: borax.com

