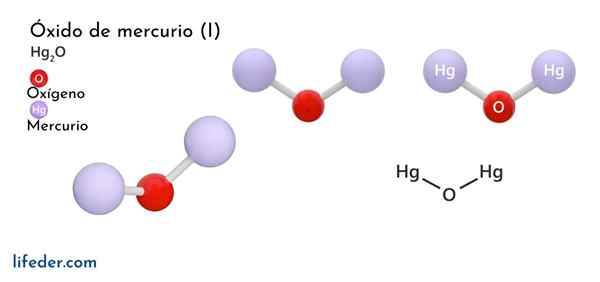
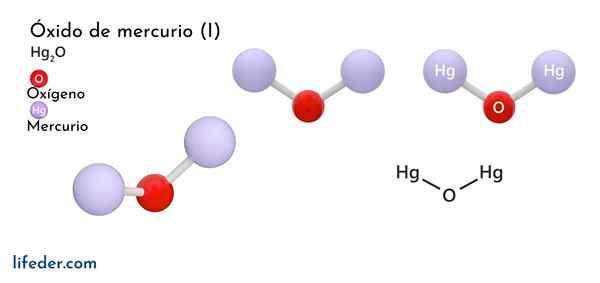
Merkuri oksida (HG2O)
- 4095
- 966
- Dewey Runolfsdottir
Apa itu merkuri oksida?
Dia Merkuri oksida (I) u ferric oxide, yang formula kimianya direpresentasikan sebagai Hg2Atau, ini adalah senyawa fase padat, dianggap sebagai toksik dan tidak stabil dari sudut pandang kimia, berubah menjadi merkuri menjadi bentuk dasar dan merkuri oksida (II).
Hanya ada dua spesies kimia yang dapat membentuk merkuri bila dikombinasikan dengan oksigen, karena logam ini hanya memiliki dua keadaan oksidasi (Hg+ dan hg2+): Merkuri oksida (I) dan merkuri oksida (II). Merkuri oksida (II) berada dalam keadaan agregasi padat, memperoleh dalam dua bentuk kristal yang relatif stabil.
Senyawa ini juga dikenal hanya sebagai merkuri oksida, jadi hanya spesies ini yang akan diperlakukan di sini. Reaksi yang sangat umum yang terjadi dengan zat ini adalah bahwa, ketika mengalami pemanasan, dekomposisinya terjadi, menghasilkan merkuri dan oksigen gas dalam proses endotermal.
Struktur kimia
Di bawah kondisi tekanan atmosfer, spesies ini disajikan dalam dua bentuk kristal: cinabrio yang disebut SO dan lainnya yang dikenal sebagai montrodite, yang sangat jarang. Kedua bentuk diubah menjadi tetragonal di atas 10 GPa tekanan.
Struktur Cinnabrio didasarkan pada sel heksagonal primitif (HP6) dengan simetri trigonal, yang sumbu heliksnya berorientasi ke kiri (P32dua puluh satu); Di sisi lain, struktur montrodite adalah ortorombik, berdasarkan pada kisi primitif yang membentuk bidang geser tegak lurus terhadap tiga sumbu (PNMA).
Sebaliknya, dua bentuk merkuri oksida dapat dibedakan secara visual, karena satu berwarna merah dan kuning lainnya. Perbedaan warna ini terjadi berkat dimensi partikel, karena kedua bentuk memiliki struktur yang sama.
Itu dapat melayani Anda: Circonium: Sejarah, sifat, struktur, risiko, penggunaanUntuk menghasilkan bentuk merah merkuri oksida, pemanasan merkuri logam dalam oksigen pada suhu sekitar 350 ° C, atau ke proses pirolisis nitrat merkuri (II) (Hg (NO3)2).
Dengan cara yang sama, menghasilkan bentuk kuning oksida ini2+ dalam bentuk berair dengan dasar.
Sifat merkuri oksida
- Ini memiliki titik leleh sekitar 500 ° C (setara dengan 773 K), di atasnya menderita dekomposisi, dan massa molar atau berat molekul 216,59 g/mol.
- Ini dalam keadaan agregasi padat dalam berbagai warna: oranye, merah atau kuning, sesuai dengan tingkat dispersi.
- Ini adalah oksida dari sifat anorganik, yang proporsinya dengan oksigen adalah 1: 1, yang menjadikannya spesies biner.
- Ini dianggap tidak larut dalam amonia, aseton, eter dan alkohol, serta dalam sifat organik lainnya.
- Kelarutannya dalam air sangat rendah, menjadi sekitar 0,0053 g/100ml pada suhu standar (25 ° C) dan meningkat dengan peningkatan suhu.
- Itu dianggap larut dalam sebagian besar asam; Namun, bentuk kuning menunjukkan reaktivitas yang lebih besar dan kapasitas yang lebih besar untuk pembubaran.
- Saat oksida merkuri terpapar dekomposisi, sementara bentuk merahnya melakukannya saat terpapar pada sumber cahaya.
- Dengan mengalami pemanasan hingga suhu di mana ia rusak, ia melepaskan gas merkuri toksisitas tinggi.
- Hanya saat dipanaskan hingga 300-350 ° C merkuri dapat dikombinasikan dengan oksigen pada tingkat yang menguntungkan.
Dapat melayani Anda: suspensi kimiaPenggunaan/Aplikasi
Ini digunakan sebagai prekursor dalam memperoleh merkuri dasar, karena menderita proses dekomposisi dengan cara yang cukup mudah; Pada gilirannya, saat membusuk menghasilkan oksigen dalam bentuk sodanya.
Demikian pula, oksida sifat anorganik ini digunakan sebagai agen penurunan nilai jenis standar untuk spesies anionik, karena senyawa dihasilkan yang memiliki stabilitas yang lebih besar daripada bentuk awalnya.
Dalam pengertian ini, merkuri oksida mengalami pembubaran ketika ditemukan dalam larutan terkonsentrasi spesies dasar, menghasilkan senyawa yang disebut hidrokokompleks.
Senyawa ini kompleks dengan struktur MX(OH)Dan, di mana m mewakili atom logam dan subskrip x y y mewakili berapa kali spesies ditemukan dalam molekul. Mereka sangat utilitas dalam investigasi kimia.
Selain itu, merkuri oksida (II) dapat digunakan di laboratorium untuk produksi garam logam yang berbeda; Misalnya, Merkurius Asetat (II), yang digunakan dalam proses sintesis organik.
Senyawa ini juga digunakan, ketika dicampur dengan grafit, sebagai bahan untuk elektroda katodik dalam produksi baterai merkuri dan listrik dan sel tipe seng oksida.
Risiko
- Zat ini, yang memanifestasikan karakteristik dasar dengan cara yang sangat lemah, adalah reagen yang sangat berguna untuk berbagai aplikasi seperti yang disebutkan di atas, tetapi pada gilirannya menghadirkan risiko penting bagi manusia ketika terpapar ini.
- Merkuri oksida memiliki toksisitas tinggi, dapat diserap oleh saluran pernapasan, karena ia mengeluarkan gas yang mengiritasi ketika dalam bentuk aerosol, selain menjadi sangat beracun jika dicerna atau jika diserap oleh kulit ketika itu bersentuhan langsung dengan ini.
Dapat melayani Anda: chirality- Senyawa ini menghasilkan iritasi mata dan dapat menyebabkan kerusakan pada ginjal yang kemudian berasal dari masalah gagal ginjal.
- Ketika dikonsumsi dengan satu atau lain cara oleh spesies perairan, bahan kimia ini adalah bioakumula dalam hal ini dan mempengaruhi organisme manusia yang secara teratur mengkonsumsinya.
- Pemanasan merkuri oksida berasal dari uap merkuri yang memiliki toksisitas tinggi selain oksigen gas, sehingga meningkatkan risiko mudah terbakar; yaitu, untuk menghasilkan kebakaran dan meningkatkan pembakaran di dalamnya.
- Oksida anorganik ini memiliki perilaku pengoksidasi yang kuat, sehingga menghasilkan reaksi kekerasan ketika bersentuhan dengan agen pereduksi dan zat kimia tertentu seperti belerang klorida (CL2S2), hidrogen peroksida (h2SALAH SATU2), klorin dan magnesium (hanya saat dia dipanaskan).