Etil asetat
- 3845
- 1142
- Frederick Pfeffer
Dia etil atau etil etana asetat Itu adalah senyawa organik yang formula kimianya adalah cho3Cooc2H5. Ini terdiri dari ester, di mana komponen alkohol berasal dari etanol, sedangkan komponen asam karboksilat berasal dari asam asetat.
Ini adalah cairan di bawah kondisi suhu dan tekanan normal, menghadirkan aroma yang menyenangkan untuk buah -buahan. Properti ini masuk dengan sempurna dalam harmoni sehingga diharapkan dari ester; yang sebenarnya adalah sifat kimia etil asetat. Untuk alasan ini ia menemukan penggunaan dalam produk makanan dan minuman beralkohol.
 Etil asetat. Sumber: Commons Wikimedia.
Etil asetat. Sumber: Commons Wikimedia. Gambar atas menunjukkan struktur kerangka etil asetatoda. Perhatikan komponen asam karboksilatnya, dan di sebelah kanan komponen alkohol. Dari sudut pandang struktural, senyawa ini dapat diharapkan berperilaku seperti hibrida antara cuka dan alkohol; Namun, ini menunjukkan propertinya sendiri.
Di sinilah hibrida yang disebut ester menonjol karena berbeda. Etil asetat tidak dapat bereaksi seperti asam, atau dehidrat dengan tidak adanya gugus OH. Sebaliknya, ia menderita hidrolisis dasar dengan adanya basis yang kuat, seperti natrium hidroksida, NaOH.
Reaksi hidrolisis ini digunakan dalam mengajar laboratorium untuk percobaan kinetika kimia; di mana reaksi, di samping itu, adalah urutan kedua. Saat hidrolisis terjadi, etano etil.
Dalam kerangka strukturalnya diamati bahwa atom hidrogen pada oksigen mendominasi. Ini mempengaruhi kemampuannya untuk berinteraksi dengan spesies kutub seperti lemak. Ini juga digunakan untuk melarutkan senyawa seperti resin, pewarna, dan secara umum padatan organik.
Meskipun memiliki aroma yang menyenangkan, paparan yang berkepanjangan untuk cairan ini menghasilkan dampak negatif (seperti hampir semua senyawa kimia) pada tubuh.
Struktur etil asetat
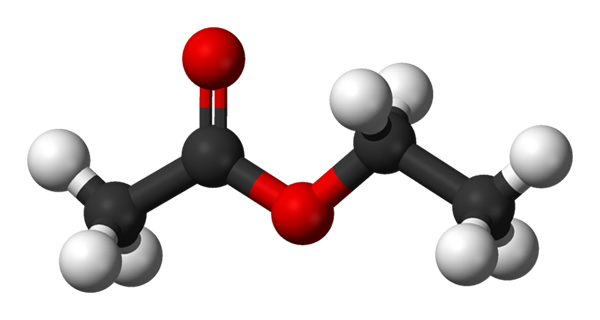
 Bola dan batang model untuk etil asetat. Sumber: Benjah-BMM27 [Domain Publik]
Bola dan batang model untuk etil asetat. Sumber: Benjah-BMM27 [Domain Publik] Gambar atas menunjukkan struktur etil asetat dengan model bola dan batang. Dalam model ini, atom oksigen dengan bola merah disorot; Di sebelah kirinya adalah fraksi yang berasal dari asam, dan di sebelah kanan fraksi yang berasal dari alkohol (alcoxi, -or).
Dapat melayani Anda: elektrolit lemah: konsep, karakteristik, contohGrup karbonil dapat dilihat dengan tautan C = O (bilah ganda). Struktur di sekitar kelompok ini dan oksigen yang berdekatan datar, karena ada relokasi beban resonansi antara kedua oksigen; Fakta yang menjelaskan keasaman hidrogen α yang relatif rendah (yang dari kelompok -ch3, ditautkan ke c = o).
Molekul, memutar dua tautannya, secara langsung menyukai bagaimana berinteraksi dengan molekul lain. Kehadiran dua atom oksigen, dan asimetri dalam struktur, memberikannya momen dipol permanen; yang pada gilirannya bertanggung jawab atas interaksi dipol-dipolnya.
Misalnya, kepadatan elektronik lebih besar di dekat dua atom oksigen, berkurang jauh pada kelompok -ch3, Dan secara bertahap di kelompok OCH2Ch3.
Karena interaksi ini, molekul etil asetat membentuk cairan dalam kondisi normal, yang memiliki titik didih yang sangat tinggi (77ºC).
Tidak adanya atom donor jembatan hidrogen
Jika struktur diamati dengan cermat, tidak adanya atom yang mampu menyumbangkan jembatan hidrogen akan diperhatikan. Namun, atom oksigen adalah akseptor dari itu, dan etil asetat sangat larut dalam air, dan berinteraksi dengan tingkat perkiraan dengan senyawa kutub dan donor jembatan hidrogen (seperti gula).
Ini juga memungkinkan Anda untuk berinteraksi dengan sangat baik dengan etanol; Alasan mengapa kehadirannya dalam minuman beralkohol tidak terkejut.
Di sisi lain, kelompok alcxi -nya membuatnya dapat berinteraksi dengan senyawa apolar tertentu, seperti kloroform, ch3Cl.
Sifat fisik dan kimia
Nama
-Etil asetat
-Etil etano
-Etil asetat
-Acetoxietano
Formula molekul
C4H8SALAH SATU2 atau ch3Cooc2H5
Berat molekul
88.106 g/mol.
Deskripsi Fisik
Cairan tidak berwarna bening.
Warna
Cairan tidak berwarna.
Bau
Karakteristik eter, mirip dengan bau nanas.
Rasa
Bagus saat diencerkan, itu membawa rasa buah ke bir.
Ambang bau
3,9 ppm. 0,0196 mg/m3 (bau rendah); 665 mg/m3 (Bau tinggi).
Dapat melayani Anda: ikatan kimiaBau yang dapat ditentukan pada 7 - 50 ppm (rata -rata = 8 ppm).
Titik didih
171 ºF pada 760 mmHg (77.1 ºC).
Titik lebur
-118.5 ºF (-83.8 ºC).
Kelarutan air
80 g/l.
Kelarutan dalam pelarut organik
Tidak dapat disembuhkan dengan etanol dan etil eter. Sangat larut dalam aseton dan benzena. Larut dengan kloroform, minyak tetap dan volatil, dan juga dengan pelarut teroksigenasi dan terklorinasi.
Kepadatan
0.9003 g/cm3.
Kepadatan uap
3.04 (dalam hubungan udara: 1).
Stabilitas
Ini terurai perlahan dengan kelembaban; tidak sesuai dengan beberapa plastik dan agen pengoksidasi yang kuat. Campuran dengan air bisa menjadi eksplosif.
Tekanan uap
93.2 mmHg pada 25 ºC
Zat yang lengket dan kental
0,423 MPOISE pada 25 ° C.
Panas pembakaran
2.238.1 kJ/mol.
Panas penguapan
35,60 kJ/mol pada 25 ºC.
Tegangan permukaan
24 dynas/cm pada 20 ºC.
Indeks bias
1.373 hingga 20 ºC/D.
Suhu penyimpanan
2 - 8 ºC.
PKA
16 - 18 hingga 25 ºC.
Perpaduan
Reaksi Fisher
Etil asetat disintesis secara industri oleh reaksi Fisher, di mana etanol diesterifikasi dengan asam asetat. Reaksi dilakukan pada suhu kamar.
Ch3Ch2Oh +ch3COOH CH3Cooch2Ch3 + H2SALAH SATU
Reaksi dipercepat dengan katalisis asam. Keseimbangan bergerak ke kanan, yaitu, menuju produksi etil asetat, dengan menghilangkan air; Menurut hukum aksi massal.
Reaksi Tishchenko
Ethyl Acetate juga disiapkan secara industri menggunakan reaksi Tishchenko, mengkonjugasikan dua asetaldehyde setara dengan penggunaan katalis sebagai katalis.
2 ch3Cho => cho3Cooch2Ch3
Metode lain
-Etil asetat disintesis sebagai produk ko -produk dalam oksidasi butana menjadi asam asetat, dalam reaksi yang dibuat pada suhu 175 ºC dan 50 atm tekanan. Ini digunakan sebagai katalis kobalt dan ion krom.
-Ethyl acetate adalah produk ko -product dari etanoly polivinil polivinil asetat.
-Etil asetat juga diproduksi dalam industri ini dengan dehidrogenasi etanol, mengkatalisasi reaksi dengan menggunakan tembaga pada suhu tinggi, tetapi kurang dari 250 ºC.
Aplikasi
Pelarut
Etil asetat digunakan sebagai pelarut dan pengencer, menggunakan pembersihan papan sirkuit. Ini digunakan sebagai pelarut dalam pembuatan ekstrak hop yang dimodifikasi, dan pada kopi dan daun teh yang berdosa. Itu digunakan dalam tinta yang digunakan untuk menandai buah dan sayuran.
Itu dapat melayani Anda: asam cyanhydric: struktur molekul, sifat, penggunaanEtil asetat digunakan dalam industri tekstil sebagai agen pembersih. Digunakan dalam kalibrasi termometer, digunakan dalam pemisahan gula. Dalam industri cat digunakan sebagai pelarut dan pengencer bahan yang digunakan.
Rasa buatan
Ini digunakan dalam elaborasi rasa buah; Misalnya: pisang, pir, persik dan nanas, serta aroma anggur, dll.
Analitik
Ini digunakan dalam penentuan bismut, boron, emas, molibdenum dan platinum, serta pelarut talium. Etil asetat memiliki kemampuan untuk mengekstraksi banyak senyawa dan elemen yang ada dalam larutan air, seperti: fosfor, kobalt, tungsten dan arsenik.
Sintesis organik
Ethyl Acetate digunakan dalam industri sebagai peredam dalam viskositas resin yang digunakan dalam formulasi photorestoning. Ini digunakan dalam produksi asetamida, asetil asetat dan metil heptanon.
Kromatografi
Di laboratorium, etil asetat digunakan sebagai fase gerak kromatografi dalam kolom dan sebagai pelarut ekstraksi. Memiliki etil asetat titik didih yang relatif rendah, mudah untuk diuapkan, yang memungkinkan Anda untuk memusatkan zat terlarut dalam pelarut.
Ilmu serangga
Ethyl Acetate digunakan dalam entomologi untuk mencekik serangga yang ditempatkan dalam wadah, memungkinkan pengumpulan dan studinya. Uap etil asetat membunuh serangga tanpa menghancurkannya dan menghindari pengerasan mereka, memfasilitasi perakitan koleksi mereka.
Risiko
-Ldlima puluh Dari etil asetat pada tikus, ini menunjukkan toksisitas rendah. Namun, itu bisa mengiritasi kulit, mata, kulit, hidung dan tenggorokan.
-Paparan ke tingkat tinggi dapat menyebabkan pusing dan pingsan. Demikian juga, paparan jangka panjang dapat mempengaruhi hati dan ginjal.
-Inhalasi etil asetat pada konsentrasi 20.000 - 43.000 ppm, dapat menghasilkan edema dan perdarahan paru.
-Batas pameran tenaga kerja telah ditetapkan oleh OSHA pada 400 ppm di udara, rata -rata, selama shift kerja 8 jam.
Referensi
- Glosarium Ilustrasi Kimia Organik: Ethhyl Acetate (EtOAC). Pulih dari: chem.UCLA.Edu
- Ethyl asetat. Diperoleh dari: CHM.Bris.Ac.Inggris

