Alkohol
- 1370
- 85
- Herbert Fritsch
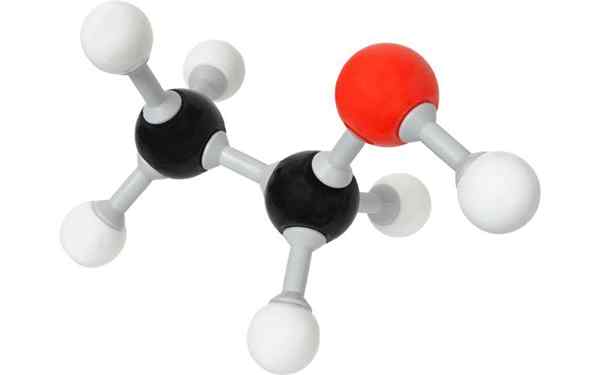
 Molekul etanol, atau etil alkohol. Dengan lisensi
Molekul etanol, atau etil alkohol. Dengan lisensi Apa itu alkohol?
Itu Alkohol Mereka adalah senyawa organik yang ditandai dengan memiliki gugus hidroksil (-OH) yang terkait dengan karbon jenuh, yaitu karbon yang terkait dengan empat atom dengan ikatan sederhana (tanpa tautan ganda atau tiga)).
Formula generik untuk keluarga senyawa yang luas dan serbaguna ini adalah ROH. Untuk dianggap sebagai alkohol dalam pengertian kimia yang ketat, kelompok OH harus menjadi yang paling reaktif dari struktur molekul. Ini penting untuk ditegaskan, di antara beberapa molekul dengan kelompok OH, yang mana dari mereka adalah alkohol.
Salah satu alkohol par excellence dan yang paling terkenal dalam budaya populer adalah etil alkohol, atau etanol, ch3Ch2Oh. Tergantung pada asal alami mereka, dan oleh karena itu lingkungan kimianya, campuran mereka dapat menyebabkan spektrum rasa yang tidak terbatas, beberapa, yang bahkan menunjukkan perubahan positif pada langit -langit seiring.
Struktur alkohol
Alkohol memiliki formula ROH umum. Kelompok OH terkait dengan kelompok alquilis, yang strukturnya bervariasi dari satu alkohol ke alkohol lainnya. Persatuan antara R dan OH adalah tautan kovalen sederhana, R-oh.
Gambar berikut menunjukkan tiga struktur generik untuk alkohol, mengingat bahwa atom karbon jenuh, yaitu, membentuk empat tautan sederhana.
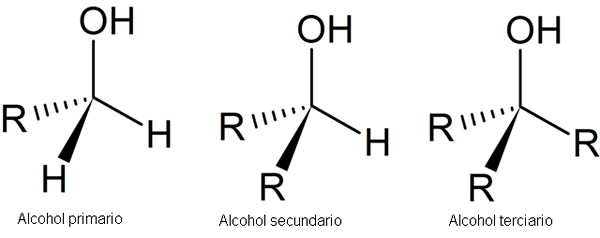 Struktur alkohol. Sumber: Secalinum, Wikimedia Commons
Struktur alkohol. Sumber: Secalinum, Wikimedia Commons Seperti dapat dilihat, R dapat berupa struktur berkarbonasi selama tidak memiliki substituen yang lebih reaktif daripada kelompok OH.
Dalam kasus alkohol primer, 1, kelompok OH terkait dengan karbon primer. Ini mudah diverifikasi dengan mengamati bahwa atom di tengah tetrahedron kiri terkait dengan R dan dua jam.
Alkohol sekunder, ke -2, diverifikasi dengan karbon tetrahedron pusat yang sekarang terkait dengan dua kelompok R dan h.
Dan akhirnya, Anda memiliki alkohol tersier, ke -3, dengan karbon terkait dengan tiga kelompok R.
Karakter Amphifile
Bergantung pada jenis karbon yang terkait dengan OH, Anda memiliki klasifikasi alkohol primer, sekunder dan tersier. Di tetrahedra perbedaan struktural di antara mereka sudah terperinci. Tapi semua alkohol, terlepas dari strukturnya, berbagi kesamaan: karakter amphiphile.
Tidak perlu mengatasi struktur untuk memperhatikannya, tetapi cukup dengan formula kimianya ROH. Kelompok sewa hampir seluruhnya dibentuk.
Di sisi lain, gugus OH dapat membentuk jembatan hidrogen dengan molekul air, oleh karena itu menjadi hidrofil, yaitu, ia menghadirkan afinitas terhadap air. Kemudian, alkohol memiliki kerangka hidrofobik, bersama dengan kelompok hidrofilik. Mereka apolar dan kutub pada saat yang sama, yang sama dengan mengatakan bahwa mereka adalah zat amfifil.
Dapat melayani Anda: Perbedaan antara campuran homogen dan campuran heterogenR-OH
(Hidrofobik) - (hidrofilik)
Seperti yang akan dijelaskan di bagian selanjutnya, karakter amfifil alkohol mendefinisikan beberapa sifat kimianya.
Struktur r
Grup Renta dapat memiliki struktur apa pun, namun penting karena memungkinkan alkohol untuk diklasifikasikan.
Misalnya, R dapat berupa rantai terbuka, seperti halnya dengan etanol atau propanol, bercabang, seperti alkohol T-butil (CH3)2Chch2Oh, ini bisa siklis, seperti dalam kasus sikloheksanol, atau dapat memiliki cincin aromatik, seperti pada benzil alkohol (c6H5) Ch2Oh, atau dalam 3-fenilpropanol (c6H5) Ch2Ch2Ch2Oh.
Rantai R bahkan dapat memiliki substituen seperti halogen atau ikatan rangkap, seperti untuk alkohol 2 sel dan 2-bunt-1-ol (CH3Ch2= Chch2OH).
Mempertimbangkan struktur R, klasifikasi alkohol menjadi kompleks. Oleh karena itu, klasifikasi berdasarkan strukturnya (alkohol ke -1, ke -2 dan ke -3) lebih mudah tetapi kurang spesifik, meskipun cukup untuk menjelaskan reaktivitas alkohol.
Sifat fisik dan kimia
- Titik didih: Salah satu sifat utama alkohol adalah bahwa mereka dikaitkan melalui jembatan hidrogen. Berkat ini, alkohol biasanya cair dengan titik didih yang tinggi.
- Kapasitas pelarut: Di rumah sangat umum untuk menggunakan alkohol isopropil untuk menghilangkan noda yang sulit dihapus di permukaan. Kapasitas pelarut ini, sangat berguna untuk sintesis kimia, disebabkan oleh karakter amphropifilnya, yang sebelumnya dijelaskan. Lemak ditandai dengan menjadi hidrofobik: itu sebabnya sulit untuk menghilangkannya dengan air. Namun, tidak seperti air, alkohol memiliki bagian hidrofobik dalam strukturnya. Dengan demikian, kelompoknya, Renta R berinteraksi dengan lemak, sedangkan kelompok OH membentuk jembatan hidrogen dengan air, membantu memindahkannya.
- Anfoterisme: Alkohol dapat bereaksi sebagai asam dan basa, yaitu, mereka adalah zat amfoten. Ini diwakili dengan dua persamaan kimia berikut:
ROH + H+ => RoH2+
ROH + oh- => Ro-
Ro- Ini adalah formula umum dari apa yang dikenal sebagai alkekum.
Tata nama
Ada dua cara untuk menyebutkan alkohol, yang kompleksitasnya akan tergantung pada strukturnya.
Nama yang umum
Alkohol dapat dipanggil untuk nama umum mereka. Untuk melakukan ini, nama grup R harus diketahui, yang ditambahkan -ICO akhir, dan didahului oleh kata 'alkohol'. Misalnya, Cho3Ch2Ch2Oh adalah alkohol propylico.
Dapat melayani Anda: sistem heterogenContoh lainnya adalah:
- Ch3Oh: Methyl Alkohol.
- (Ch3)2Chch2Oh: Isobutyl Alkohol.
- (Ch3)3COH: alkohol tert-boutil.
Sistem IUPAC
Adapun nama umum, Anda harus mulai dengan mengidentifikasi r. Keuntungan dari sistem ini adalah jauh lebih tepat daripada yang lain.
A, karena itu adalah kerangka karbon, ia dapat memiliki konsekuensi atau beberapa rantai. Rantai terpanjang, yaitu, dengan lebih banyak atom karbon, adalah nama alkohol akan diberikan.
Nama rantai terpanjang ditambahkan ke nama alkana, penghentian 'l' ditambahkan. Itulah sebabnya Cho3Ch2Oh disebut etanol (cho3Ch2- + OH).
Umumnya, OH harus memiliki enumerasi sesedikit mungkin. Misalnya, BRCH2Ch2Ch2(Oh) cho3 Ini disebut 4-bromo-2-butanol, dan bukan 1-bromo-3-butanol.
Perpaduan
Hidrasi Alkena
Proses craaking minyak menghasilkan campuran empat atau lima atom karbon, yang dapat dengan mudah memisahkan.
Alkena ini dapat menjadi alkohol dengan penambahan air langsung atau dengan reaksi alkena dengan asam sulfat, diikuti oleh penambahan air yang dibagi asam, yang berasal dari alkohol.
Proses oxo
Di hadapan katalis yang memadai, alkena bereaksi dengan karbon dan hidrogen monoksida untuk menghasilkan aldehida. Aldehida dapat dengan mudah dikurangi menjadi alkohol dengan reaksi hidrogenasi katalitik.
Seringkali ada sinkronisasi proses OXO sehingga pengurangan aldehida hampir simultan dengan pembentukannya.
Katalis yang paling banyak digunakan adalah dekobalto octocarbonil, diperoleh dengan reaksi antara kobalt dan karbon monoksida.
Fermentasi karbohidrat
Fermentasi karbohidrat untuk ragi masih sangat penting dalam produksi etanol dan alkohol lainnya. Gula berasal dari tebu atau pati yang diperoleh dari butiran yang berbeda. Untuk alasan ini, etanol juga disebut "alkohol gandum"
Aplikasi
Minuman
- Meskipun ini bukan fungsi utama alkohol, keberadaan etanol dalam beberapa minuman adalah salah satu pengetahuan yang paling populer. Dengan demikian, etanol, produk fermentasi tebu, anggur, apel, dll., Ini ada dalam berbagai minuman konsumsi sosial.
Bahan baku kimia
- Metanol digunakan dalam produksi formaldehida, melalui oksidasi katalitiknya. Formaldehyde digunakan dalam pembuatan plastik, lukisan, tekstil, bahan peledak, dll.
- Butanol digunakan dalam produksi butanoat butana, ester yang digunakan sebagai penyedap di industri makanan dan permen.
- Alkohol Allyic digunakan dalam produksi ester, termasuk phthalate dialilo dan dialilo isftalate, yang berfungsi sebagai monomer.
- Fenol ini digunakan dalam produksi resin, pembuatan nilon, deodoran, kosmetik, dll.
- Alkohol rantai linier dari 11-16 atom karbon digunakan sebagai perantara untuk mendapatkan plasticizer. Misalnya, polivinil klorida.
- Alkohol berlemak yang disebut SO digunakan sebagai perantara dalam sintesis deterjen.
Pelarut
- Metanol digunakan sebagai pelarut cat, serta alkohol 1-butanol dan isobutilik.
- Etil alkohol digunakan sebagai pelarut dari banyak senyawa yang tidak larut di dalam air, digunakan sebagai pelarut dalam lukisan, kosmetik, dll.
- Alkohol berlemak digunakan sebagai pelarut di industri tekstil, pada pewarna, dalam deterjen dan lukisan. Isobutanol digunakan sebagai pelarut dalam bahan pelapis, lukisan dan perekat.
Bahan bakar
- Metanol digunakan sebagai bahan bakar dalam mesin bensin internal dan aditif untuk meningkatkan pembakaran.
- Etil alkohol digunakan dalam kombinasi dengan bahan bakar fosil pada kendaraan bermotor. Untuk itu, daerah luas Brasil dimaksudkan untuk penanaman tebu untuk produksi etil alkohol. Alkohol ini memiliki keuntungan memproduksi dalam pembakarannya hanya karbon dioksida. Saat etil alkohol terbakar, ia menghasilkan nyala api yang bersih dan tanpa asap, itulah sebabnya ia digunakan sebagai bahan bakar di dapur kampanye.
- Alkohol Gelified diproduksi dengan kombinasi metanol atau etanol dengan kalsium asetat. Alkohol ini digunakan sebagai sumber panas dalam kompor kampanye, dan karena tumpah itu lebih aman daripada alkohol cair.
- Biobutanol yang disebut SO digunakan sebagai bahan bakar transportasi, serta alkohol isoproplik, meskipun penggunaannya tidak disarankan.
Antiseptik
- Konsentrasi 70% Isopropil alkohol digunakan sebagai antiseptik eksternal untuk penghapusan kuman dan keterbelakangan pertumbuhannya, seperti halnya etil alkohol.
Penggunaan lainnya
- Cyclohexanol dan Methylciclohexanol digunakan dalam lapisan tekstil, furnitur yang diproses dan chitamanchas.
Contoh alkohol dan formulasinya
- Metanol (ch3OH).
- 1-propanol (c3H7OH).
- Etanol (c2H5OH).
- Isobutanol (c4H9OH).
- Isopropanol (c3H8SALAH SATU).
- Alkohol allilic (c3H6SALAH SATU).
- Benzyl alkohol (c7H8SALAH SATU).
- Termal (c₄h₁₀o).
- Pentenol (c5HsebelasOH).
- 2-butanol (ch3-Ch2-Choh-ch3).
- Fenol (c6H6SALAH SATU).
- 2-propanol (ch3-Choh-ch3).
- Isodecanol (c10H21OH).
- Alkohol cetyl (c16H3. 4SALAH SATU).
- Alkohol propargilic (c3H4SALAH SATU).
- Alkohol tetrahydrofurilic (c5H10SALAH SATU2).
- Sikloheksanol (c6H12SALAH SATU).
- 2-chlorotanol (c2H5Clo.
- Heptanol (c7H16SALAH SATU).
- Hexanol (c₆h₁₄o).
Referensi
- Kimia organik. MC Graw Hill.
- Alkohol. Diperoleh dari Colapret.cm.Utexas.Edu.

