Alkena
- 3326
- 589
- Miss Marion Graham
 Alkena atau olefin adalah hidrokarbon tak jenuh yang memiliki setidaknya ikatan karbon karbon ganda dalam strukturnya
Alkena atau olefin adalah hidrokarbon tak jenuh yang memiliki setidaknya ikatan karbon karbon ganda dalam strukturnya Apa itu alkena?
Itu alkena atau olefin Mereka adalah hidrokarbon tak jenuh yang memiliki setidaknya ikatan rangkap dalam strukturnya. Mereka disebut olefin karena kemampuan etene atau etilen untuk bereaksi dengan halogen untuk menghasilkan minyak atau minyak. Saat ini, istilah olefinas telah tidak digunakan dan senyawa ini sekarang disebut alkena.
Sifat fisik alkena dipengaruhi oleh berat molekulnya, serta kerangka berkarbonasi mereka. Misalnya, alkena dengan 2 hingga 4 karbon (buteno etene) adalah gas. Dengan 5 hingga 18 atom karbon dalam rantai panjang adalah cairan. Sedangkan alkena dengan lebih dari 18 atom karbon padat.
Kehadiran ikatan rangkap memberikan reaktivitas besar, sehingga mengalami banyak reaksi kimia, seperti penambahan, eliminasi, hidrogenasi, hidrasi dan polimerisasi, yang memungkinkannya menghasilkan banyak kegunaan dan aplikasi.
Alkena diproduksi secara industri oleh retak termal dengan berat molekul tinggi (lilin parafin); Dehidrogenasi katalitik dan klorinasi-dehidrokloklinasi.
Struktur kimia alkena
 Sumber: Made sendiri
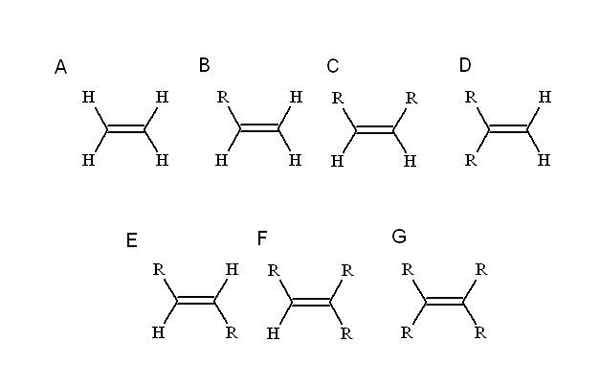
Sumber: Made sendiri Alkena ditandai dengan memiliki satu atau lebih tautan ganda dalam strukturnya. Ini direpresentasikan sebagai c = c, memiliki kedua atom karbon hibridisasi sp2.
Oleh karena itu, wilayah rantai di mana ikatan rangkap atau tidak jenuh, datar. Juga merupakan Meritor untuk menunjukkan bahwa kedua karbon dapat dikaitkan dengan dua substituen lainnya (atau kelompok).
Substituen yang mana? Siapa pun yang menggantikan salah satu hidrogen alkene paling sederhana: etilen (atau eteno). Mulai dari dia (A, Image Superior) R, yang merupakan substituen alquilis, menempati tempat salah satu dari empat hidrogen yang menyebabkan alkene mono-tersubstitusi (b).
Sejauh ini, terlepas dari hidrogen mana yang diganti, identitas B tidak diubah. Ini berarti bahwa ia tidak memiliki stereoisomer, disusun dengan formula kimia yang sama tetapi dengan disposisi spasial yang berbeda dari atom -atomnya.
Dapat melayani Anda: titik kesetaraanStereoisomer
Ketika hidrogen kedua digantikan oleh R lain, seperti pada C, sekarang stereoisomer C, D dan E. Ini karena orientasi spasial sehubungan dengan kedua R dapat bervariasi, dan untuk saling membedakan, penugasan CIS-Trans atau E-Z digunakan.
Dalam C, alkena di-substitut, kedua R dapat berupa rantai dengan panjang apa pun atau heteroátomo. Satu berada dalam posisi frontal dalam kaitannya dengan yang lain. Jika keduanya terdiri dari substituen yang sama, f, misalnya, maka C adalah stereoisomer-cis.
Di D, kedua kelompok R bahkan lebih dekat, karena mereka terkait dengan atom karbon yang sama. Ini adalah stereoisomer geminal, meskipun lebih dari stereoisomer, sebenarnya adalah ikatan rangkap terminal, yaitu, pada akhirnya atau prinsip rantai (karena alasan itu memiliki dua hidrogen karbon lainnya).
Dan di E, stereoisomer yang paling stabil (atau isomer geometris), kedua kelompok R dipisahkan oleh jarak yang lebih besar, yang melintasi diagonal ikatan rangkap. Mengapa yang paling stabil? Itu karena karena pemisahan spasial di antara mereka lebih besar, jadi tidak ada ketegangan saudara perempuan di antara keduanya.
Di sisi lain, F dan G masing-masing adalah alken yang ditransmisikan oleh tetra dan tetra. Sekali lagi, mereka tidak dapat menghasilkan stereoisomer apa pun.
Sifat fisik dan kimia alkena
Kelarutan
Mereka tidak bisa dimengerti dengan air karena polaritasnya yang rendah. Tetapi mereka larut dalam pelarut organik.
Titik fusi pada ºC
Etano -169, Propeno -185, 1 -Pentine -165, 1 -hepteno -119, 3 -toctein
-101.9, 3 -none -81.4 dan 5 -dechenum -66,3.
Titik didih di º C
Etano -104, propeno -47, trans2buteno 0,9, cis2buteno 3,7, 1-penten 30, 1-hepteno 115, 3-OK 122, 3-noneno 147 dan 5-decend.
Dapat melayani Anda: filter laboratorium): Karakteristik, fungsi, jenisTitik didih meningkat dalam hubungan langsung dengan jumlah karbon alkena. Di sisi lain, semakin banyak bercabang strukturnya, yang terlemah adalah interaksi antarmolekulnya, yang tercermin dalam penurunan titik mendidih atau fusi.
Kepadatan
Etano 0,6128 mg/ml, propeno 0,6142 mg/ml dan 1-butene 0,6356 mg/ml, 1-pente 0,64 mg/mL dan 1-hexen 0,673.
Pada alkena kepadatan maksimum adalah 0,80 mg/ml. Yaitu, mereka kurang padat dari air.
Polaritas
Itu tergantung pada struktur kimia, substitusi dan adanya kelompok fungsional lainnya. Alkena memiliki dipmers, dengan demikian isomer cis 2-butene.
Reaktivitas alkena
Alkena memiliki kapasitas besar untuk bereaksi karena tautan ganda yang mereka miliki. Di antara reaksi yang terlibat adalah: penambahan, eliminasi, penggantian, hidrogenasi, hidrasi dan polimerisasi.
Reaksi tambahan
H2C = ch2 + Cl2 => Clch2-CCLH2 (Ethylene Dichloride)
Reaksi hidrogenasi
Itu terjadi pada suhu tinggi dan di hadapan katalis yang memadai (PT, PD, atau dibagi dengan halus)
Ch2= Ch2 + H2 => Ch3-Ch3 (Etano)
Reaksi hidrasi
Reaksi yang merupakan sumber generasi alkohol dari turunan minyak:
H2C = ch2 + H2O => h3C-ch2Oh (etil alkohol)
Reaksi polimerisasi
Ethylene dengan adanya katalis seperti aluminium uji coba dan titanium tetrachloride polymeriza dalam polietilen, yang mengandung sekitar 800 atom karbon. Jenis polimer ini disebut polimer tambahan.
Penggunaan dan aplikasi alkena
Polimer
- Polyethylene kepadatan rendah digunakan dalam pembuatan tas, plastik rumah kaca, kemasan, piring, kapal, dll. Sementara kepadatan tinggi lebih kaku dan resisten secara mekanis, menggunakan dalam pembuatan kotak, furnitur, pelindung seperti helm dan lutut, mainan dan palet.
- Polypropylene, propylene polymer, digunakan dalam elaborasi wadah, lembaran, peralatan laboratorium, mainan, film kemasan, filamen sogas, pelapis dan karpet.
- Polyvinyl chloride (PVC) adalah polimer vinil klorida yang digunakan dalam pembuatan tabung, ubin untuk lantai, saluran, pintu dan bingkai jendela, dll.
- Polybutadiene, polimer 1,3-butadiene, dimaksudkan untuk pembuatan pita bantalan, selang dan sabuk kendaraan, serta untuk lapisan kaleng logam.
- Kopolimer etilen dan propilena digunakan dalam pembuatan selang, tubuh dan bagian sasis untuk tekstil, dll.
Alkena
- Mereka digunakan dalam mendapatkan pelarut seperti etilen glikol dan dioksan. Ethylene Glycol digunakan sebagai antibeku dalam radiator mobil.
- Ethylene adalah hormon tanaman yang mengendalikan pertumbuhannya, perkecambahan benih dan pengembangan buah -buahan. Oleh karena itu, ini digunakan untuk menginduksi pematangan pisang saat mereka mencapai tujuan mereka.
- Mereka digunakan sebagai bahan baku untuk pembuatan banyak senyawa seperti alkil halida, etilen oksida dan terutama etanol. Mereka juga memiliki penggunaan dalam industri, perawatan pribadi dan kedokteran.
- Mereka digunakan dalam memperoleh dan memproduksi pernis, deterjen, aldehida dan bahan bakar. 1.3-butadieno digunakan sebagai bahan baku dalam pembuatan karet sintetis.
Referensi
- Penugasan kimia. Sifat fisik alkena. Diambil dari: penugasan kimia.com
- Wikipedia. (2018). Alkena. Diambil dari: di.Wikipedia.org
- Libretteks Kimia. Sifat fisik alkena. Diambil dari: chem.Librettexts.org
- Whitten, Davis, Peck & Stanley. Kimia. (Edisi ke -8.). Pembelajaran Cengage.
- Francis a. Tortoiseshell. Kimia organik. (Edisi Keenam., Halaman 194). MC Graw Hill.
- Houchton Mifflin Harcourt. (2016). Alkena: formula molekuler dan struktural. Diambil dari: Cliffsnotes.com
- Chipera, Angie. (25 April 2017). Apa itu olefin dalam kimia? Ilmu pengetahuan. Diambil dari: Ilmu Pengetahuan.com

