Formula yang diserap panas, cara menghitungnya dan menyelesaikan latihan

- 4682
- 581
- Mr. Darrell Streich
Dia panas yang diserap Itu didefinisikan sebagai transfer energi antara dua tubuh pada suhu yang berbeda. Yang dengan suhu yang lebih rendah menyerap panas daripada pada suhu yang lebih tinggi. Ketika ini terjadi, energi termal zat yang menyerap panas meningkat, dan partikel -partikel yang menyusunnya bergetar lebih cepat, meningkatkan energi kinetiknya.
Ini dapat diterjemahkan menjadi peningkatan suhu atau perubahan keadaan. Misalnya bergerak dari padatan ke cairan, seperti es saat meleleh bersentuhan dengan air atau soda pada suhu kamar.
 Sendok teh logam menyerap panas kopi panas. Sumber: Pixabay.
Sendok teh logam menyerap panas kopi panas. Sumber: Pixabay. Berkat panas, mungkin juga objek mengubah dimensinya. Pelebaran termal adalah contoh yang baik dari fenomena ini. Ketika sebagian besar zat dipanaskan, mereka biasanya mengalami peningkatan dimensinya.
Pengecualian untuk ini adalah air. Jumlah air cair yang sama meningkatkan volumenya saat didinginkan di bawah 4 ºC. Selain itu, perubahan suhu juga dapat mengalami perubahan pada tingkat kepadatannya, sesuatu yang juga sangat dapat diamati dalam kasus air.
[TOC]
Apa itu dan formula
Dalam kasus energi dalam perjalanan, unit panas yang diserap adalah joule. Namun, untuk waktu yang lama panasnya memiliki unit sendiri: kalori.
Masih hari ini unit ini digunakan untuk mengukur kandungan energi makanan, meskipun dalam kenyataannya kalori makanan sesuai dengan kilokalori panas.
Kalori
Kalori, disingkat sebagai jeruk nipis, Itu adalah jumlah panas yang diperlukan untuk menaikkan suhu 1 gram air dengan 1 º C.
Pada abad ke -19, Sir James Prescott Joule (1818 - 1889) melakukan percobaan terkenal di mana ia berhasil mengubah pekerjaan mekanis menjadi panas, memperoleh kesetaraan berikut:
1 kalori = 4.186 Joules
Di unit Inggris, unit panas disebut btu (UNIT TERMAL Inggris), yang didefinisikan sebagai jumlah panas yang dibutuhkan untuk menaikkan suhu satu pon air dalam 1 ºF.
Itu dapat melayani Anda: Kurva Kalibrasi: Untuk apa itu, bagaimana melakukannya, contohKesetaraan antara unit adalah sebagai berikut:
1 btu = 252 kalori
Masalah dengan unit lama ini adalah jumlah panas tergantung pada suhu. Artinya, tidak sama dengan yang diperlukan untuk melewati dari 70 ºC hingga 75 ° C daripada yang dibutuhkan untuk memanaskan air dari 9 ° C hingga 10 ºC, misalnya.
Itulah sebabnya definisi tersebut merenungkan interval yang ditentukan dengan baik: 14.5 hingga 15.5 ° C dan 63 hingga 64 ° F untuk masing -masing kalori dan btu.
Apa yang tergantung pada jumlah panas yang diserap?
Jumlah panas yang diserap yang mengumpulkan bahan tergantung pada beberapa faktor:
- Massa. Semakin tinggi massa, semakin banyak panas yang mampu menyerap.
- Karakteristik substansi. Ada zat yang tergantung pada struktur molekul atau atomnya, mampu menyerap lebih banyak panas daripada yang lain.
- Suhu. Diperlukan untuk menambahkan lebih banyak panas untuk mendapatkan suhu yang lebih tinggi.
Jumlah panas, dilambangkan sebagai Q, Itu sebanding dengan faktor yang dijelaskan. Karena itu, Anda dapat menulis sebagai:
Q = m.C.ΔT
Di mana M Itu adalah massa objek, C adalah konstan yang dipanggil panas spesifik, sifat intrinsik dari zat dan δT Ini adalah variasi suhu yang dicapai dengan menyerap panas.
Δt = tF - Tsalah satu
Perbedaan ini memiliki tanda positif, karena saat menyerap panas diharapkan itu TF > Tsalah satu. Ini terjadi kecuali zat tersebut mengalami perubahan fase, seperti air saat cairan uap lewat. Saat air mendidih, suhunya tetap konstan pada sekitar 100 º C, terlepas dari seberapa cepatnya mendidih.
Cara menghitungnya?
Dengan menghubungi dua objek pada suhu yang berbeda, setelah beberapa saat keduanya mencapai keseimbangan termal. Jadi, suhu disamakan dan perpindahan panas berhenti. Hal yang sama terjadi jika lebih dari dua objek menghubungi. Setelah waktu tertentu, semua orang akan berada pada suhu yang sama.
Itu dapat melayani Anda: magnetisasi: momen magnetik orbital dan putaran, contohDengan asumsi bahwa objek dalam kontak membentuk sistem tertutup, dari mana panas tidak dapat melarikan diri, prinsip konservasi energi diterapkan, sehingga dapat ditegaskan bahwa:
Q terserap = - q Melesat
Ini mewakili keseimbangan energi, mirip dengan pintu masuk dan biaya seseorang. Itulah sebabnya panas ceded memiliki tanda negatif, karena untuk objek yang menghasilkan, suhu akhir lebih rendah dari awal. Karena itu:
Δt = tF - Tsalah satu < 0
Persamaan q terserap = - q Melesat Itu digunakan setiap kali dua objek bersentuhan.
Keseimbangan energi
Untuk melakukan keseimbangan energi, perlu untuk membedakan objek yang menyerap panas dari yang menghasilkan, lalu:
Σ qk= 0
Yaitu, jumlah keuntungan dan kerugian energi dalam sistem tertutup harus sama dengan 0.
Panas spesifik suatu zat
Untuk menghitung jumlah panas yang diserap, Anda perlu mengetahui panas spesifik dari setiap zat yang berpartisipasi. Ini adalah jumlah panas yang dibutuhkan untuk menaikkan suhu 1 g material dengan 1 º C. Unit -unitnya dalam sistem internasional adalah: joule/kg . K.
Ada tabel dengan panas spesifik dari berbagai zat, umumnya dihitung dengan menggunakan kalorimeter atau alat serupa.
Contoh cara menghitung panas spesifik suatu bahan
250 kalori diperlukan untuk menaikkan suhu cincin logam 20 hingga 30 ºC. Jika cincin memiliki massa 90 g. Apa panas panas spesifik di unit SI?
Larutan
Unit pertama kali dikonversi:
Q = 250 kalori = 1046.5 J
m = 90 g = 90 x 10-3 kg
Dapat melayani Anda: guncangan elastis: dalam dimensi, kasus khusus, latihan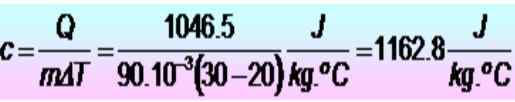
Olahraga diselesaikan
Cangkir aluminium berisi 225 g air dan agitator tembaga 40 g, semuanya pada 27 ° C. Sampel 400 g perak pada suhu awal 87 ° C ditempatkan di dalam air.
Agitator digunakan untuk mengaduk campuran sampai mencapai suhu kesetimbangan akhir 32 ° C. Hitung massa cangkir aluminium, mengingat tidak ada kerugian panas terhadap lingkungan.
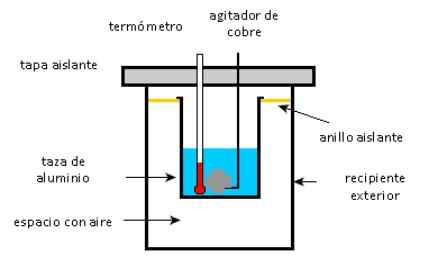 Skema kalorimeter. Sumber: Solidswiki.
Skema kalorimeter. Sumber: Solidswiki. Mendekati
Seperti yang dinyatakan di atas, penting untuk membedakan objek yang menghasilkan panas dari yang menyerap:
- Cangkir aluminium, tembaga dan agitator air menyerap panas.
- Sampel perak menghasilkan panas.
Data
Panas spesifik dari setiap zat disediakan:
- Perak: C = 234 J/kg. ºC
- Tembaga: C = 387 J/kg. ºC
- Aluminium C = 900 J/kg. ºC
- Air C = 4186 J/kg. ºC
Panas yang diserap atau ditetapkan oleh setiap zat dihitung dengan persamaan:
Q = m.C.λT
Larutan
Perak
Q Melesat = 400 x 10 -3 . 234 x (32 - 87) j = -5148 j
Agitator Tembaga
Q terserap = 40 x 10 -3 . 387 x (32 - 27) j = 77.4 J
Air
Q terserap = 225 x 10 -3 . 4186 x (32 - 27) j = 4709.25 J
Piala Aluminium
Q terserap = m aluminium . 900 x (32 - 27) j = 4500 .M aluminium
Melakukan penggunaan:
Σ qk= 0
77.4 + 4709.25 + 4500 .M aluminium = - (-5148)
Akhirnya massa aluminium dibersihkan:
M aluminium = 0.0803 kg = 80.3 g
Referensi
- Giancoli, d. 2006. Fisika: Prinsip dengan aplikasi. 6th. Ed. Prentice Hall. 400 - 410.
- Kirkpatrick, l. 2007. Fisika: Pandangan Dunia. 6ta Edisi Singkat. Pembelajaran Cengage. 156 - 164.
- Rex, a. 2011. Dasar -dasar fisika. Pearson. 309 - 332.
- Sears, Zemansky. 2016. Fisika Universitas dengan Fisika Modern. 14th. Volume1. 556 - 553.
- Serway, r., Vulle, c. 2011. Dasar -dasar fisika. 9na Pembelajaran Cengage. 362 - 374

