Struktur Kalium Karbonat (K2CO3), Properti, Penggunaan, Memperoleh

- 4596
- 112
- Leland Robel
Dia Kalium karbonat Itu adalah senyawa anorganik yang dibentuk oleh dua ion kalium k+ dan co ion batubara32-. Formula kimianya adalah k2BERSAMA3. Ini adalah padatan putih higroskopis, yaitu, mudah menyerap air dari lingkungan. Oleh karena itu di laboratorium digunakan untuk menyerap air dari zat lain.
Sangat larut dalam larutan alkali pembentuk air, yang kaya akan ion OH-dan karena itu dengan nilai pH yang tinggi. Larutan airnya, karena alkali, digunakan dalam beberapa proses industri untuk menyerap gas asam seperti karbon dioksida2 dan hidrogen sulfida h2S, lalu dengan mudah menetralisir mereka.
 Kalium karbonat k2BERSAMA3 padat. Ondřej Mangl [domain publik]. Sumber: Wikimedia Commons.
Kalium karbonat k2BERSAMA3 padat. Ondřej Mangl [domain publik]. Sumber: Wikimedia Commons. K2BERSAMA3 Ini digunakan untuk menyiapkan sabun, produk pembersih, deterjen untuk mencuci pakaian dan campuran untuk mencuci piring. Ini juga digunakan dalam pemrosesan beberapa serat tekstil seperti wol.
Ini banyak digunakan di laboratorium kimia, misalnya untuk menyerap air dari senyawa lain atau untuk alkalisasi campuran reaksi kimia dan juga dalam analisis kimia.
Ini juga ditambahkan ke beberapa makanan, misalnya, untuk menghilangkan rasa pahit biji kakao selama produksi cokelat.
[TOC]
Struktur
Kalium karbonat terdiri dari dua kalium kasium+ dan co anion karbonat32-. Anion karbonat memiliki struktur datar dan simetris, sedangkan tiga atom oksigen mengelilingi karbon yang membentuk segitiga datar.
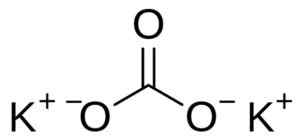 Struktur kalium karbonat k2BERSAMA3. Pengguna: Edgar181 [Domain Publik]. Sumber: Wikimedia Commons.
Struktur kalium karbonat k2BERSAMA3. Pengguna: Edgar181 [Domain Publik]. Sumber: Wikimedia Commons. Tata nama
- Kalium karbonat
- Kalium karbonat
- Dipotasium karbonat
- Kalium karbonat
- Garam kalium asam karbonat.
Properti
Keadaan fisik
Solid kristal tidak berwarna hingga putih.
Berat molekul
138.205 g/mol.
Titik lebur
899 ºC.
Titik didih
Itu membusuk.
Kepadatan
2.29 g/cm3
Kelarutan
Sangat larut dalam air: 111 g/100 g air pada 25 ° C. Tidak larut dalam etanol dan aseton.
Dapat melayani Anda: Kontribusi dari Kimia ke Kedokteranph
Larutan berair dapat memiliki pH 11,6, yaitu, cukup basa.
Sifat kimia
Kalium karbonat adalah lezat atau higroskopis, yaitu, ia menyerap kelembaban lingkungan. Itu memiliki hidrat yang stabil, k2BERSAMA3.2h2SALAH SATU.
K2BERSAMA3 Dalam larutan berair dihidrolisis, yaitu, bereaksi dengan air dengan melepaskan gugus OH- yang merupakan orang yang memberikan alkalinitas pada solusi:
BERSAMA32- + H2Atau ⇔ oh- + HCO3-
HCO3- + H2Atau ⇔ oh- + H2BERSAMA3
Memperoleh
Dapat diperoleh dari abu yang tersisa saat membakar tanaman. Juga oleh karbonasi KOH kalium hidroksida, yaitu, menambahkan kelebihan karbon dioksida CO2 Ke Koh:
KOH + CO2 → Khco3
2 KHCO3 + panas → k2BERSAMA3 + H2SALAH SATU
Cara lain untuk mendapatkannya adalah memanaskan KCL Kalium klorida dengan magnesium karbonat3, air dan rekannya2 dibawah tekanan. Magnesium terhidrasi ganda dan garam kalium dan kalium diperoleh terlebih dahulu3.Khco3.4H2Atau, disebut Salt Engels:
2 kcl + 3 mgco3 + BERSAMA2 + 5 jam2O → MGCO3.Khco3.4H2Atau ↓ + mgcl2
Garam terhidrasi ganda engel mengendap dan dipisahkan dari larutan dengan penyaringan. Kemudian karbonat mobil kalium dipanaskan dan terbentuk2BERSAMA3 itu dengan menambahkan air larut saat magnesium mgco karbonat3 tetap tidak larut dan dihilangkan dengan penyaringan.
Mgco3.Khco3.4H2O + panas → mgco3↓ + 2 k+ + BERSAMA32- + BERSAMA2↑ + 9 jam2SALAH SATU
Aplikasi
Dalam penyerapan CO2 Dalam proses industri
Larutan kalium karbonat adalah pengobatan klasik untuk co carbon dioksida co2 Dalam berbagai proses, terutama dalam aplikasi tekanan tinggi dan suhu.
 S Solusi2BERSAMA3 Mereka digunakan untuk menyerap CO2 Dalam berbagai proses industri. Penulis: Nicola Giordano. Sumber: Pixabay.
S Solusi2BERSAMA3 Mereka digunakan untuk menyerap CO2 Dalam berbagai proses industri. Penulis: Nicola Giordano. Sumber: Pixabay. Penghapusan CO2 terjadi sesuai dengan reaksi berikut:
K2BERSAMA3 + BERSAMA2 + H2Atau ⇔ 2 khco3
Metode ini digunakan misalnya untuk mengobati gas alam. Juga di pabrik pembangkit energi, untuk menghindari emisi CO2 ke atmosfer, dan dalam produksi es kering.
Dapat melayani Anda: tembaga hidroksida (ii): struktur, properti, nomenklatur, penggunaan S Solusi2BERSAMA3 Mereka digunakan untuk mendapatkan co2 yang berfungsi untuk membuat es kering. ProjectManhattan [CC BY-SA (https: // CreativeCommons.Org/lisensi/by-sa/3.0)]. Sumber: Wikimedia Commons.
S Solusi2BERSAMA3 Mereka digunakan untuk mendapatkan co2 yang berfungsi untuk membuat es kering. ProjectManhattan [CC BY-SA (https: // CreativeCommons.Org/lisensi/by-sa/3.0)]. Sumber: Wikimedia Commons. K -Solusi2BERSAMA3 Ini dapat beregenerasi secara termal, yaitu, karena suhu pemanasan sekitar 100 ° C.
Agar larutan kalium karbonat untuk menyerap CO2 dengan kecepatan yang baik, promotor ditambahkan yang mempercepat proses seperti dietanolamine (DEA).
Dalam penghapusan h2S dari proses tertentu
Larutan kalium karbonat juga digunakan untuk menghilangkan gas hidrogen sulfida h2S dari arus proses. Terkadang kalium tiffosfat k ditambahkan3PO4 Untuk membuat proses lebih cepat.
Di laboratorium kimia
K2BERSAMA3 memungkinkan sintesis organik, misalnya, dalam reaksi kondensasi dan untuk menetralkan. Itu berfungsi untuk menghilangkan air dari cairan organik, sebagai agen dehidrasi atau pengeringan di laboratorium.
Ini juga digunakan dalam reaksi kimia analitik dan untuk melakukan alkali di industri farmasi.
Di industri produk pembersih
K2BERSAMA3 Ini digunakan untuk memproduksi sabun, formula pembersih, produk untuk pakaian dan pencucian hidangan dan juga untuk menyiapkan sampo dan produk perawatan pribadi lainnya.
 K2BERSAMA3 Ini digunakan dalam persiapan sabun. LaCrosus [domain publik]. Sumber: Wikimedia Commons.
K2BERSAMA3 Ini digunakan dalam persiapan sabun. LaCrosus [domain publik]. Sumber: Wikimedia Commons. Di industri makanan
Kalium karbonat ditambahkan ke berbagai makanan dengan beberapa tujuan.
Misalnya, ditambahkan ke biji kakao untuk menghilangkan rasa pahit mereka dan menggunakannya dalam produksi cokelat. Itu ditambahkan ke anggur dalam proses pengeringan untuk mendapatkan anggur yang kencang.
 Biji kakao diperlakukan dengan k2BERSAMA3 Untuk mengurangi rasanya pahit saat membuat cokelat. Penulis: Couret Magali. Sumber: Pixabay.
Biji kakao diperlakukan dengan k2BERSAMA3 Untuk mengurangi rasanya pahit saat membuat cokelat. Penulis: Couret Magali. Sumber: Pixabay. Di toko kue digunakan sebagai leudant (bertindak sebagai ragi) dari tepung untuk menyiapkan makanan yang dipanggang.
Dapat melayani Anda: lutecio: struktur, sifat, penggunaan, mendapatkan K2BERSAMA3 Itu dapat digunakan sebagai ledant dalam kue karena saat mengeluarkan CO2 Selama memasak ini peningkatan volume. Penulis: Pixel1. Sumber: Pixabay.com
K2BERSAMA3 Itu dapat digunakan sebagai ledant dalam kue karena saat mengeluarkan CO2 Selama memasak ini peningkatan volume. Penulis: Pixel1. Sumber: Pixabay.com Di pupuk
K2BERSAMA3 Ini digunakan untuk menyuburkan tanah asam, seperti co ion batubara32- Kontak dengan air menghasilkan ion OH- yang meningkatkan pH tanah. Selain kalium k+ Ini adalah nutrisi untuk tanaman.
Kalium karbonat juga telah digunakan untuk membuat pupuk pelepasan lambat.
Pupuk pelepasan lambat atau nutrisi longgar sehingga tidak dilarutkan dan diseret oleh air. Berkat ini, mereka dapat menghabiskan lebih banyak waktu yang tersedia untuk akar tanaman.
Dalam beberapa aplikasi
Kalium karbonat k2BERSAMA3 Itu juga digunakan untuk:
- Proses pembersihan pengeringan, pemutihan dan bersih dan kegiatan industri tekstil lainnya
- Memperoleh garam kalium organik dan anorganik lainnya, seperti KCN kalium sianida.
- Berfungsi sebagai regulator keasaman dalam berbagai proses.
- Buat keramik dan tembikar.
- Proses ukiran dan litografi.
- Tan.
- Siapkan tinta cetak, pigmen.
- Kaca manufacce2BERSAMA3 Itu lebih kompatibel daripada naisat naisat na2BERSAMA3 Dengan timbal, barium dan strontium oksida yang mengandung kaca ini.
- Pengolahan air.
- Tunda api (dalam bentuk solusi air).
- Menghambat korosi dan sebagai agen anti-sela dalam tim proses.
Referensi
- ATAU.S. Perpustakaan Kedokteran Nasional. (2019). Kalium karbonat. Pulih dari pubchem.NCBI.Nlm.Nih.Pemerintah.
- Steele, d. (1966). Kimia elemen logam. Pergamon Press Ltd. London.
- Mokhatab, s. et al. (2019). Perawatan Gas Alam. Larutan kalium karbonat. Dalam Buku Pegangan Transmisi dan Pemrosesan Gas Alam (Edisi Keempat). Pulih dari scientedirect.com.
- Kakaras, e. et al. (2012). Sistem siklus gabungan fluidized tertekan (PFBC). Pembakaran bed fluidisasi bertekanan dengan penangkapan dan penyimpanan karbon. Dalam sistem siklus gabungan untuk pembangkit listrik emisi hampir nol. Pulih dari scientedirect.com.
- Speight, J.G. (2019). Produksi hidrogen. Menggosok basah. Dalam pemulihan dan peningkatan minyak berat. Pulih dari scientedirect.com.
- Branan, c.R. (2005). Perawatan Gas: Bab yang diperbarui oleh Chris Higman. Proses karbonat panas. Dalam Aturan Jempol untuk Insinyur Kimia (Edisi Keempat). Pulih dari scientedirect.com.
- Kirk-Othmer (1994). Encyclopedia of Chemical Technology. Edisi keempat. John Wiley & Sons.
- Ensiklopedia Kimia Industri Ullmann. (1990). Edisi Kelima. Vch verlagsgellschaft mbh.
- Li, dan. dan Cheng, F. (2016). Sintesis pupuk kalium pelepasan lambat baru dari slag magnesium pidgeon yang dimodifikasi oleh kalium karbonat. J Air Waste Manag Assoc, 2016 Agustus; 66 (8): 758-67. NCBI pulih.Nlm.Nih.Pemerintah.

