Struktur, penggunaan, konformasi sikloheksan
- 1879
- 102
- Mr. Darrell Streich
Dia Sikloheksan Ini adalah siklus yang relatif stabil dengan formula molekul C6H12. Ini adalah cairan yang tidak berwarna dan mudah terbakar yang memiliki aroma pelarut lembut, tetapi itu bisa menembus kotoran.
Ini memiliki kepadatan 0,779 g/cm3; Rebus pada 80,7 ° C; dan membeku pada 6,4 ° C. Itu dianggap tidak larut di dalam air, karena kelarutannya hanya bisa hanya 50 ppm (kira -kira.) pada suhu kamar. Namun, mudah dicampur dengan alkohol, eter, kloroform, benzena dan aseton.
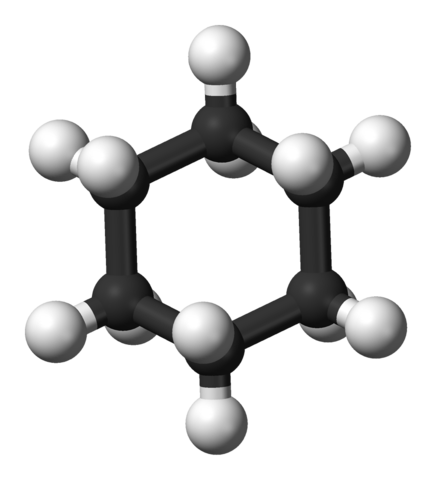
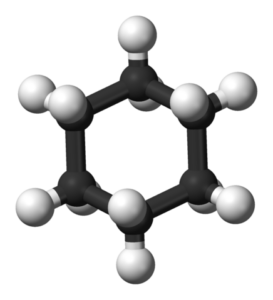 Model 3D molekul sikloheksana. Jynto dan Ben Mills / Domain Publik
Model 3D molekul sikloheksana. Jynto dan Ben Mills / Domain Publik Sistem cincin cychaxan lebih umum di antara molekul organik alam daripada sikloalcanos lainnya. Ini mungkin karena stabilitasnya dan selektivitas yang ditawarkan oleh konformasi yang didirikan dengan baik.
Faktanya, karbohidrat, steroid, produk tanaman, pestisida dan banyak senyawa penting lainnya mengandung cincin yang mirip dengan cyclohexan, yang konformasi sangat penting untuk reaktivitas mereka.
[TOC]
Struktur
Cyclohexan adalah hidrokarbon alicklic enam anggota. Ada terutama dalam konformasi di mana semua ikatan C-H dalam atom karbon tetangga terhuyung-huyung, dengan sudut dihedral sama dengan 60 °.
Karena memiliki sudut dan ketegangan torsi terendah. Ini juga membuat sikloheksan.
Posisi substituen
Ada dua jenis posisi untuk substituen dalam cincin sikloheksan: posisi aksial dan posisi khatulistiwa. Tautan khatulistiwa C-H ditemukan dalam sebuah pita di sekitar ecuador ring.
Pada gilirannya, setiap atom karbon memiliki hidrogen aksial yang tegak lurus terhadap bidang cincin dan sejajar dengan porosnya. Hidrogen aksial bergantian ke atas dan ke bawah; Setiap atom karbon memiliki posisi aksial dan khatulistiwa; Dan setiap sisi cincin memiliki tiga posisi aksial dan tiga ekuatorial dalam pengaturan alternatif.
Dapat melayani Anda: natrium karbonat (NA2CO3)Model Studi
Cyclohexan lebih baik mempelajari model molekuler fisik atau dengan program pemodelan molekuler. Ketika salah satu dari model ini digunakan, dimungkinkan untuk dengan mudah mengamati hubungan puntir dan orientasi atom hidrogen dan aksial atom.
Namun, disposisi atom hidrogen juga dapat dianalisis dalam proyeksi Newman saat mengamati pasangan tautan C-C paralel apa pun.
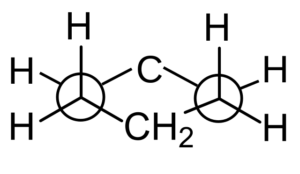 Proyeksi Newman dari Cychaxan. Durfo / CC0
Proyeksi Newman dari Cychaxan. Durfo / CC0 Konformasi
Cyclohexan dapat terjadi dalam dua konformasi yang dapat diselingi: perahu dan kursi. Namun, yang terakhir adalah konformasi yang paling stabil, karena tidak ada sudut atau tegangan torsional dalam struktur sikloheksan; Lebih dari 99% molekul berada dalam konformasi kursi pada waktu tertentu.
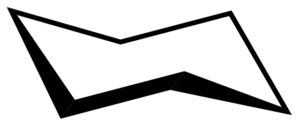 Konformasi kursi cychaxan. Chem Sim 2001 / Domain Publik
Konformasi kursi cychaxan. Chem Sim 2001 / Domain Publik Konformasi kursi
Dalam konformasi kursi, semua sudut tautan C-C adalah 109,5 °, yang melepaskannya dari tegangan sudut. Karena tautan C-C sangat terhuyung-huyung, konformasi kursi juga bebas dari ketegangan torsional. Selain itu, atom hidrogen di sudut yang berlawanan dari cincin sikloheksan dipisahkan hingga maksimum.
Formasi perahu
Konformasi kursi dapat mengambil bentuk lain yang disebut Formasi Perahu. Ini terjadi sebagai akibat dari rotasi parsial pada ikatan C-C sederhana. Konformasi seperti itu juga tidak memiliki ketegangan sudut, tetapi memang memiliki ketegangan torsional.
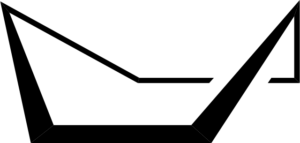 Konformasi perahu sikloheksan. Keministi / domain publik
Konformasi perahu sikloheksan. Keministi / domain publik Ketika Anda melihat model konformasi kapal, di sumbu tautan C-C di setiap sisi, ditemukan bahwa ikatan C-H dalam atom karbon tersebut dikalahkan, menghasilkan tegangan torsional.
Itu dapat melayani Anda: turunan benzenaSelain itu, dua atom hidrogen cukup dekat satu sama lain untuk menghasilkan gaya tolakan van der Waals.
Bajingan
Jika konformasi perahu ditekuk, konformasi kapal bengkok yang dapat meringankan bagian dari tegangan torsional dan juga mengurangi interaksi antara atom hidrogen diperoleh.
Namun, stabilitas yang diperoleh dengan fleksi tidak cukup untuk membuat konformasi perahu bengkok lebih stabil daripada konformasi kursi.
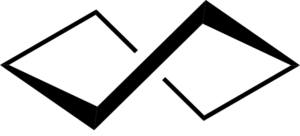 Konformasi perahu crooly cyclohexan. Keministi / CC0
Konformasi perahu crooly cyclohexan. Keministi / CC0 Aplikasi
Pembuatan nilon
Hampir seluruh sikloheksan yang terjadi secara komersial (lebih dari 98%) banyak digunakan sebagai bahan baku dalam produksi industri prekursor nilon: asam adipat (60%), caprolactam dan hexamethylendiamine. 75% dari caprolactam yang diproduksi di seluruh dunia digunakan untuk pembuatan nilon 6.
 Gitar dengan tali nilon. Sumber: Pexels.com
Gitar dengan tali nilon. Sumber: Pexels.com Pembuatan senyawa lain
Namun, cyclohexan juga digunakan dalam pembuatan benzena, sikloheksil klorida, nitrocylohexan, sikloheksanol dan sikloheksanon; dalam pembuatan bahan bakar padat; dalam formulasi fungisida; dan dalam rekristalisasi industri steroid.
Aplikasi minoritas
Fraksi yang sangat kecil dari siklus yang diproduksi digunakan sebagai pelarut non -polar untuk industri kimia dan pengencer dalam reaksi polimer. Ini juga dapat digunakan sebagai penghapus cat dan pernis; dalam ekstraksi minyak esensial; dan pengganti kaca.
Karena sifat kimia dan konformasi yang unik, sikloheksana juga digunakan di laboratorium kimia analitik untuk penentuan berat badan molekul dan sebagai standar.
Pembuatan
Proses tradisional
Cyclohexan hadir dalam minyak mentah dalam konsentrasi yang bervariasi antara 0.1 dan 1.0%. Oleh karena itu, dulu diproduksi secara tradisional oleh distilasi fraksional bensin di mana konsentrat sikloheksana 85% diperoleh dengan berlebihan.
Dapat melayani Anda: atom karbon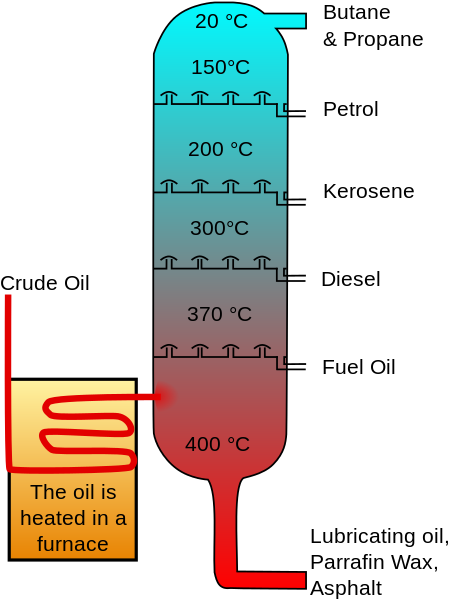 Distilasi minyak fraksinasi. Crude_oil_distilation-Fr.SVG: Gambar Asli: Psaria, Theresa Knott; Image Vectorielle: RogilberTerivative Work: UTain ()/CC BY-SA (http: // createveCommons.Org/lisensi/by-sa/3.0/)
Distilasi minyak fraksinasi. Crude_oil_distilation-Fr.SVG: Gambar Asli: Psaria, Theresa Knott; Image Vectorielle: RogilberTerivative Work: UTain ()/CC BY-SA (http: // createveCommons.Org/lisensi/by-sa/3.0/) Konsentrat ini dijual, karena pemurnian tambahan yang diperlukan untuk melakukan proses isomerisasi pentans, retak panas untuk menghilangkan hidrokarbon rantai terbuka dan perlakuan asam sulfat untuk menghilangkan senyawa aromatik.
Sebagian besar kesulitan mendapatkan sikloheksana dengan kemurnian yang lebih besar adalah karena sejumlah besar komponen minyak dengan titik didih yang sama.
Proses efisiensi tinggi
Saat ini, sikloheksana terjadi pada skala industri dengan bereaksi benzena dengan hidrogen (hidrogenasi katalitik) karena kesederhanaan proses dan efisiensinya yang tinggi.
Reaksi ini dapat dilakukan dengan menggunakan metode fase cairan atau uap dengan adanya katalis yang sangat tersebar atau di lapisan katalitik tetap. Beberapa proses telah dikembangkan di mana nikel, platinum atau paladium digunakan sebagai katalis.
Sebagian besar tanaman sikloheksana menggunakan gas reformer yang diproduksi oleh benzena dan sejumlah besar hidrogen dengan produk sebagai bahan baku untuk produksi sikloheksana.
Karena biaya hidrogen dan benzena sangat penting untuk pembuatan sikloheksana dengan cara yang menguntungkan, tanaman biasanya terletak di dekat kilang besar di mana bahan baku berbakti rendah tersedia.
Referensi
- Campbell, m. L. (2014). Sikloheksana. Ensiklopedia Kimia Industri Ullmann (7th ed.). New York: John Wiley & Sons.
- McMurry, J. (2011). Dasar -dasar Kimia Organik (7th ed.). Belmont: Brooks/Cole.
- Pusat Nasional Informasi Bioteknologi. (2020) Database pubchem. Sikloheksana, cid = 8078. Bethesda: Perpustakaan Kedokteran Nasional. Pulih dari: pubchem.NCBI.Nlm.Nih.Pemerintah
- Ouellette, r. J., & Rawn, J. D. (2014). Kimia Organik - Struktur, Mekanisme, dan Sintesis. San Diego: Elsevier.
- Petrucci, r. H., Herring, f. G., Bissonnette, c., & Dewasa, j. D. (2017). Kimia Umum: Prinsip dan Aplikasi Modern (11th ed.). New York: Pearson.
- Solomon, t. W., Fryhle, c. B., & Snyder, s. KE. (2016). Kimia Organik (12th ed.). Hoboken: John Wiley & Sons.
- Wade, l. G. (2013). Kimia Organik (edisi ke -8.). New York. Pearson.

