Asam hiposulfur
- 995
- 157
- Irvin Reichel
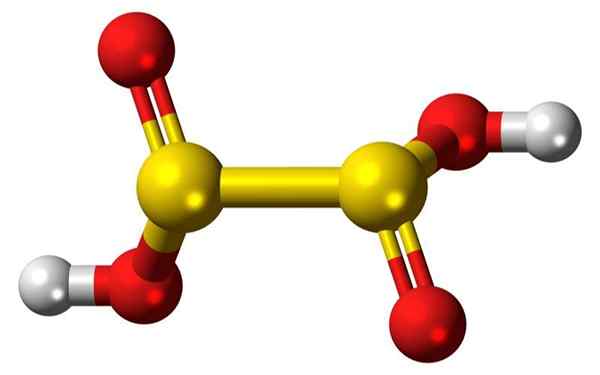
 Batang 3D batang dan balon molekul asam hiposulfirus. Sumber: Jynto
Batang 3D batang dan balon molekul asam hiposulfirus. Sumber: Jynto Apa itu asam hiposulfirus?
Dia Asam hiposulfur, o asam dionat, tidak diketahui, tidak stabil murni, tidak memiliki keberadaan independen dan belum terdeteksi dalam larutan air.
Secara teoritis, itu akan menjadi asam yang relatif lemah, sebanding dengan asam belerang, H2SO3. Hanya garamnya yang diketahui, dionitos, yang stabil dan agen pereduksi yang kuat. Garam asam natrium dionat adalah natrium dionito.
Rumus
Formula asam hiposulfurus adalah sebagai berikut:
Asam Dionat: h2S2SALAH SATU4
Dionito Anion: S2O42−
Sodium Dionito: NA2S2SALAH SATU4
Nomor CAS: 20196-46-7 Asam hiposulfurous (atau dital)
Nomor CAS: 14844-07-6 asam hiposulfurous (atau dition, ion)
Nomor CAS: 7775-14-6 Sodium Dionito (Sodium Sodium Asam Ditoring)
Sifat fisik dan kimia
- Dalam garam natrium dionito, penampilannya adalah kristal, putih hingga debu keabu -abuan, dengan serpihan hijau sulfur yang ringan dan lemah.
- Berat molekul asam tited adalah 130.132 g/mol. Anion Dionito, 128.116 g/mol, dan natrium dionito, 174.096 g/mol.
- Pada titik mendidih natrium dionito, ia membusuk, dan titik lelehnya adalah 52 ° C.
- Kepadatan natrium dionito adalah 2.38 g/cm³ (anhydrous), dan kelarutannya dalam air adalah 18.2 g/100 ml (anhidrat, 20 ° C).
- Asam hyposulfurous adalah sulfur oxoacid dengan formula kimia H2S2SALAH SATU4.
- Oxoacid belerang adalah senyawa kimia yang mengandung sulfur, oksigen dan hidrogen. Namun, beberapa dari mereka hanya dikenal karena garamnya (seperti asam hiposulfur, asam ditionic, asam disulfida dan asam sulfur).
Itu dapat melayani Anda: piridin: struktur, sifat, penggunaan, toksisitas, sintesisDi antara karakteristik struktural oxoacid yang kita miliki:
- Sulfur tetrahedral saat dikoordinasikan dengan oksigen.
- Atom oksigen di jembatan dan terminal.
- Kelompok periodinal.
- Terminal s = s.
- Rantai (-s-) n
Asam sulfat adalah oxoacid sulfur paling terkenal.
- Anion Dionito ([s2SALAH SATU4] 2-) adalah oxoanion (ion dengan rumus generik axoy z-) dari sulfur yang secara formal berasal dari asam ditionic.
- Ion dionito mengalami hidrolisis asam dan alkali hingga tiosulfat dan bisulfit, dan sulfit dan sulfida.
- Garam asam natrium dionat adalah natrium dionit (juga dikenal sebagai natrium hidrosulfit).
- Dapat diperoleh dari natrium bisulfit melalui reaksi berikut:
2 nahso3 + Zn → NA2Sw4 + Zn (oh) ²
Aplikasi
Ion dionit sering digunakan bersamaan dengan zat kompleks (misalnya, asam sitrat), untuk mengurangi besi oxi-hidroksida (III) dalam senyawa besi terlarut (II) dan menghilangkan fase mineral amorf yang mengandung zat besi (III) di tanah Analisis (ekstraksi selektif).
Dionito memungkinkan untuk meningkatkan kelarutan besi. Berkat afinitas yang kuat dari Ion Dionito untuk kation logam bivalen dan trivalen, ini digunakan sebagai agen pengkelat.
Dekomposisi Dionito menghasilkan spesies sulfur yang berkurang yang bisa sangat agresif untuk korosi baja dan stainless steel.
Di antara aplikasi natrium dionito yang kami miliki:
Di industri
- Senyawa ini adalah garam yang larut dalam air, dan dapat digunakan sebagai zat pereduksi dalam larutan berair.
- Ini digunakan seperti itu dalam beberapa proses pewarna industri, terutama yang melibatkan pewarna sulfur dan pewarna tub, di mana pewarna yang tidak larut air dapat dikurangi menjadi garam logam alkali yang larut dalam air (misalnya, pewarna indigo).
Dapat melayani Anda: asam: karakteristik dan contoh- Sifat reduksi natrium dionito juga menghilangkan kelebihan pewarna, residu oksida dan pigmen yang tidak diinginkan, sehingga meningkatkan kualitas warna global.
- Sodium Dionito juga dapat digunakan untuk pengolahan air, pemurnian gas, pembersihan dan ekstraksi. Ini juga dapat digunakan dalam proses industri seperti zat sulfonan atau sumber natrium.
- Selain industri tekstil, senyawa ini digunakan dalam industri yang berhubungan dengan kulit, makanan, polimer, fotografi, dan banyak lainnya. Ini juga digunakan sebagai agen dekolorasi dalam reaksi organik.
Dalam ilmu biologi
- Sodium Dionito sering digunakan dalam percobaan fisiologi sebagai sarana untuk mengurangi potensi redoks dari solusi.
Dalam Ilmu Geologi
- Sodium Dionito sering digunakan dalam percobaan kimia tanah untuk menentukan jumlah zat besi yang tidak dimasukkan dalam mineral silikat primer.
Keamanan dan risiko
Manipulasi elemen ini harus dilakukan dalam kondisi perawatan yang ekstrem. Ini sangat beracun dan dapat bereaksi berbahaya dalam hubungannya dengan air dan udara.
Selanjutnya, kami menyoroti beberapa aspek.
Reaksi udara dan air
- Sodium dionito adalah bahan bakar padat yang terurai perlahan saat bersentuhan dengan air atau uap air, membentuk tiosulfat dan bisulfit.
- Reaksi ini menghasilkan panas, yang selanjutnya dapat mempercepat reaksi atau menyebabkan bahan di sekitarnya terbakar. Jika campuran terbatas, reaksi dekomposisi dapat mengakibatkan tekanan wadah, yang dapat dipatahkan dengan kuat. Saat tetap di udara, ia mengoksidasi perlahan, menghasilkan gas sulfur dioksida beracun.
Dapat melayani Anda: nitrofuran: karakteristik, mekanisme aksi dan klasifikasiBahaya kebakaran
- Sodium Dionito adalah bahan yang mudah terbakar dan mudah terbakar. Dapat meradang kontak dengan udara basah atau kelembaban. Anda dapat dengan cepat membakar dengan efek suar. Dapat bereaksi dengan kuat atau eksplosif dalam kontak dengan air.
- Dapat dipecah secara eksplosif saat dipanaskan atau terlibat dalam api. Dapat hidup lagi setelah api padam. Limpasan dapat menciptakan bahaya api atau ledakan. Wadah dapat meledak saat dipanaskan.
Bahaya kesehatan
- Setelah bersentuhan dengan api, natrium dionito akan menghasilkan gas yang mengiritasi, korosif dan/atau beracun. Menghirup produk dekomposisi dapat menyebabkan cedera serius atau kematian. Kontak dengan zat dapat menyebabkan luka bakar yang serius pada kulit dan mata. Limpasan kontrol kebakaran dapat menyebabkan kontaminasi.
Referensi
- Benjah-BMM27 (2006). Model ball-and-stick dari ion dititonit [gambar] yang dipulihkan dari.Wikipedia.org.
- Mills, b. (2009). Sodium-Dithionite -tal-1992-3D-bola [gambar] dipulihkan dari: di.Wikipedia.org.

