Struktur kromat seng, sifat, memperoleh, menggunakan
- 2947
- 47
- Ernesto Mueller
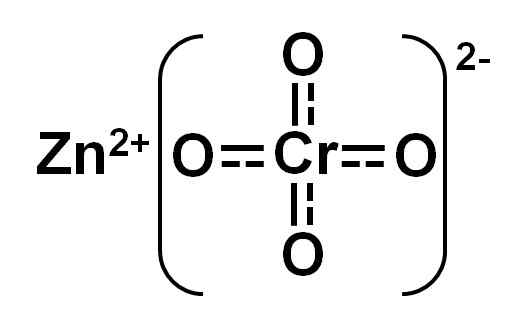
Dia Seng Chromate O CINC Chromate adalah senyawa anorganik yang dibentuk oleh elemen seng (Zn), krom (CR) dan oksigen (O) (O). Itu memiliki ion Zn2+ dan cro42-. Formula kimianya adalah Zncro4.
Istilah 'kromat seng' secara komersial berfungsi secara komersial untuk menunjuk tiga senyawa dengan struktur molekul yang berbeda: (a) kromat seng yang tepat zncro4, (B) Kromat dasar FIFCRO4• 4ZN (OH)2, dan (c) kromat dasar seng dan 3zncro kalium4• zn (oh)2• k2Cro4• 2H2SALAH SATU.
 Struktur kromat seng. Penulis: Marilú Stea.
Struktur kromat seng. Penulis: Marilú Stea. Ini terutama digunakan dalam lukisan atau dana yang melindungi logam korosi. Untuk melakukan ini, dicampur dengan lukisan, pernis dan polimer yang kemudian dioleskan pada permukaan logam.
Ini juga digunakan dalam lapisan dekoratif dan pelindung yang dicapai dengan kromat lain dan asam yang melapisi berbagai objek seperti alat. Itu juga berfungsi untuk mempertahankan konduktivitas listrik dari bagian logam.
Ini digunakan sebagai katalis dalam reaksi hidrogenasi (penambahan hidrogen) dalam senyawa organik. Itu adalah bagian dari pigmen yang sebelumnya digunakan dalam lukisan artistik.
Ini adalah bahan yang menghasilkan kanker dan ini karena kromat memiliki krom dalam keadaan oksidasi +6.
[TOC]
Struktur
 Chromate Zincro4 Itu adalah senyawa kuning. Penulis: Marilú Stea.
Chromate Zincro4 Itu adalah senyawa kuning. Penulis: Marilú Stea. Seng kromat adalah senyawa ionik yang dibentuk oleh lima belas kation zn2+ dan anion cromato42-. Yang terakhir dibentuk oleh Chrome dengan Valencia +6 (Hexavalent Chrome, Cr6+) dan empat atom oksigen dengan keadaan oksidasi -2.
Ion Zn2+ Ini memiliki struktur elektronik berikut:
1s2, 2s2 2 p6, 3S2 3p6 3d10.
Untuk bagiannya, chrome heksavalen memiliki orbital elektroniknya pada konformasi berikut:
1s2, 2s2 2 p6, 3S2 3p6.
Kedua struktur sangat stabil karena orbital selesai.
Tata nama
- Seng Chromate
- Garam seng asam kromik
- Seng kuning (walaupun dengan istilah ini senyawa lain yang mengandung zncro juga disebut4).
Properti
Keadaan fisik
Padatan kristal kuning lemon kuning. Kristal berbentuk prisma.
Berat molekul
181.4 g/mol
Titik lebur
316 ºC
Kepadatan
3,40 g/cm3
Kelarutan
Air larut dalam air: 3,08 g/100 g h2SALAH SATU. Itu mudah dilarutkan dalam asam dan amonia cair. Tidak larut dalam aseton.
Dapat melayani Anda: konstanta ionisasiph
Menurut beberapa sumber, solusi air mereka bersifat asam.
Sifat kimia
Ini adalah senyawa yang sangat mengoksidasi, sehingga dapat bereaksi dengan agen pereduksi menghasilkan panas. Di antara zat yang dapat bereaksi organik, seperti sianida, ester dan tiocianates. Anda juga dapat menyerang beberapa logam.
Dalam larutan air, ion kromat menyajikan berbagai saldo tergantung pada pH dan membentuk spesies yang berbeda.
Spesies yang dibentuk oleh chromate
Di atas pH 6 hadir ion cromato42- (kuning); Antara pH 2 dan pH 6 adalah ion HCRO dalam keseimbangan4- dan CR Dichromate2SALAH SATU72- (oranye merah); pada pH kurang dari 1 spesies utama adalah h2Cro4.
Ketika kation seng (II) ditambahkan ke larutan berair ini, Zncro endapan4.
Saldo adalah sebagai berikut:
Hcro4- ⇔ cro42- + H+
H2Cro4 ⇔ hcro4- + H+
Cr2SALAH SATU72- + H2Atau ⇔ 2 hcro4-
Dalam medium dasar berikut ini terjadi:
Cr2SALAH SATU72- + Oh- ⇔ hcro4- + Cro42-
Hcro4- + Oh- ⇔ cro42- + H2SALAH SATU
Zncro4 Itu tidak bereaksi cepat dengan udara atau air.
Memperoleh
Ini dapat diproduksi dengan bereaksi lumpur berair seng oksida atau hidroksida dengan garam kromat terlarut dan kemudian menetralkan.
Secara industri, proses cronak digunakan, di mana kabut logam direndam dalam larutan natrium dikromat (NA2Cr2SALAH SATU7) dan asam sulfat (h2Sw4).
Ini juga dapat disiapkan dengan memicunya dari larutan di mana ada seng yang larut dan garam kromat:
K2Cro4 + Znso4 → Zncro4↓ + k2Sw4
Aplikasi
Dalam perlindungan logam
Dalam industri metalurgi ini terutama digunakan dalam lukisan latar belakang (cat persiapan atau lapisan awal) yang diterapkan pada logam, yang memberikan ketahanan korosi korosi.
Ini digunakan sebagai pigmen dalam lukisan dan pernis, dimasukkan ke dalam matriks polimer organik.
Jenis cat ini diberikan pada pipa, tangki minyak, struktur baja seperti jembatan, menara transmisi daya listrik dan bagian mobil untuk menghambat korosi.
 Struktur baja jembatan dicat dengan dasar kromat seng sebelum cat akhir untuk melindunginya dari korosi. Penulis: オギクボ マンサク. Sumber: Pixabay.
Struktur baja jembatan dicat dengan dasar kromat seng sebelum cat akhir untuk melindunginya dari korosi. Penulis: オギクボ マンサク. Sumber: Pixabay. Pasifan
Ini juga melindungi komponen logam yang ditutupi dengan seng yang telah dilewatkan menggunakan kromat logam alkali. Pasifan terdiri dari hilangnya reaktivitas kimia dalam kondisi lingkungan tertentu.
Dapat melayani Anda: sel elektrokimiaPelapis ini juga berfungsi sebagai hasil akhir dekoratif dan untuk mempertahankan konduktivitas listrik. Mereka biasanya berlaku untuk artikel harian seperti alat dan dapat dikenali dengan warna kuningnya.
 Beberapa alat ditutupi dengan seng kromat. Penulis: Duk. Sumber: Wikimedia Commons.
Beberapa alat ditutupi dengan seng kromat. Penulis: Duk. Sumber: Wikimedia Commons. bagaimana cara kerjanya
Penyelidik tertentu menemukan bahwa perlindungan terhadap korosi logam yang dilakukan oleh fi -kromat bisa disebabkan oleh fakta bahwa itu menghambat pertumbuhan jamur. Dengan cara ini kerusakan lapisan cat anti -korosif.
Studi lain menunjukkan bahwa efek anti korosif bisa karena senyawa mempercepat pembentukan oksida pelindung pada logam.
 Latar belakang antikorosif seng kromat untuk perlindungan permukaan logam. 水水/cc by-sa (https: // createveCommons.Org/lisensi/by-sa/4.0). Sumber: Wikimedia Commons.
Latar belakang antikorosif seng kromat untuk perlindungan permukaan logam. 水水/cc by-sa (https: // createveCommons.Org/lisensi/by-sa/4.0). Sumber: Wikimedia Commons. Katalisis Reaksi
Senyawa ini telah digunakan sebagai katalis dalam berbagai reaksi kimia, seperti karbon monoksida hidrogenasi (CO) untuk mendapatkan metanol (CH3OH).
Ester dapat dikonversi menjadi alkohol primer dengan hidrogenasi, menggunakan senyawa ini untuk mempercepat reaksi.
Menurut beberapa peneliti, tindakan katalitiknya adalah karena fakta bahwa padatan tidak menghadirkan struktur stoikiometrik, yaitu, ia menyimpang dari formula Zncro -nya4 Dan itu lebih tepatnya:
Zn1-xCr2-xSALAH SATU4
Yang menyiratkan bahwa ada cacat dalam struktur yang secara energik mendukung katalisis.
Aplikasi lain
Ditemukan di beberapa pewarna berminyak, berfungsi untuk dicetak, ini adalah agen untuk perawatan permukaan, diterapkan di lantai lantai dan merupakan reagen di laboratorium kimia.
Penggunaan yang dihentikan
Sejak tahun 1940 -an, turunan Zncro digunakan4, Seng dan tembaga, sebagai fungisida foliar untuk tanaman kentang.
 Tanaman paus. Penulis: Dirk (Beeki®) Schumacher. Sumber: Pixabay.
Tanaman paus. Penulis: Dirk (Beeki®) Schumacher. Sumber: Pixabay. Penggunaan ini telah ditinggalkan oleh toksisitas dan efek berbahaya dari senyawa.
Dalam lukisan artistik abad kesembilan belas, keberadaan garam kromat seng kompleks telah ditemukan, 4Zncro4• k2Atau • 3H2O (seng kromat dan kalium terhidrasi), yang merupakan pigmen kuning yang disebut lemon kuning.
Dapat melayani Anda: lithium chloride (LICL): properti, risiko dan penggunaanRisiko
Meskipun bukan bahan bakar, saat dipanaskan, ia memancarkan gas beracun. Dapat meledak jika Anda bersentuhan dengan agen pereduksi atau bahan organik.
Debu mengiritasi mata dan reaksi alergi yang menghasilkan kulit. Inhalasinya menyebabkan iritasi hidung dan tenggorokan. Itu mempengaruhi paru -paru, menyebabkan pemendekan, bronkitis, pneumonia dan asma.
Konsumsinya mempengaruhi saluran pencernaan, hati, ginjal, sistem saraf pusat, menghasilkan keruntuhan peredaran darah dan merusak sistem kekebalan tubuh.
Generator kanker
Ini adalah karsinogen yang dikonfirmasi, meningkatkan risiko kanker paru dan rongga hidung. Ini beracun bagi sel (sitotoksik) dan juga merusak kromosom (genotoksik).
 Seng Chromate menghasilkan kanker paru -paru dan saluran udara. Penulis: OpenClipart-Vektor. Sumber: Pixabay.
Seng Chromate menghasilkan kanker paru -paru dan saluran udara. Penulis: OpenClipart-Vektor. Sumber: Pixabay. Telah ditentukan bahwa toksisitas dan karsinogenisitas senyawa ini terutama disebabkan oleh aksi krom dalam oksidasi +6. Namun, keberadaan cinc memberikan kelilin pada produk dan ini juga mempengaruhi kerusakan yang dihasilkannya.
Efek pada lingkungan
Ini sangat beracun bagi hewan dan untuk kehidupan akuatik, menyebabkan efek berbahaya yang bertahan dari waktu ke waktu. Ahli kimia ini bisa bioakumulasi di seluruh rantai makanan.
Untuk semua alasan ini, proses yang melibatkan kromat (hexavalent chrome) sedang diatur oleh organisasi kesehatan dunia dan digantikan oleh teknik alternatif tanpa ion ini.
Referensi
- ATAU.S. Perpustakaan Kedokteran Nasional. (2019). Seng Chromate. Pulih dari pubchem.NCBI.Nlm.Nih.Pemerintah.
- Timah, d.R. (Editor) (2003). Buku Pegangan Kimia dan Fisika CRC. 85th CRC Press.
- Xie, h. et al. (2009). Seng Chromate Induts Ketidakstabilan Kromosom dan DNA Doble Strad Break dalam Sel Lun Manusia. Toxicol Appl Pharmacol 2009 1 Feb; 234 (3): 293-299. NCBI pulih.Nlm.Nih.Pemerintah.
- Jackson, r.KE. et al. (1991). Aktivitas katalitik dan struktur cacat kromat seng. CATAL LETT 8, 385-389 (1991). Tautan pulih.Peloncat.com.
- Yahalom, J. (2001). Metode perlindungan korosi. Dalam Encyclopedia of Material: Sains dan Teknologi. Pulih dari scientedirect.com.
- Stranger-Johannessen, m. (1988). Efek antimikroba dari pigmen dalam cat pelindung korosi. Di Houchton d.R., Eggins, h.SALAH SATU.W. (eds) Biodeteriasi 7. Tautan pulih.Peloncat.com.
- Barrett, a.G.M. (1991). Pengurangan. Dalam memahami sintesis organik. Pulih dari scientedirect.com.
- Kamon, h.W. et al. (1948). Kromat sebagai fungisida kentang. American Potato Journal 25, 406-409 (1948). Tautan pulih.Peloncat.com.
- Lynch, r.F. (2001). Seng: Paduan, Pemrosesan Termokimia, Properti, dan Aplikasi. Dalam Encyclopedia of Material: Sains dan Teknologi. Pulih dari scientedirect.com.
- Ramesh Kumar, a.V. dan nigam, r.K. (1998). Studi spektroskopi mössbauer dari produk korosi di bawah lapisan pertama yang mengandung pigmen anti korosi. J Radianal Nucl Chem 227, 3-7 (1998). Tautan pulih.Peloncat.com.
- Otero, v. et al. (2017). Barium, seng, dan kuning stontium di lukisan minyak abad ke-19 akhir abad ke-19. Herit Sci 5, 46 (2017). Pulih dari HeritageencienceJournal.Springeropen.com.
- Kapas, f. Albert dan Wilkinson, Geoffrey. (1980). Kimia anorganik canggih. Edisi keempat. John Wiley & Sons.
- Wikipedia (2020). Seng Chromate. Diterima dari.Wikipedia.org.
- Wikipedia (2020). Lapisan konversi kromat. Diterima dari.Wikipedia.org.
- « Sabuk Kebakaran Pasifik, Karakteristik, Gunung Berapi Utama
- Struktur seng klorida (zncl2), properti, memperoleh, penggunaan »

