Diphenylamine
- 1160
- 261
- Domingo Gutkowski
Apa defilaminnya?
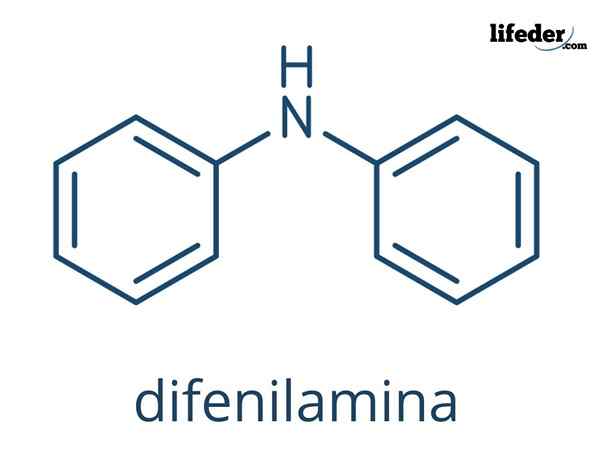
Itu Diphenylamine Itu adalah senyawa organik yang formula kimianya (c6H5)2NH. Namanya menunjukkan bahwa itu adalah amina, serta formulanya (-nh2). Di sisi lain, istilah "diffenil" mengacu pada keberadaan dua cincin aromatik yang terkait dengan nitrogen. Akibatnya, defilamin adalah amina aromatik.
Di dalam dunia senyawa organik, kata aromatik tidak selalu terkait dengan keberadaan baunya, tetapi dengan karakteristik yang menentukan perilaku kimianya terhadap spesies tertentu.
Dalam kasus difenilamin, aromatiknya dan fakta bahwa padatan mereka menyajikan aroma yang khas bertepatan. Namun, fondasi atau mekanisme yang mengatur reaksi kimianya dapat dijelaskan oleh karakter aromatiknya, tetapi bukan karena aromanya yang menyenangkan.
Struktur kimianya, kebencian, aromatik, dan interaksi antar molekul adalah variabel yang bertanggung jawab atas sifat -sifatnya: dari warna kristal hingga penerapannya sebagai agen antioksidan.
Struktur kimia defilamin

Dalam gambar superior, struktur kimia difenilamin diwakili. Bola hitam sesuai dengan atom karbon, atom putih hingga hidrogen dan biru ke atom nitrogen.
Perbedaan antara kedua gambar adalah model bagaimana mereka mewakili molekul secara grafis. Di bagian bawah itu menyoroti aromatik cincin dengan garis -garis yang dihiasi hitam dan, juga, geometri datar cincin ini dibuktikan.
Tak satu pun dari dua gambar yang menunjukkan pasangan elektron soliter yang tidak dibagikan pada atom nitrogen. Elektron ini "berjalan" melalui sistem π terkonjugasi dari ikatan rangkap dalam cincin. Sistem ini membentuk semacam awan yang bersirkulasi yang memungkinkan interaksi antar molekul; yaitu, dengan cincin lain dari molekul lain.
Itu dapat melayani Anda: termometer laboratorium: karakteristik, untuk apa, penggunaan, contohDi atas berarti bahwa torsi nitrogen non -shared berjalan melalui kedua cincin, mendistribusikan kepadatan elektroniknya, dan kemudian mereka kembali ke nitrogen, untuk mengulangi siklus lagi.
Dalam proses ini, ketersediaan elektron ini berkurang, menghasilkan penurunan kebesaran dipelamin (kecenderungannya untuk menyumbangkan elektron sebagai basis Lewis).
Penggunaan/Aplikasi Dipenylamine
Diphenylamine adalah agen pengoksidasi yang mampu memenuhi serangkaian fungsi, dan di antaranya adalah sebagai berikut:
- Selama penyimpanannya, apel dan pir mengalami proses fisiologis yang disebut Scatding, terkait dengan produksi trieno terkonjugasi, yang menyebabkan kerusakan kulit buah -buahan. Tindakan Dipenylamine memungkinkan untuk meningkatkan periode penyimpanan, mengurangi kerusakan buah menjadi 10 % dari apa yang diamati dalam ketidakhadiran mereka.
- Saat melawan oksidasi, difenilamin dan turunannya memperluas fungsi mesin dengan menghindari penebalan minyak bekas.
- Diphenylamine digunakan untuk membatasi aksi ozon di manufaktur karet.
- Diphenylamine digunakan dalam kimia analitik untuk deteksi nitrat (NO3-), Klorat (clo3-) dan agen pengoksidasi lainnya.
- Ini adalah indikator yang digunakan dalam tes deteksi keracunan nitrat.
- Ketika RNA dihidrolisis selama satu jam, ia bereaksi dengan defilamin; Ini memungkinkan kuantifikasi.
- Dalam Kedokteran Hewan, Dipe -pilamin digunakan secara topikal dalam pencegahan dan pengobatan manifestasi cacing borerida pada hewan pengembangbiakan.
- Beberapa turunan duelamin termasuk dalam kategori obat antiinflamasi non-steroid. Mereka juga dapat memiliki efek farmakologis dan terapeutik seperti antimikroba, analgesik, antikonvulsan dan aktivitas anti -kanker.
Persiapan Dipenylamine
Secara alami, defilamin diproduksi di bawang, di ketumbar, di daun teh hijau dan hitam, dan di cangkang buah jeruk jeruk. Secara sintetis, ada banyak rute yang mengarah pada senyawa ini, seperti:
Deaminasi termal anilin
Disiapkan dengan deaminasi termal anilin (c6H5NH2) Di hadapan katalis pengoksidasi.
Jika anilin dalam reaksi ini tidak menggabungkan atom oksigen ke strukturnya, mengapa Anda mengoksidasi? Karena cincin aromatik adalah kelompok penarik elektron, tidak seperti atom H, yang menyumbangkan kepadatan nitrogen elektroniknya yang rendah dalam molekul.
2 c6H5NH2 => (C5H5)2 NH+NH3
Juga, anilin dapat bereaksi dengan garam anilin hidroklorida (c6H5NH3+Cl-) di bawah pemanasan 230 ºC selama dua puluh jam.
C6H5NH2 + C6H5NH3+Cl- => (C5H5)2 NH
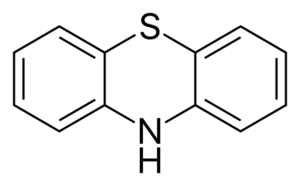
Reaksi fenotiazin
Dipenylamine berasal dari beberapa turunan saat dikombinasikan dengan reagen yang berbeda. Salah satunya adalah fenotiazin, yang, disintesis dengan sulfur adalah prekursor turunan dengan tindakan farmasi.
(C6H5)2Nh +2s => s (c6H4) Nh +h2S

Sifat Dipenylamine
Dipenylamine adalah padatan kristal putih yang, tergantung pada kotorannya, dapat memperoleh nada bronchneal, kuning atau kuning. Ini memiliki aroma bunga yang menyenangkan, memiliki berat molekul 169,23 g/mol dan kepadatan 1,2 g/ml.
Molekul-molekul dari padatan ini berinteraksi dengan gaya van der Waals, di antaranya adalah jembatan hidrogen yang dibentuk oleh atom nitrogen (NH-NH) dan susun cincin aromatik, mengistirahatkan "awan elektronik" mereka satu di sisi lain.
Dapat melayani Anda: seng sulfida (Zns)Saat cincin aromatik banyak menempati. Di atas menyebabkan padatan tidak memiliki titik fusi yang sangat tinggi (53 ºC).
Namun, dalam keadaan cair molekul lebih terpisah dan efektivitas jembatan hidrogen meningkat. Demikian juga, defilamin relatif berat, membutuhkan banyak panas untuk bergerak ke fase gas (302 ºC, titik didihnya). Ini juga sebagian karena berat dan interaksi cincin aromatik.
Kelarutan dan kebasa
Sangat tidak larut dalam air (0,03 g/100 g air) karena karakter hidrofobik dari cincin aromatiknya. Sebaliknya, sangat larut dalam pelarut organik seperti benzena, karbon tetraklorida (CCL4), aseton, etanol, piridin, asam asetat, dll.
Konstanta Keasamannya (PKA) adalah 0,79, yang mengacu pada keasaman asam terkonjugasinya (c6H5NH3+). Proton yang ditambahkan ke nitrogen memiliki kecenderungan untuk berpisah, karena sepasang elektron yang terkait dapat berjalan melalui cincin aromatik. Dengan demikian, ketidakstabilan tinggi c6H5NH3+ Itu mencerminkan kebesaran rendah difenilamin.
Referensi
- Lubrizol Corporation. (2018). Antioksidan difenilamin. Pulih dari lubrizol.com
- Arun Kumar Mishra, Arvind Kumar. (2017). Aplikasi Farmakologis Diphenylamine dan turunannya sebagai senyawa bioaktif yang kuat: ulasan. Senyawa bioaktif saat ini, volume 13.
- Prapchem. (2015-2016). Persiapan difenilamin. Pulih dari prepchem.com
- Pubchem. (2018). Diphenylamine. Pulih dari pubchem.NCBI.Nlm.Nih.Pemerintah.
- Wikipedia. (2018). Diphenylamine. Diterima dari.Wikipedia.org

