Strontium chloride (SRCL2)
- 4311
- 962
- Irvin Reichel
Apa itu strontium chloride?
Dia Strontium klorida Ini adalah senyawa anorganik yang dibentuk oleh strontium, logam alkalinoterreo (SR. Becamgbara) dan klorin halogen. Karena kedua elemen memiliki elektronegativitas yang sangat berbeda, senyawa ini adalah padatan ionik yang formula kimianya SRCL2.
Seperti halnya padatan ionik, terdiri dari ion. Dalam kasus SRCL2, Mereka adalah kation SR2+ Untuk setiap dua anion cl-. Sifat dan aplikasinya mirip dengan kalsium dan barium klorida.
Seperti kalsium klorida (CACL2), adalah higroskopis dan kristalnya menyerap air untuk membentuk garam heksahidrat, di mana enam molekul air hadir dalam kisi kristal (SRCL2· 6h2SALAH SATU). Faktanya, ketersediaan hidrat lebih besar dari SRCL2 anhidrat (tanpa air).
Salah satu aplikasi utamanya adalah sebagai pendahulu dari senyawa strontium lainnya; yaitu, itu merupakan sumber strontium dalam sintesis kimia tertentu.
Struktur kimia strontium klorida
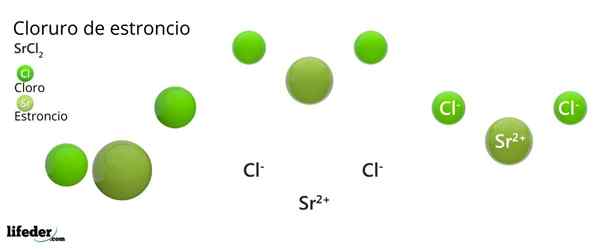
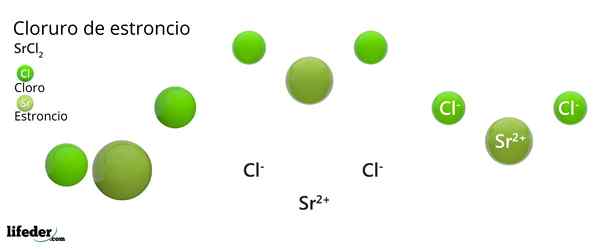
 Struktur kristal strontium klorida
Struktur kristal strontium klorida Gambar superior mewakili jenis struktur kristal yang dideformasi SRCL2 Anhidrat. Dalam hal ini, bidang hijau kecil sesuai dengan ion SR2+, Sedangkan bidang hijau tebal mewakili ion CL-.
Dalam struktur ini setiap ion SR2+ Itu "dipenjara" oleh delapan cl ion-, Akibatnya memiliki angka koordinasi sama dengan 8 dan, mungkin, geometri kubik di sekitarnya. Yaitu, empat bola hijau membuat atap kubus, sedangkan yang lainnya empat lantai, terletak SR2+ Di tengahnya.
Apa yang akan menjadi struktur fase soda? Struktur Lewis untuk garam ini adalah CL-SR-CL, tampaknya linier dan dengan asumsi seratus persen dari tautannya. Namun, dalam fase gas -srcl2(g)- "Garis" ini menunjukkan sudut sekitar 130 °, sebenarnya menjadi semacam V.
Dapat melayani Anda: Gaseous State: Karakteristik, Hukum Umum, ContohAnomali ini tidak dapat dijelaskan dengan sukses, mengingat fakta bahwa Strontium tidak memiliki elektron yang sama yang menempati volume elektronik. Mungkin itu bisa disebabkan oleh partisipasi orbital D dalam tautan, atau gangguan inti-elektron.
Penggunaan/Aplikasi Strontium Chloride
SRCL2· 6h2Atau telah digunakan sebagai aditif dalam polimer organik; Misalnya, dalam alkohol polivinil, untuk memodifikasi sifat mekanik dan listriknya.
Ini digunakan sebagai strontium ferit dalam pembuatan magnet keramik dan kaca yang ditakdirkan untuk membuat kristal depan televisi.
Bereaksi dengan natrium kromat (na2CRO4) untuk menghasilkan strontium chromate (srcro4), yang digunakan sebagai cat tahan korosi untuk aluminium.
Ketika mereka dipanaskan dengan api, senyawa strontium bersinar dengan api kemerahan, itulah sebabnya mereka ditakdirkan untuk elaborasi suar dan kembang api.
Aplikasi obat
Radioisotop Strontium Chloride 89 (isotop yang paling berlimpah adalah 85Tn.
Penggunaan larutan encer (3-5 %) selama lebih dari dua minggu dalam pengobatan rinitis alergi (peradangan kronis mukosa hidung), menunjukkan peningkatan penurunan bersin dan menggosok hidung.
Setelah digunakan dalam formulasi pasta denifrik untuk mengurangi sensitivitas gigi, membentuk penghalang pada mikrotubulus dentinal.
Studi senyawa ini menunjukkan kemanjuran terapeutik dibandingkan dengan prednisolon (metabolit obat prednison) dalam pengobatan kolitis ulserativa.
Itu dapat melayani Anda: fraksi molar: bagaimana itu dihitung, contoh, latihanHasilnya didasarkan pada model tikus; Meski begitu, itu mewakili harapan bagi pasien yang juga menderita osteoporosis, karena mereka dapat pergi ke obat yang sama untuk memerangi kedua penyakit tersebut.
Ini digunakan untuk mensintesis strontium sulfat (SRSO4), bahkan lebih padat daripada SRCL2. Namun, kelarutan air minimumnya tidak membuatnya cukup ringan untuk diterapkan dalam radiologi, tidak seperti barium sulfat (BASO4).
Persiapan strontium klorida
Strontium klorida dapat disiapkan dengan aksi langsung asam klorida (HCl) pada logam murni, sehingga terjadi reaksi tipe redoks:
MR (S) + HCL (AC) => SRCL2(Ac) + h2(G)
Di sini, logam strontium dioksidasi dengan menyumbangkan dua elektron untuk memungkinkan pembentukan hidrogen gas.
Juga, hidroksida dan strontium karbonat (SR (OH)2 dan srco3) Bereaksi dengan asam ini dengan mensintesisnya:
Sr (oh)2(s) + 2hcl (ac) => srcl2(Ac) + 2h2Atau (l)
Srco3(s) + 2hcl (ac) => srcl2(ac) + co2(g) + h2Atau (l)
Menerapkan teknik kristalisasi, SRCL diperoleh2· 6h2SALAH SATU. Setelah mengalami dehidrasi oleh aksi termal sampai SRCL akhirnya menghasilkan2 Anhidrat.
Sifat strontium klorida
Sifat fisik dan kimia dari senyawa ini tergantung pada apakah itu dalam bentuk terhidrasi atau anhidratnya. Ini karena interaksi elektrostatik berubah karena molekul air ditambahkan ke kisi kristal SRCL2.
Anhidrat
Strontium klorida adalah padatan kristal putih, dengan berat molekul 158,53 g/mol, dan kepadatan 3,05 g/ml.
Titik lelehnya (874 ºC) dan mendidih (1250 ºC) tinggi, menunjukkan interaksi elektrostatik yang kuat antara ion SR2+ dan Cl-. Itu juga mencerminkan energi retikular kristal besar yang dimiliki struktur anhidratnya.
Dapat melayani Anda: selulosa asetatSRCL Formasi Entalpi2 padatan adalah 828,85 kJ/mol. Ini mengacu pada energi termal yang dilepaskan oleh setiap tahi lalat yang terbentuk dari komponennya di keadaan standarnya: klorin dan gas padat untuk strontium.
Hexahidrat
Dalam bentuk heksahidrat memiliki berat molekul yang lebih tinggi daripada bentuk anhidrat (267 g/mol), dan kepadatan yang lebih rendah (1,96 g/ml). Penurunan kepadatannya ini disebabkan oleh fakta bahwa molekul air "melebarkan" kristal, meningkatkan volume; Oleh karena itu, kepadatan struktur berkurang.
Hampir dua kali padat dari air pada suhu kamar. Kelarutan airnya sangat tinggi, tetapi dalam etanolnya sedikit larut. Ini karena karakter organiknya terlepas dari polaritasnya. Yaitu, heksahidrat adalah senyawa kutub anorganik. Akhirnya, pada 150 ºC menjadi dehidrasi untuk menghasilkan garam anhidrat:
Srcl2· 6h2Atau (s) => srcl2(S) + 6H2O (g)
Referensi
- Wikipedia. (2018). Strontium klorida. Diterima dari.Wikipedia.org
- CHANKBANK. (2018). Strontium chloride SR-89. Bank Drug pulih.Ac
- Pubchem. (2018). Strontium klorida. Pulih dari pubchem.NCBI.Nlm.Nih.Pemerintah
- Banteng. Mater. (2010). Pengaruh stontium granular klorida sebagai aditif pada sifat listrik dan mekanik submary untuk alkohol polivinil murni. Sci., Vol. 33, tidak. 2, hlm. 149-155. Akademi Ilmu Pengetahuan India.
- Ccoil. (4 September 2009). Stontium-chloride -tal-3d-sf. [Angka]. Diperoleh pada 13 April 2018, dari: Commons.Wikimedia.org
- Semua reaksi. SRCL2 - Stontium Chloride. Pulih dari allreactions.com