Struktur klorin dioksida (CLO2), penggunaan, memperoleh, risiko, sifat

- 2042
- 19
- Joseph Nader PhD
Dia klorin dioksida Ini adalah senyawa anorganik yang dibentuk oleh elemen klorin (CL) dan oksigen (O). Formula kimianya adalah CLO2. Itu adalah gas kuning kehijauan hingga kemerahan. Itu tidak ditemukan secara alami di lingkungan.
Ini sangat reaktif, jadi umum untuk dipersiapkan di tempat di mana ia akan digunakan. Salah satu kegunaannya yang paling penting adalah sebagai mikrobisida, antiseptik dan deodorisasi karena menghilangkan bakteri, virus, dan jamur dengan sangat mudah dan dalam konsentrasi yang sangat rendah.
 Beberapa makanan yang dijual di supermarket mungkin didisinfeksi dengan clo klorin dioksida2. Penulis: ElasticComputEfarm. Sumber: Pixabay.
Beberapa makanan yang dijual di supermarket mungkin didisinfeksi dengan clo klorin dioksida2. Penulis: ElasticComputEfarm. Sumber: Pixabay. Ini memungkinkan untuk mendisinfeksi makanan seperti sayuran, buah -buahan, daging, burung dan makanan laut. Ini berfungsi untuk menghapus permukaan, lantai, kamar mandi, sistem ventilasi, kolam renang, peralatan laboratorium, peralatan dokter gigi, dll.
Oleh karena itu, digunakan dalam pengolahan makanan, di rumah sakit dan klinik, di industri dan toko. Ini digunakan untuk memurnikan air yang digunakan untuk minum dan juga air limbah kota.
Ini sangat efektif sebagai zat pengoksidasi, sehingga digunakan untuk memutihkan bubur kertas, minyak, tepung, kulit, serat tekstil, antara lain.
Ketika itu dalam bentuk gas itu sangat berbahaya, karena sangat eksplosif, dan terutama digunakan dalam larutan air. Itu beracun jika menghirup.
[TOC]
Struktur
Klorin dioksida dibentuk oleh penyatuan atom klorin (CL) dengan dua atom oksigen (O). Tautan klorin dengan masing -masing oksigen adalah kovalen dan ganda. Klorin dalam senyawa ini memiliki valensi +4.
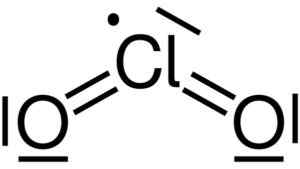 Lewis Struktur klorin dioksida2. Yikrazuul [domain publik]. Sumber: Wikimedia Commons.
Lewis Struktur klorin dioksida2. Yikrazuul [domain publik]. Sumber: Wikimedia Commons. Ini memiliki struktur berbentuk simetris dan sudut, karena memiliki elektron gratis. Yaitu, mereka tidak membentuk tautan dengan atom lainnya.
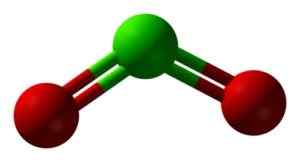 Struktur CLO2 dalam tiga dimensi. Hijau = klorin; Merah = oksigen. Ben Mills dan Jynto [domain publik]. Sumber: Wikimedia Commons.
Struktur CLO2 dalam tiga dimensi. Hijau = klorin; Merah = oksigen. Ben Mills dan Jynto [domain publik]. Sumber: Wikimedia Commons. Tata nama
- Klorin dioksida
- Klorin oksida (iv)
Properti
Keadaan fisik
Gas kuning kuning ke kemerahan.
Berat molekul
67.45 g/mol.
Titik lebur
-59 ºC.
Titik didih
11 ºC.
Kepadatan
Cairan pada 0 ° C = 1.642 g/cm3
Gas = 2.33 (kepadatan relatif udara, udara = 1).
Itu dapat melayani Anda: isoamyl alkohol: struktur, sifat, penggunaan dan risikoKelarutan
Soluble Air: 2000 cm3 dari clo2 gas pada 100 cm3 air dingin atau 0,8 g/100 ml air pada 20 ° C. Larut dalam larutan alkali dan dalam larutan asam sulfat h2Sw4.
Sifat kimia
Clo2 Itu sangat reaktif dan dapat dieksploitasi dengan keras. Ini adalah agen pengoksidasi yang sangat efektif.
Clo2 Itu pecah jika bersentuhan dengan bahan organik. Jika Anda berada di udara pada konsentrasi yang lebih besar dari 10%, ia dapat meledak karena sinar matahari atau panas.
Anda juga dapat meledak di hadapan merkuri (Hg) atau karbon monoksida (CO).
Di bawah aksi ultraviolet (UV) atau ozon CLO2 Itu menjadi klorin heksoksida2SALAH SATU6, senyawa yang sangat tidak stabil.
Sifat dari solusi air Anda
Solusi berairnya berwarna kuning atau kuning kemerahan. Mereka stabil jika mereka tetap dingin, tertutup rapat dan terlindungi dari sinar matahari. Di hadapan cahaya, larutan ini perlahan -lahan dipecah untuk memberikan asam klorida HCl dan asam klorat HClo3.
 Larutan air CLO2 di mana diamati bahwa gas kuning dilepaskan yaitu clo2. Penulis: MaterialScientist. Sumber: Wikimedia Commons.
Larutan air CLO2 di mana diamati bahwa gas kuning dilepaskan yaitu clo2. Penulis: MaterialScientist. Sumber: Wikimedia Commons. Dalam solusi alkali CLO2 Itu dipecah menjadi ion klorit clo2- dan clorate3-. Dalam larutan asam, asam kloro membentuk hclo2 Dan kemudian ini dipecah menjadi asam klorida HCl dan asam klorat HCLO3.
Properti lainnya
Uap CLO yang terkonsentrasi2 Mereka berpotensi eksplosif, jadi tidak mungkin untuk memampatkan tidak hanya dicampur dengan gas lain. Karena alasan ini lebih disukai untuk menyiapkannya di situs tempat itu akan digunakan.
Ketika suhu yang sangat rendah dalam bentuk terhidrasi, yang merupakan cara yang kadang -kadang ditransfer, itu adalah padatan dalam bentuk blok seperti es dan oranye.
Itu memiliki bau yang mirip dengan klorin. Beracun dengan inhalasi.
Memperoleh
Dapat diperoleh dalam beberapa cara. Misalnya, dalam beberapa kasus solusi CLO2 Mereka bersiap untuk melewati campuran gas klorin (CL2) dan udara (atau gas klorin dan nitrogen2) melalui kolom yang mengandung butiran natrium klorit (NaClo2).
Dapat melayani Anda: Lapisan Valencia2 Naclo2 + Cl2 → 2 NaCl + 2 CLO2
Produk yang dihasilkan mengandung sekitar 90% CLO2, Di antara senyawa klorin lainnya.
Ini juga diperoleh dari kalium klorat (KCLO3) dan asam sulfat (h2Sw4) Dengan adanya asam oksalat sebagai peredam. Dalam hal ini, karbon dioksida juga terbentuk (CO2) Itu berfungsi untuk mencairkan clo2.
Ini dapat disiapkan di lokasi penggunaan berdasarkan natrium klorat (NaClo3), asam sulfat (h2Sw4) dan metanol (pilih3OH).
Di industri ini diperoleh dengan natrium klorat (NaClo3) dan sulfur dioksida (jadi2) Di hadapan asam sulfat.
2 Naclo3 + Sw2 + H2Sw4 → 2 clo2 + 2 nahso4
Penggunaan sebagai desinfektan
Ini dapat digunakan sebagai agen antimikroba yang kuat. Telah ditemukan bahwa itu sangat efektif melawan beberapa mikroorganisme, seperti Escherichia coli dan Staphylococcus aureus.
Dengan yang terakhir, konsentrasi hanya 5 ppm clo2 untuk menghilangkan 100% dari mereka. Ini adalah bakterisidal, antiseptik dan deodorisasi. Itu efektif pada interval pH yang luas.
Dalam makanan
Ini digunakan sebagai zat antimikroba dalam air untuk fumigasi buah dan sayuran, dalam pemrosesan burung burung, daging merah, baik daging dan organ, dan produk laut dan makanan laut makanan laut.
 Daging merah supermarket mungkin telah diobati dengan klorin dioksida untuk mendisinfeksi mereka. Penulis: Karamo. Sumber: Pixabay.
Daging merah supermarket mungkin telah diobati dengan klorin dioksida untuk mendisinfeksi mereka. Penulis: Karamo. Sumber: Pixabay. Larutan klorin dioksida harus digunakan dalam konsentrasi yang tidak melebihi 3 ppm (pihak per juta) dari CLO2 residual, sehingga tidak memiliki efek pada makanan.
Setelah perawatan dengan CLO2 Semua makanan harus diperintah sepenuhnya dengan air minum, atau harus digunakan sebagai siram, memasak atau dikalengkan.
Dalam hal produk laut larutan selokan2 Itu harus digunakan di air dan es yang digunakan dalam bilas, mencuci, mencairkan, transportasi atau penyimpanan. Makanan laut mentah kemudian harus dicuci dengan sangat baik dengan air minum sebelum dikonsumsi.
 Air dingin dan es dengan buah laut yang mengandung sejumlah kecil clo2. Penulis: Domain Publik Publik. Sumber: Pixabay.
Air dingin dan es dengan buah laut yang mengandung sejumlah kecil clo2. Penulis: Domain Publik Publik. Sumber: Pixabay. Di atas kertas dan kardus yang akan bersentuhan dengan makanan
Solusi CLO2 Mereka digunakan untuk menghilangkan mikroorganisme yang menyebabkan ramping (seperti ganggang, bakteri dan jamur) dalam proses air yang digunakan dalam pembuatan kertas dan kardus yang akan bersentuhan dengan makanan.
Dapat melayani Anda: molekul apolarDi air minum
Itu berfungsi untuk memurnikan air dan membuatnya bisa diminum (aman untuk diminum). Ini digunakan dalam pretreatment air yang kemudian akan dibotolkan untuk minum atau air yang akan digunakan sebagai bahan dalam pembuatan minuman atau minuman ringan.
 Beberapa minuman ringan olahan dapat berisi air yang diolah dengan CLO2. Susan Slater [CC BY-SA (https: // CreationCommons.Org/lisensi/by-sa/4.0)]. Sumber: Wikimedia Commons.
Beberapa minuman ringan olahan dapat berisi air yang diolah dengan CLO2. Susan Slater [CC BY-SA (https: // CreationCommons.Org/lisensi/by-sa/4.0)]. Sumber: Wikimedia Commons. Dalam kedokteran gigi
Itu digunakan dalam instrumen yang digunakan oleh dokter gigi atau dokter gigi untuk mendisinfeksi mereka dan menghancurkan organisme patogen di dalamnya.
Dalam aplikasi medis
Solusi CLO yang berair2 Mereka telah digunakan untuk mengobati kandidiasis oral (infeksi mulut). Candidiasis adalah infeksi jamur Candida albicans.
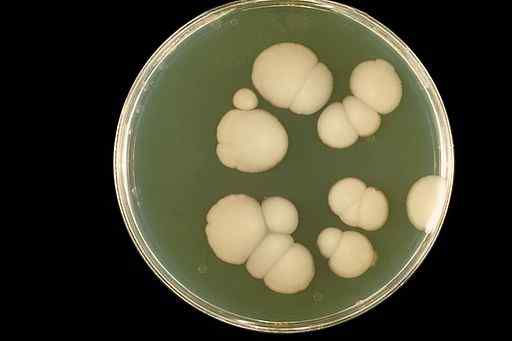 Penampilan jamur Candida albicans di tanaman laboratorium. CDC/DR. William Kaplan [domain publik]. Sumber: Wikimedia Commons.
Penampilan jamur Candida albicans di tanaman laboratorium. CDC/DR. William Kaplan [domain publik]. Sumber: Wikimedia Commons. Klorin dioksida menghilangkan mulut dari mulut dan secara signifikan meningkatkan penampilan jaringan oral tanpa efek samping.
Beberapa peneliti medis menunjukkan bahwa solusi clo2 Diterapkan pada luka operasi bedah, mereka dapat mengurangi atau menekan pembentukan aksesi tanpa mempengaruhi penyembuhan yang sama, dengan keuntungan tambahan dari sifat antiseptiknya.
Penggunaan lainnya
Untuk sifat pengoksidasi dan mikrobisida2 digunakan untuk:
- Pemutihkan selulosa kayu dalam pembuatan pulpa dan kertas, memberikan kilau yang stabil.
- Hiasi lemak dan minyak, kulit, tepung putih dan tekstil.
- Aplikasi pertanian seperti mendisinfeksi permukaan keras, peralatan, sistem air dan rumah kaca jamur.
- Aplikasi di industri, toko dan rumah sakit seperti mendisinfeksi permukaan keras (dinding, lantai, kamar mandi), sistem ventilasi, peralatan laboratorium.
- Disinfeksi Flat dan Kamar Mandi Rumah Tangga, Sistem Pendingin Udara, Sistem Sirkulasi Air Berenang.
- Pengolahan air limbah kota dan industri.
- Pembersihan polusi ladang minyak.
- Pembuatan garam klorida (CL-).
Risiko
- Uap CLO yang terkonsentrasi2 Mereka berpotensi meledak.
- Itu beracun dengan inhalasi dan konsumsi. Ini adalah mata, hidung, dan tenggorokan yang menjengkelkan, dapat menyebabkan edema paru dan bronkitis kronis.
- Menurut sumber yang berkonsultasi dengan CLO2 tidak menyebabkan mutasi DNA atau menyebabkan kanker pada manusia.
Referensi
- ATAU.S. Perpustakaan Kedokteran Nasional. (2019). Klorin dioksida. Pulih dari pubchem.NCBI.Nlm.Nih.Pemerintah.
- Dean, J.KE. (editor). (1973). Buku Pegangan Kimia Lange (Edisi Kesebelas). Perusahaan Buku McGraw-Hill.
- Ensiklopedia Kimia Industri Ullmann. (1990). Edisi Kelima. Vch verlagsgellschaft mbh.
- Kapas, f. Albert dan Wilkinson, Geoffrey. (1980). Kimia anorganik canggih. Edisi keempat. John Wiley & Sons.
- Bajpai, hlm. (2012). Pemutih klorin dioksida. Efek pemutihan klorin dioksida pada kualitas pulp. Dalam pendekatan lingkungan jinak untuk pemutihan pulp (edisi kedua). Pulih dari scientedirect.com.
- Moran, s. (2018). Kimia Air. Klorin dioksida. Dalam panduan terapan untuk desain pabrik dan pengolahan limbah. Pulih dari scientedirect.com.
- McKen, l. (2012). Pengantar foodradition dan sterilisasi medis. Gasoous Chorine Diexide. Dalam efek sterilisasi pada plastik dan elastomer (edisi ketiga). Pulih dari scientedirect.com.
- « Karakteristik Paleolitik Atas, Seni, Organisasi Sosial
- Struktur asam sulfonat, nomenklatur, sifat, penggunaan »

