Enantiomer
- 1883
- 339
- Irvin Reichel
Kami menjelaskan apa enansiomer dan chirality, sifatnya, nomenklatur dan beberapa contoh
 Dua senyawa ini adalah enansiomer, karena mereka dibentuk oleh atom yang sama, disatukan dengan cara yang sama dan merupakan gambar specular satu sama lain
Dua senyawa ini adalah enansiomer, karena mereka dibentuk oleh atom yang sama, disatukan dengan cara yang sama dan merupakan gambar specular satu sama lain Apa enansiomer?
Itu Enantiomer Mereka adalah pasangan senyawa yang merupakan gambar cermin yang tidak dapat diendapkan satu sama lain. Pasangan senyawa ini adalah jenis isomer tertentu, yaitu, mereka adalah senyawa yang berbeda yang memiliki rumus molekul yang sama.
Ada berbagai jenis isomer di antaranya adalah stereoisomer, di mana semua atom disatukan dalam urutan yang sama dan dengan jenis tautan yang sama, tetapi mereka memiliki orientasi yang berbeda dalam ruang (stereo berarti ruang).
Di dalam stereoisomer, kami menemukan enansiomer, yang karakteristik utamanya adalah menjadi gambar specular satu sama lain.
Enantiomer sangat umum. Faktanya, hampir semua senyawa organik yang ada dalam sel dari semua makhluk hidup adalah salah satu dari dua enansiomer yang mungkin.
Sebagai contoh, semua asam amino yang merupakan bagian dari protein alami sesuai dengan enansiomer L dari masing -masing asam amino (isomer lainnya mengidentifikasi dengan huruf d).
Di sisi lain, bahan aktif dari sebagian besar obat juga ada sebagai pasangan enansiomer, yang hanya satu yang efektif. Kesulitan dalam memisahkan enansiomer satu sama lain berarti bahwa obat -obatan yang hanya mengandung isomer yang berguna sangat mahal.
Enantiomer dan kiralitas
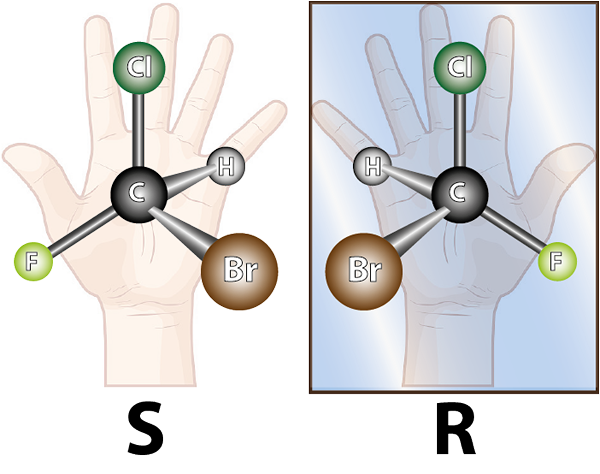
Enantiomer dibentuk oleh molekul kiral. Chirality adalah milik tidak dapat ditumpangkan dengan gambar cerminnya. Kata Chiral berasal dari istilah Yunani, Kheir yang berarti tangan, mengingat fakta bahwa tangan juga merupakan gambar specular satu sama lain, dan mereka tidak dapat tumpang tindih.
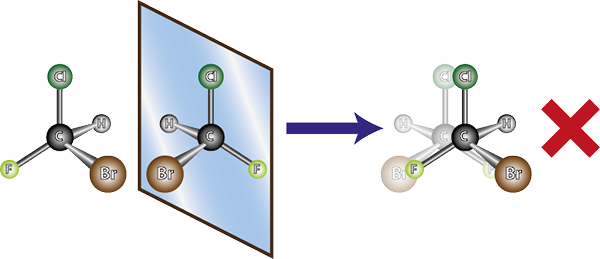 Molekul kiri adalah kiral, karena ketika membandingkannya dengan gambar cerminnya, dapat dilihat bahwa mereka tidak tumpang tindih. Dengan kata lain, tidak ada cara untuk memutar atau mengubahnya sedemikian rupa sehingga semua atom bertepatan satu sama lain
Molekul kiri adalah kiral, karena ketika membandingkannya dengan gambar cerminnya, dapat dilihat bahwa mereka tidak tumpang tindih. Dengan kata lain, tidak ada cara untuk memutar atau mengubahnya sedemikian rupa sehingga semua atom bertepatan satu sama lain Mengingat hal di atas, dapat disimpulkan bahwa untuk setiap molekul kiral, harus ada molekul kiral lain yang bukan gambar cermin yang tidak tumpang tindih, yaitu enansiomernya. Dengan kata lain, setiap kali molekul dikatakan.
Dapat melayani Anda: neodymium: struktur, sifat, penggunaanPusat kiral
Banyak senyawa kiral memiliki satu atau lebih pusat asimetris yang bertanggung jawab atas chirality molekul. Ini disebut pusat kiral dan dalam banyak senyawa organik terdiri dari atom karbon yang terkait dengan 4 atom atau kelompok atom yang berbeda.
Bentuk khusus karena keempat kelompok ini didistribusikan di sekitar karbon asimetris menentukan mana dari dua enansiomer yang sesuai dengan molekul kiral. Kehadiran pusat quiral tunggal memastikan bahwa molekulnya adalah kiral, tetapi jika ada lebih dari satu, itu mungkin kiral karena mungkin tidak.
Properti Enontiomer
Kebanyakan sifat fisik dan kimia identik
Seperti tangan kanan dan tangan kiri, enansiomer hanya datang berpasangan. Senyawa ini praktis identik satu sama lain. Faktanya, sebagian besar sifat fisik dan kimianya seperti titik fusi, mendidih, tekanan uap dan kelarutan dalam beberapa pelarut, antara lain, identik.
Aktivitas optik
Semua senyawa kiral memiliki properti unik yang membedakannya dari mereka yang tidak: mereka memiliki kemampuan untuk memutar bidang cahaya terpolarisasi. Properti ini dipanggil Aktivitas optik, Dan itu adalah salah satu dari sedikit sifat yang membedakan senyawa kiral dari enansiomernya.
Yang terakhir ini disebabkan oleh fakta bahwa bidang cahaya terpolarisasi dapat diputar di salah satu dari dua arah, baik ke arah jarum jam (disebut dextrogyr dan diwakili dengan simbol +) atau terhadap jarum jam (levógiro, diwakili dengan simbol -).
Jika senyawa quiral memutar bidang cahaya terpolarisasi dalam satu arah, enansiomernya akan memutarnya ke arah yang berlawanan.
-
Contoh
Larutan D-glukosa berputar di bidang cahaya terpolarisasi ke arah jarum jam (ke kanan, dekstrogiral), sedangkan larutan L-glikose membuatnya berputar ke arah yang berlawanan.
Itu dapat melayani Anda: Erlenmeyer Flask: Karakteristik, Penggunaan, Metode PenggunaanReaktivitas diferensial
Properti lain yang memungkinkan membedakan satu enantión dari yang lain, adalah reaktivitasnya terhadap senyawa kiral lainnya.
Reaktivitas diferensial dapat dibandingkan dengan cara sarung tangan hanya terlihat bagus di satu tangan, tetapi tidak yang lain, atau sebagai sepatu kanan cocok dengan kaki kanan, tetapi tidak ke kiri.
Konsekuensi penting dari reaktivitas diferensial adalah efek berbeda yang dapat menyebabkan dua enansiomer dari beberapa obat. Perbedaan -perbedaan ini bisa tidak berbahaya, tetapi juga bisa sangat berbahaya.
-
Contoh
- Dari dua enantimer aspartame (yang merupakan pemanis buatan), satu manis sementara yang lain tidak memiliki rasa.
- Hanya enansiomer omeprazole yang efektif sebagai pelindung lambung sementara yang lain tidak menghasilkan efek apa pun.
- D-Penicilamine adalah obat terhadap rheumatoid arthritis, sedangkan enansiomernya, L-penikilamin adalah racun yang berbahaya.
Penyerapan diferensial
Enantiomer juga berbeda dalam cara mereka diserap dalam resin atau padatan yang juga kiral. Campuran enansiomer dapat dipisahkan jika dilewatkan melalui kolom pemisahan kiral, karena salah satu dari dua enansiomer akan diserap lebih kuat daripada yang lain.
Nomenklatur enansiomer
Ada beberapa metode untuk mengidentifikasi satu atau lain enansiomer, tetapi yang paling banyak digunakan adalah sistem Cahn-ingold-prelog (CIP). Ini terdiri dari langkah -langkah berikut:
- Tingkat hierarki ditugaskan ke empat kelompok yang melekat pada setiap pusat kiral. Prioritas kelompok ditugaskan sesuai dengan nomor atom atom yang terkait langsung ke pusat quiral. Jika ada dua atom yang sama, angka atom atom yang terkait dengan yang pertama ditambahkan untuk menambahkan angka atom.
- Arah di mana tiga kelompok prioritas dilalui ketika titik prioritas terendah ditentukan.
- Jika arah rute berada di arah tangan jam, konfigurasi ditetapkan R, Kalau tidak, konfigurasi ditetapkan S.
Contoh
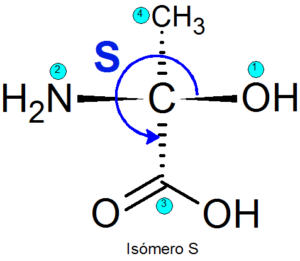
Contoh enansiomer
D-gliseraldehida dan L-gliseraldehida
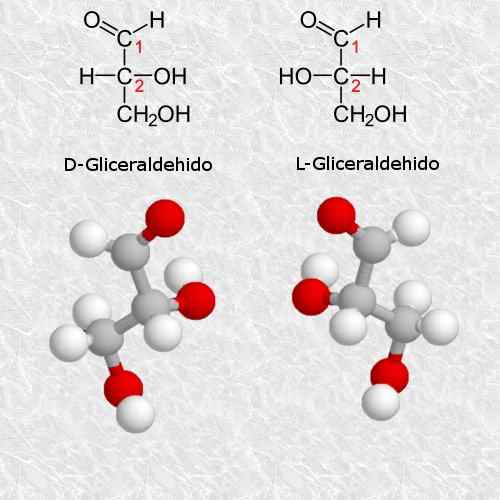
Gliseraldehida adalah karbohidrat quiral paling sederhana dan paling kecil yang ada, dan sangat penting untuk kimia dan biologi.
Menurut aturan sistem Cahn-ingold-prelog, isomer D sesuai dengan isomer (r) dan isomer L sesuai dengan (s).
D-alanina dan L-alanina
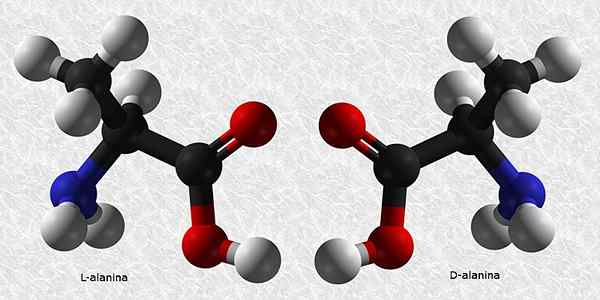
Alanine adalah salah satu asam amino esensial untuk pembangunan protein. Seperti hampir semua asam amino, ia memiliki karbon kiral sehingga memiliki dua enansiomer:
Dari keduanya, L-alanina adalah yang paling umum dan hadir di semua makhluk hidup, sedangkan D-alanina hanya ada di beberapa dinding sel bakteri.
Asam D-Tartaric dan L-Tartaric
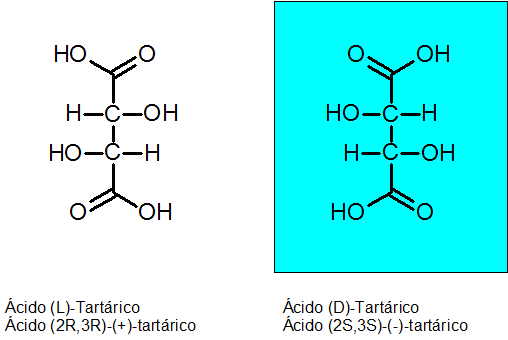
Chirality ditemukan oleh Louis Pasteur pada tahun 1848 berkat asam tartarat. Senyawa ini memiliki 2 karbon asimetris dan dapat ada sebagai dua enansiomer ditambah isomer ketiga yang disebut senyawa meso.
Konfigurasi absolut dari dua karbon kiral adalah r untuk enantiómero levógiro dan s untuk dextrogyan enantiom.
2-butanol
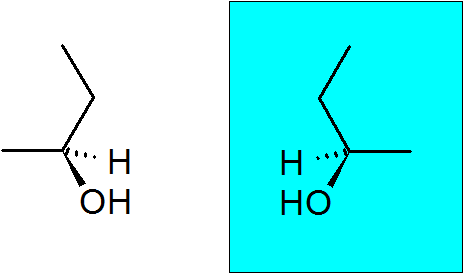
Alkohol ini juga memiliki karbon quiral, yang membuat senyawa ini memiliki dua enansiomer.
Bromocloroetan
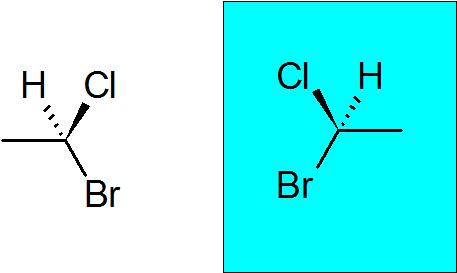
Ini adalah senyawa kiral yang sangat sederhana dengan hanya dua karbon. Karbon quiral telah bergabung dengan bromin, klorin, metil dan hidrogen.
Referensi
- Chirality (Kimia). (18 Maret 2021), di Wikipedia.com
- Carey, f. KE. (2008). Kimia organik. Boston: Pendidikan Tinggi McGraw-Hill.
- Smith, m., Maret, j., & Maret, J. (2001). Kimia Organik Lanjutan March: Reaksi, Mekanisme, dan Strupture. New York: Wiley.
- M.H. Hyun (2012). 8.13 Pemisahan dan Analisis Kromatografi: Fase Stasioner Berbasis Chiral Crown Ether. Editor: Erick M. Carreira, Hisashi Yamamoto. Memahami kiralitas. Elsevier. Halaman 263-285. ISBN 9780080951683,
- Nguyen, l. KE., Dia, h., & Pham-huy, c. (2006). Obat kiral: Tinjauan umum. Jurnal Internasional Ilmu Biomedis: IJBS, 2(2), 85-100.

