Persamaan, aplikasi, latihan keseimbangan termal

- 3751
- 708
- Joseph Nader PhD
Keseimbangan termal dari dua badan yang berada dalam kontak termal adalah keadaan yang dicapai setelah waktu yang cukup lama sehingga suhu kedua badannya sama dengan.
Dalam termodinamika, kontak termal dari dua badan (atau dua sistem termodinamika) dipahami sebagai situasi di mana tubuh memiliki kontak mekanis atau dipisahkan tetapi dalam kontak dengan permukaan yang hanya memungkinkan lorong panas dari satu tubuh ke yang lain (permukaan diheratermik ).
-
 Gambar 1. Setelah beberapa saat es dan minuman akan mencapai keseimbangan termal mereka. Sumber: Pixabay
Gambar 1. Setelah beberapa saat es dan minuman akan mencapai keseimbangan termal mereka. Sumber: Pixabay
Dalam kontak termal seharusnya tidak ada reaksi kimia antara sistem yang bersentuhan. Seharusnya hanya ada pertukaran panas.
Situasi sehari -hari di mana ada pertukaran panas disajikan dengan sistem seperti minuman dingin dan gelas, kopi panas dan sendok teh, atau tubuh dan termometer, di antara banyak contoh lainnya.
[TOC]
Saat dua atau lebih sistem berada dalam keseimbangan termal?
Hukum termodinamika kedua menetapkan bahwa panas selalu berubah dari badan suhu tertinggi ke suhu terendah. Perpindahan panas berhenti segera setelah suhu disamakan dan status keseimbangan termal tercapai.
Aplikasi praktis keseimbangan termal adalah termometer. Termometer adalah perangkat yang mengukur suhunya sendiri, tetapi berkat keseimbangan termal kita dapat mengetahui suhu benda lain, seperti orang atau hewan.
Termometer kolom merkuri ditempatkan dalam kontak termal dengan tubuh, misalnya di bawah lidah, dan cukup waktu diharapkan mencapai keseimbangan termal antara tubuh dan termometer dan bahwa pembacaannya tidak bervariasi lebih.
Saat titik ini tercapai, suhu termometer sama dengan tubuh.
Hukum nol termodinamika menetapkan bahwa jika badan A berada dalam kesetimbangan termal dengan tubuh C dan badan C yang sama berada dalam kesetimbangan termal dengan B, maka A dan B berada dalam kesetimbangan termal bahkan ketika antara A dan B tidak ada kontak termal termal.
Kami menyimpulkan bahwa dua atau lebih sistem berada dalam keseimbangan termal ketika mereka memiliki suhu yang sama.
Persamaan keseimbangan termal
Kami mengasumsikan tubuh pada suhu awal dalam kontak termal dengan tubuh B lain dengan suhu awal TB. Kami juga berasumsi bahwa ta> tb, kemudian menurut hukum kedua panas ditransfer dari A ke B.
Setelah beberapa saat keseimbangan termal akan tercapai dan kedua badan akan memiliki TF suhu akhir yang sama. Ini akan memiliki nilai menengah untuk TA dan TB, yaitu, ta> tf> tb.
Jumlah panas yang ditransfer dari A ke B akan menjadi qa = ma ca (tf - ta), di mana ma adalah massa tubuh a, ca kapasitas panas per unit massa y (tf - ta) perbedaan suhu. Jika TF kurang dari maka QA negatif, menunjukkan bahwa tubuh memberi panas.
Demikian pula untuk tubuh B Anda harus qb = mb cb (tf - tb); Dan jika TF lebih besar dari TB maka QB positif, menunjukkan bahwa tubuh B menerima panas. Karena tubuh A dan B berada dalam kontak termal di antara mereka, tetapi terisolasi dari lingkungan, jumlah total panas yang dipertukarkan harus nol: qa + qb = 0
Lalu ma ca (tf - ta) + mb cb (tf - tb) = 0
Suhu keseimbangan
Mengembangkan ekspresi ini dan membersihkan suhu TF, suhu kesetimbangan termal akhir diperoleh.
-
 Gambar 2. Suhu keseimbangan akhir. Sumber: Made sendiri
Gambar 2. Suhu keseimbangan akhir. Sumber: Made sendiri
TF = (MA CA TA + MB CB TB) / (MA CA + MB CB).
Sebagai kasus tertentu, pertimbangkan kasus bahwa badan A dan B identik dalam massa dan dalam kapasitas panas, dalam hal ini suhu keseimbangan adalah:
Tf = (ta + tb) / 2 ↔ jika ma = mb dan ca = cb.
Kontak termal dengan perubahan fase
Dalam beberapa situasi terjadi bahwa ketika dua badan ditempatkan dalam kontak termal, pertukaran panas menyebabkan perubahan keadaan atau fase di salah satunya. Jika ini terjadi, harus diperhitungkan bahwa selama perubahan fase tidak ada perubahan suhu dalam tubuh yang memodifikasi statusnya.
Jika perubahan fase salah satu badan dalam kontak termal terjadi, konsep panas laten L diterapkan, yang merupakan energi per unit massa yang diperlukan untuk perubahan keadaan:
Q = l ∙ m
Misalnya, melelehkan 1 kg es pada 0 ° C, 333,5 kJ/kg diperlukan dan nilainya adalah panas laten dari pencairan es.
Selama fusi, air padat diubah menjadi air cair, tetapi air itu mempertahankan suhu es yang sama selama proses merger.
Aplikasi
Keseimbangan termal adalah bagian dari kehidupan sehari -hari. Misalnya, mari kita periksa situasi ini secara rinci:
-Latihan 1
Seseorang ingin mandi dengan air hangat pada suhu 25 ° C. Di tempat kubus 3 liter air dingin pada suhu 15 ° C dan di dapur panas air hingga 95 ° C.
Berapa banyak liter air panas yang harus ditambahkan ke kubus air dingin untuk memiliki suhu akhir yang diinginkan?
Larutan
Misalkan itu air dingin dan air panas:
-
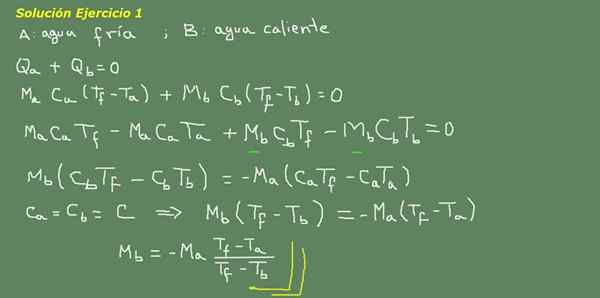 Gambar 3. Latihan 3 Solusi. Sumber: Made sendiri.
Gambar 3. Latihan 3 Solusi. Sumber: Made sendiri.
Kami mengusulkan persamaan keseimbangan termal, seperti yang ditunjukkan pada Dewan Gambar 3 dan dari sana kami membersihkan air MB.
Massa awal air dingin dapat diperoleh karena kepadatan air diketahui, yaitu 1kg untuk setiap liter. Yaitu, kami memiliki 3 kg air dingin.
MA = 3kg
Jadi
MB = - 3 kg*(25 ° C - 15 ° C)/(25 ° C - 95 ° C) = 0,43 kg
Maka cukup dengan 0,43 lts air panas untuk akhirnya mendapatkan 3,43 liter air hangat pada 25 ° C.
Latihan terpecahkan
-Latihan 2
Sepotong logam dengan massa 150 g diperkenalkan dan dengan suhu 95 ° C ke wadah yang mengandung setengah liter air pada suhu 18 ° C. Setelah beberapa saat keseimbangan termal dan suhu air dan logam tercapai adalah 25 ° C.
Misalkan wadah dengan air dan potongan logam adalah termos tertutup yang tidak memungkinkan pertukaran panas dengan lingkungan.
Dapatkan panas spesifik logam.
Larutan
Pertama kita akan menghitung panas yang diserap oleh air:
QA = MA CA (TF - TA)
Qa = 500g 1cal/(g ° C) (25 ° C - 18 ° C) = 3500 kalori.
Itu adalah panas yang sama yang diberikan oleh logam:
QM = 150g cm (25 ° C - 95 ° C) = -3500 kalori.
Kemudian kita bisa mendapatkan kapasitas panas logam:
Cm = 3500 kal/ (150g 70 ° C) = ⅓ kal/ (g ° C).
Latihan 3
Anda memiliki 250 c.C. air pada suhu 30 ° C. Ke air yang ada dalam termos isolasi, 25g es batu pada 0 ° C ditambahkan, dengan tujuan mendinginkannya.
Tentukan suhu keseimbangan; yaitu, suhu yang akan tetap ada setelah semua es meleleh dan air es telah dipanaskan sampai air yang awalnya memiliki kaca.
Solusi 3
Latihan ini dapat diselesaikan dalam tiga tahap:
- Yang pertama adalah perpaduan es yang menyerap panas dari air awal untuk meleleh dan menjadi air.
- Kemudian penurunan suhu air awal dihitung, karena telah memberikan panas (qed<0) para fundir el hielo.
- Akhirnya, air cair (dari es) harus seimbang secara termal dengan air yang awalnya ada.
-
 Gambar 4. Latihan 3 Solusi. Sumber: Made sendiri.
Gambar 4. Latihan 3 Solusi. Sumber: Made sendiri.
Mari kita menghitung panas yang diperlukan untuk perpaduan es:
Qf = l * mh = 333,5 kj/kg * 0,025kg = 8.338 kJ
Kemudian, panas yang ditetapkan oleh air untuk melelehkan es adalah qed = -qf
Panas yang ditugaskan oleh air ini menurunkan suhunya ke nilai yang dapat kita hitung sebagai berikut:
T '= T0 - qf/(ma*ca) = 22.02 ° C
Dimana ca adalah kapasitas panas air: 4,18 kJ/(kg ° C).
Akhirnya massa air asli yang sekarang pada 22,02 ° C akan menghasilkan panas ke air cair dari es yang berada pada 0 ° C.
Akhirnya, suhu keseimbangan akan tercapai setelah cukup waktu:
TE = (MA * T ' + MH * 0 ° C) / (MA + MH) = (0,25kg * 22,02 ° C + 0,025kg * 0 ° C) / (0,25kg + 0,025kg).
Akhirnya mendapatkan suhu keseimbangan:
TE = 20.02 ° C.
-Latihan 4
Sepotong timbal 0,5 kg meninggalkan oven pada suhu 150 ° C, yang cukup di bawah titik lelehnya. Bagian itu ditempatkan dalam wadah dengan 3 liter air pada suhu kamar 20 ° C. Tentukan suhu keseimbangan akhir.
Juga Hitung:
- Jumlah panas yang dikirimkan oleh air.
- Jumlah panas yang diserap oleh air.
Data:
Panas timbal spesifik: CP = 0,03 kapur/(G ° C); Panas air spesifik: Ca = 1 kapur/(G ° C).
Larutan
Di tempat pertama kami menentukan suhu keseimbangan akhir:
Te = (ma ca ta + mp cp tp) / (ma ca + mp cp)
TE = 20,65 ° C
Maka jumlah panas yang ditetapkan oleh timbal adalah:
Qp = mp cp (te - tp) = -1.94 x 10³ kapur.
Jumlah panas yang diserap oleh air adalah:
QA = MA CA (TE - TA) = +1.94x 10³ Lime.
Referensi
- Atkins, hlm. 1999. Kimia Fisik. Edisi Omega.
- Bauer, w. 2011. Fisika untuk Teknik dan Ilmu Pengetahuan. Volume 1. MC Graw Hill.
- Giancoli, d. 2006. Fisika: Prinsip dengan aplikasi. 6 ... Ed Prentice Hall.
- Hewitt, Paul. 2012. Ilmu Fisik Konseptual. Ke -5. Ed. Pearson.
- Resnick, r. (1999). Fisik. Vol. 1. Edisi ke -3. di Spanyol. Perusahaan Editorial Kontinental S.KE. dari c.V.
- Rex, a. 2011. Dasar -dasar fisika. Pearson.
- Sears, Zemansky. 2016. Fisika Universitas dengan Fisika Modern. 14. Ed. Volume 1.
- Serway, r., Jewett, J. (2008). Fisika untuk Sains dan Teknik. Volume 1. 7. Ed. Pembelajaran Cengage.
- « Karakteristik Sistem Produksi Berkelanjutan, Keuntungan, Contoh
- Penyebab Revolusi Liberal Ekuador, Pembangunan dan Konsekuensi »

