Indian

- 4189
- 1310
- Joseph Nader PhD
 Sepotong India Metalik. Sumber: Gambar Hi-Res Elemen ofchemical [CC BY (https: // CreationCommons.Org/lisensi/oleh/3.0)]
Sepotong India Metalik. Sumber: Gambar Hi-Res Elemen ofchemical [CC BY (https: // CreationCommons.Org/lisensi/oleh/3.0)] Apa itu India?
Dia Indian Ini adalah logam yang termasuk dalam kelompok 13 dari tabel periodik dan memiliki simbol kimia di. Nomor atom Anda adalah 49, 49Di, dan disajikan di alam sebagai dua isotop: 113Di dan 115Dalam, yang terakhir menjadi yang paling berlimpah. Di Bumi Atom -atom India ditemukan sebagai kotoran dalam seng dan mineral utama.
Ini adalah logam tertentu, karena ini adalah yang paling lembut yang dapat disentuh tanpa banyak risiko kesehatan; Tidak seperti lithium dan rubidium, yang akan membakar kulit dengan sangat baik saat bereaksi dengan kelembabannya. Sepotong India dapat dipotong dengan pisau dan patah tulang dengan kekuatan jari, memancarkan krisis yang khas.
Siapa pun yang mendengar logam ini pasti akan datang ke pikiran India, tetapi namanya berasal dari warna indigo, yang diamati ketika tes api dilakukan. Dalam hal ini, terlihat cukup banyak kalium, membakar logamnya atau senyawanya dengan nyala api yang sangat khas, yang melaluinya orang India terdeteksi untuk pertama kalinya dalam mineral sphenset.
India berbagi banyak kualitas kimia dengan aluminium dan gallium, menyajikan sebagian besar senyawa dengan jumlah oksidasi +3 (dalam3+). Itu menggabungkan dengan sangat baik dengan gaul membentuk paduan dengan titik leleh rendah, salah satunya menjadi Galinstan.
Aplikasi India didasarkan pada lapisan bahan dengan paduannya, menjadikannya konduktor listrik dan fleksibel. Orang India memiliki gelas untuk memberi mereka glitter yang lebih besar, menggantikan perak. Di dunia teknologi, orang India ditemukan di layar sentuh dan LCD.
Penemuan
Pada tahun 1863, ahli kimia Jerman Ferdinand Reich sedang mencari jejak elemen Talio, menggunakan garis hijau spektrum emisinya, dalam mineral Cinc; Khususnya sampel sphalerite (Zns) di sekitar Saxony. Setelah memanggang mineral, lepaskan kandungan belerangnya, mencerna mereka dalam asam klorida, dan menyaring seng klorida, memperoleh endapan pijizo.
Mengingat temuan itu, Reich memutuskan untuk melakukan analisis spektroskopi; Tetapi karena dia tidak memiliki mata yang baik untuk mengamati warnanya, dia pergi ke rekannya Hariomus Theodor Richter untuk membantunya dalam tugas ini. Richter adalah orang yang mengamati garis spektral kebiruan, yang tidak cocok dengan spektrum elemen lain.
Itu dapat melayani Anda: asam iodose (HIO2): sifat dan penggunaanDua ahli kimia Jerman menghadapi unsur baru, yang disebut warna India untuk warna nila nyala api ketika senyawa mereka terbakar; Dan pada gilirannya, nama warna ini berasal dari kata Latin Indicum, Apa arti India.
Setahun kemudian, pada tahun 1864, bersemangat dan setelah serangkaian curah hujan dan pemurnian yang berkepanjangan, mereka mengisolasi sampel India logam melalui elektrolisis garam terlarut dalam air.
Struktur India
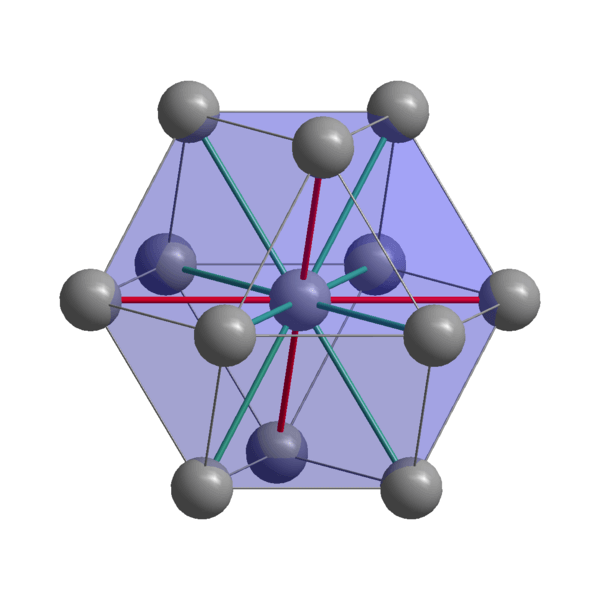 Struktur Kristal India
Struktur Kristal India India, dalam, atom kohesi menggunakan elektron valensi mereka untuk membangun ikatan logam. Dengan demikian, mereka akhirnya dipesan dalam struktur tetragonal yang terdistorsi yang berpusat pada tubuh. Interaksi antara atom-atom in-in-in-in-in-in-in-in-in-in-in-in-in-in-in-in-in-in-in-in-in-in-in-in-in-in-in-in-in-in-in-in-neighbor bersifat relatif lemah, yang menjelaskan mengapa orang India memiliki titik leleh yang rendah (156 ºC).
Di sisi lain, kekuatan yang menyatukan dua atau lebih kristal India juga tidak kuat, jika tidak mereka tidak akan bergerak di atas satu sama lain, menganugerahkan kelembutan karakteristik logam.
Properti India
Penampilan fisik
Itu adalah logam perak yang sangat lembut. Itu bisa robek dengan tekanan kuku, dipotong dengan pisau, atau menggaruk sapuan terang di selembar kertas. Bahkan dimungkinkan untuk mengunyahnya dan mengubah bentuknya dengan gigi, asalkan itu diratakan. Ini juga sangat ulet dan ditempa, memiliki sifat plastik.
Saat orang India dipanaskan dengan obor menolak nyala warna nila, bahkan lebih cerah dan lebih berwarna daripada kalium.
Masa molar
114.81 g/mol
Titik lebur
156.60 ºC
Titik didih
2072 ºC.
Seperti Gaul, orang India memiliki interval suhu yang besar antara titik fusi dan mendidih. Ini mencerminkan fakta bahwa interaksi masuk dalam cairan lebih kuat daripada yang mendominasi dalam kaca; Dan karena itu, lebih mudah untuk mendapatkan setetes India daripada uap mereka.
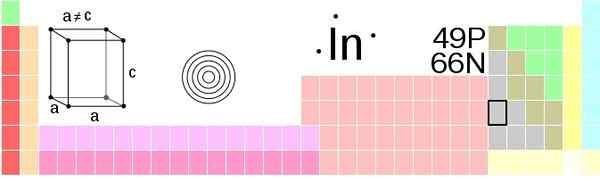 Lokasi India di tabel periodik. Sumber: Daniel Mayer atau Greatpatton Vektorisasi: Sushant Savla, CC BY-SA 3.0, via Wikimedia Commons
Lokasi India di tabel periodik. Sumber: Daniel Mayer atau Greatpatton Vektorisasi: Sushant Savla, CC BY-SA 3.0, via Wikimedia Commons Kepadatan
Pada suhu kamar: 7,31 g/cm3
Tepat di titik leleh: 7.02 g/cm3
Elektronegativitas
1.78 pada skala Pauling
Energi ionisasi
Pertama: 558.3 kJ/mol
Kedua: 1820.7 kJ/mol
Ketiga: 2704 kJ/mol
Konduktivitas termal
81.8 w/(m · k)
Resistivitas listrik
83.7 nΩ · m
Kekerasan Mohs
1.2. Ini nyaris sedikit lebih sulit daripada bedak (tidak membingungkan keuletan dengan keras).
Reaktivitas
India larut dalam asam untuk menyebabkan garam, tetapi tidak larut dalam larutan alkali, bahkan dengan kalium hidroksida panas. Bereaksi dalam kontak langsung dengan sulfur, oksigen dan halogen.
Dapat melayani Anda: pengenceran: konsep, bagaimana hal itu dilakukan, contoh, latihanOrang India relatif amfoter, tetapi berperilaku lebih sebagai dasar daripada sebagai asam, menjadi larutan airnya yang sedikit dasar. The In (oh)3 Itu dididokasikan kembali dengan penambahan lebih banyak alkali yang menyebabkan kompleks indate, di (OH)4-, seperti halnya aluminat.
Konfigurasi elektronik
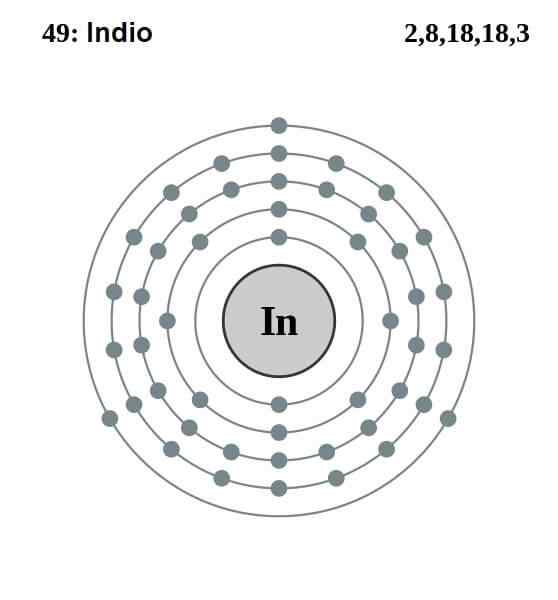 Konfigurasi India Elektronik
Konfigurasi India Elektronik Konfigurasi elektronik orang India adalah sebagai berikut:
[Kr] 4d10 5S2 5 p1
Dari tiga belas elektron itu, tiga orbital terakhir dan 5p adalah yang dari Valencia. Dengan ketiga elektron ini atom India menetapkan ikatan logamnya, seperti aluminium dan gallium, dan membentuk ikatan kovalen dengan atom lainnya.
Angka oksidasi
Di atas digunakan untuk berdiri sekaligus bahwa orang India mampu kehilangan tiga elektron Valencia, atau memenangkan lima untuk menjadi isolektronik ke xenon gas mulia.
Jika dalam senyawa kami berasumsi bahwa ia telah kehilangan tiga elektron, ia akan tetap sebagai kation trivalen3+ (Dalam analogi al3+ dan ga3+) dan, oleh karena itu, nomor oksidasi Anda adalah +3. Kebanyakan senyawa India berada di (III).
Di antara angka oksidasi lainnya yang ditemukan untuk orang India yang kami miliki: -5 (IN5-), -2 (dalam2-), -1 (dalam-), +1 (dalam+) dan +2 (dalam2+).
Beberapa contoh senyawa dalam (i) adalah: inf, incl, inbr, ini dan in in2SALAH SATU. Semuanya adalah senyawa yang relatif langka, sedangkan yang ada di (iii) adalah dominan: dalam (OH)3, Di dalam2SALAH SATU3, Termasuk3, Inf3, dll.
Dalam (i) senyawa adalah agen pereduksi yang kuat, di mana masuk+ menyumbangkan dua elektron ke spesies lain untuk masuk3+.
Isotop
Orang India disajikan di alam sebagai dua isotop: 113Di dan 115Di dalam, yang kelimpahan tanahnya masing -masing 4,28% dan 95,72%. Karena itu, di bumi kita memiliki lebih banyak atom 115Dalam hal itu 113Di dalam. Dia 115Dalam memiliki setengah kehidupan 4,41 · 1014 bertahun -tahun, sangat bagus sehingga praktis dianggap stabil, meskipun menjadi radioisotope.
Saat ini, total 37 isotop buatan India, semua radioaktif dan sangat tidak stabil telah dibuat. Dari semuanya, yang paling stabil adalah 111Di, yang memiliki setengah kehidupan 2,8 hari.
Penggunaan/Aplikasi
Paduan
Orang India rukun dengan gallium. Kedua logam membentuk paduan yang mel. Juga, orang India juga mudah digabungkan, memiliki kelarutan 57% di merkuri.
Dapat melayani Anda: asam asetat (CH3COOH)Paduan India digunakan untuk merancang cermin perak tanpa menggunakan perak. Ketika mereka dituangkan di area material apa pun, ia bertindak sebagai penganut, sehingga kaca, logam, kuarsa, dan keramik dapat dikumpulkan.
elektronik
 Tanpa India, layar sentuh tidak akan pernah ada
Tanpa India, layar sentuh tidak akan pernah ada Orang India itu juga bergaul dengan Germanio, jadi senyawanya ditambahkan sebagai doping ke nitruro Jerman dari LED, mereproduksi campuran lampu biru ini, ungu dan hijau. Ini juga bagian dari transistor, termistor dan sel fotovoltaik.
Yang paling penting dari senyawanya adalah timah dan oksida India, yang digunakan sebagai lapisan gelas untuk mencerminkan beberapa panjang gelombang. Ini memungkinkan Anda untuk digunakan dalam kacamata pengelasan, dan di kaca goresan sehingga tidak memanaskan di dalam.
Kaca yang dilapisi oksida ini adalah konduktor listrik yang baik; Seperti yang dari jari kita. Dan itulah sebabnya ditakdirkan untuk pembuatan layar sentuh, bahkan lebih banyak aktivitas saat ini karena munculnya lebih banyak dan lebih banyak smartphone.
Risiko
 India di Solid State. Sumber: w. Oelen, CC BY-SA 3.0, via Wikimedia Commons
India di Solid State. Sumber: w. Oelen, CC BY-SA 3.0, via Wikimedia Commons Orang India tidak mewakili risiko terhadap lingkungan pada contoh pertama, seperti yang ada di dalam ion -ionnya3+ Mereka tidak disebarluaskan dalam jumlah yang cukup. Tidak ada informasi mengenai apa dampaknya terhadap tanah, mempengaruhi tanaman, dan baik di fauna atau laut.
Di dalam tubuh tidak diketahui jika ion masuk3+ Mereka memiliki beberapa partisipasi penting dalam metabolisme dalam jumlah jejak. Namun, ketika senyawa mereka dicerna, mereka berbahaya bagi beberapa organ, itulah sebabnya mereka dianggap sebagai zat yang sangat beracun.
Faktanya, partikel ITO (timah dan oksida India, untuk akronimnya dalam bahasa Inggris: Indium timah oksida), sangat diperlukan untuk pembuatan layar untuk komputer dan smartphone, mereka dapat berdampak negatif terhadap kesehatan pekerja, menyebabkan mereka penyakit yang disebut paru -paru India.
Asupan partikel -partikel ini terjadi di atas semua dengan inhalasi dan dengan kontak melalui kulit dan mata.
Di sisi lain, partikel India logam halus cenderung terbakar dan menyebabkan kebakaran jika mereka adalah pagar sumber panas.

