Ionisasi dalam konsep fisika dan kimia, proses dan contoh

- 3286
- 842
- Ray Thiel
Itu ionisasi Itu semua proses di mana beban listrik dihasilkan dari partikel netral. Ini dapat terjadi melalui berbagai mekanisme atau kekuatan alami, baik dengan radiasi, panas, medan listrik, medan magnet atau reaksi kimia. Ion diproduksi sebagai konsekuensi, yang merupakan atom yang dimuat secara positif atau negatif.
Ionisasi adalah proses mendasar untuk simfin fenomena fisik, kimia atau alam, yang terakhir berkali -kali merupakan campuran dari perubahan fisikokimia. Misalnya, dalam ionisasi fisik, pada prinsipnya, reaksi kimia tidak terjadi; Yaitu, produksi ion tidak menyiratkan kerusakan atau pembentukan tautan baru.
 Banyak fenomena alam, seperti lampu utara, didasarkan pada ionisasi molekul atmosfer. Sumber: Pixabay.
Banyak fenomena alam, seperti lampu utara, didasarkan pada ionisasi molekul atmosfer. Sumber: Pixabay. Namun, dalam fenomena alam ionisasi ini biasanya disertai dengan reaksi kimia, seperti pembentukan ozon pada ketinggian rendah. Juga, selama badai nitrogen oksida dihasilkan karena sinar dan suhu intensnya, yang mengoksidasi nitrogen udara.
Di sisi lain, ionisasi dapat menyelinap ke atas: di dalam air yang sama, dalam gosok antara dua permukaan, dalam oksidasi logam atau dalam pembubaran gas tertentu dalam air.
[TOC]
Ionisasi Kimia
Pengurangan oksidasi
 Selama pengoperasian baterai mainan, ion dan elektron terus -menerus. Sumber: D J Shin/CC BY-SA (https: // CreativeCommons.Org/lisensi/by-sa/3.0)
Selama pengoperasian baterai mainan, ion dan elektron terus -menerus. Sumber: D J Shin/CC BY-SA (https: // CreativeCommons.Org/lisensi/by-sa/3.0) Dalam ionisasi kimia, ion diproduksi dengan pemecahan atau pembentukan tautan. Dua zat menghasilkan atau kehilangan elektron secara ireversibel: yang kehilangan elektron memperoleh beban positif, sedangkan orang yang menang mempertahankan beban negatif.
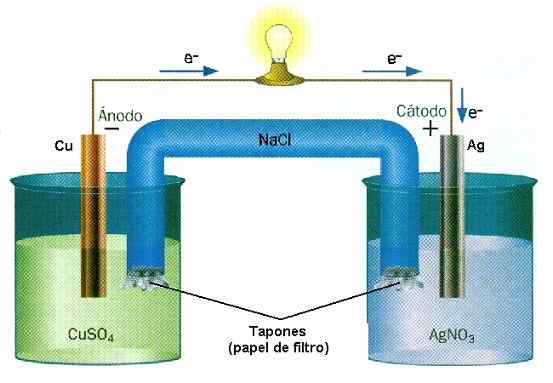
 Contoh pengurangan reaksi oksida dalam tumpukan Cu-AG. Sumber: Dinding Air/CC BY-SA (http: // CreationCommons.Org/lisensi/by-sa/3.0/)
Contoh pengurangan reaksi oksida dalam tumpukan Cu-AG. Sumber: Dinding Air/CC BY-SA (http: // CreationCommons.Org/lisensi/by-sa/3.0/) Di baterai, sebuah zat kehilangan elektron sementara yang lain memenangkannya. Elektron ini melakukan perjalanan dan mengaktifkan sirkuit listrik peralatan, untuk akhirnya kembali ke kompartemen tumpukan kedua, di mana zat lain menunggu mereka menangkapnya dan memuat secara negatif. Ini adalah contoh ionisasi kimia yang dilakukan oleh reaksi reduksi oksida.
Dapat melayani Anda: asam glukonat: struktur, sifat, sintesis, penggunaanPecahnya heterolitik
Jenis lain dari ionisasi kimia adalah karena pecahnya heterolitik. Saat istirahat ini terjadi, tautan A-B rusak untuk membentuk ion+ dan B-, Karena elektron diarahkan ke atom yang mereka "rasakan" afinitas yang lebih besar. Pecahnya heterolitik biasanya merupakan langkah pertama yang mengatur mekanisme banyak reaksi organik.
Selfionisasi
Beban listrik tidak hanya dapat muncul dengan gerakan elektron itu sendiri, tetapi oleh tautan yang rusak atau terbentuk dalam pertukaran atom. Ini adalah kasus self -alization, yang terjadi antara dua molekul dari senyawa yang sama.
Dari semua ionisasi kimia, diri sendiri adalah yang paling sederhana dan paling tidak terlihat, karena tidak memiliki kemampuan untuk melakukan arus listrik dengan sendirinya.
Ionisasi dalam fisika
Listrik statis
 Rambut gadis ini menagih secara positif dan mengusir satu sama lain karena listrik statis. Sumber: biseup ganguly/cc by (https: // createveCommons.Org/lisensi/oleh/3.0)
Rambut gadis ini menagih secara positif dan mengusir satu sama lain karena listrik statis. Sumber: biseup ganguly/cc by (https: // createveCommons.Org/lisensi/oleh/3.0) Ionisasi juga memiliki banyak partisipasi dalam fenomena fisik. Secara umum, ionisasi fisika tidak menyiratkan reaksi kimia. Atom -atom materi dibebankan secara elektrik tanpa kehilangan identitas aslinya.
Permukaan dapat bertukar elektron saat mereka menggosoknya jika salah satunya lebih efektif dalam menyimpannya, yang mengarah ke listrik statis. Tidak ada lagi pembicaraan tentang atom, tetapi dari seluruh bahan yang memperoleh beban negatif atau positif, dan bahwa ketika keseimbangan dipulihkan, sengatan listrik dapat secara harfiah menghasilkan antara dua bahan atau tubuh.
Ionisasi gas
Atom gas yang tersebar dapat kehilangan elektron jika dikenakan medan listrik. Dengan melakukan itu, atom bersemangat dan dilepaskan elektron. Kemudian, saat mendinginkan dan kembali ke status mereka sebagai energi kecil, foton mengucapkan selamat tinggal. Dan prosesnya diulang lagi dan lagi. Hasilnya: Sumber pencahayaan atau listrik.
Dapat melayani Anda: boron oksida (b2o3): apa itu, struktur, sifat, penggunaanIonisasi radiasi atau tabrakan
Demikian pula, materi dapat memperoleh energi yang disediakan oleh berbagai jenis radiasi (gamma, x -rays, ultraviolet, dll.) atau dengan bertabrakan dengan partikel energi tinggi (Alfas, Betas dan Neutron).
Energi yang disumbangkan sedemikian rupa sehingga elektron atom adalah instan. Jenis ionisasi ini terkait dengan beberapa fenomena radioaktif dan kosmik.
Ionisasi air
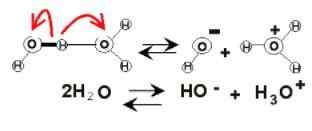 Disosiasi air
Disosiasi air Di dada air, muatan listrik mungkin muncul karena ionisasi. Ini adalah bahan kimianya, karena dua molekul air tiba -tiba bereaksi satu sama lain untuk memisahkan dan menghasilkan ion H3SALAH SATU+ dan oh-:
2h2Atau (l) ⇌ h3SALAH SATU+(Ac) + oh-(AC)
Saldo ini telah sangat terlantar ke air, jadi hampir tidak ada jumlah yang tercela dari ion -ion ini.
Ionisasi udara
Molekul udara tidak berpartisipasi dalam keseimbangan diri apa pun. Oksigen, nitrogen, argon, uap air dan gas lain yang membentuk udara, tidak bertukar atom atau elektron. Oleh karena itu, udara bukan konduktor listrik yang baik dalam kondisi normal.
Namun, jika mengalami medan listrik, radiasi, atau suhu yang intens, itu bisa menjadi ion dan menjadi pengemudi yang baik. Inilah yang terjadi, misalnya, ketika sinar listrik jatuh dari awan ke bumi, elektron bepergian melalui udara dengan ledakan cahaya yang tiba -tiba.
Contoh ionisasi
Di seluruh bagian sebelumnya, beberapa contoh ionisasi telah ditunjuk. Akhirnya, beberapa lainnya akan disebutkan.
Oksidasi logam
Saat logam teroksidasi, baik dengan aksi oksigen bumi atau dengan serangan zat asam, mereka masing -masing memperoleh muatan positif untuk membentuk oksida atau garam, masing -masing.
Dapat melayani Anda: Proses Kimia: Prinsip, Jenis, ContohMisalnya, besi terionisasi berkat oksigen untuk berubah menjadi ion iman3+, Terletak di kristal oksida besi. Magnesium, di sisi lain, larut dalam asam sulfat untuk kehilangan elektron dan tetap sebagai ion Mg2+ Dalam garam magnesium sulfat.
Pembubaran gas dalam air
Beberapa gas, seperti amonia dan hidrogen klorida, larut dalam air untuk kehilangan netralitasnya dan menimbulkan pembentukan ion. Misalnya, amonia saat larut sebagian melepaskan ion NH4+ dan oh-. Sementara itu, hidrogen klorida saat larut akan menghasilkan ion H3SALAH SATU+ dan Cl- sama sekali.
Kasing serupa adalah pembubaran garam dalam air, seperti magnesium sulfat, MGSO4. Namun, ion MG2+ Dan sebagainya42- Mereka sudah hadir di kristal garam sebelum larut dalam air.
Lampu atau tabung pencahayaan

Dalam lampu uap atau tabung pencahayaan, atom gas dengan sengatan listrik bersemangat untuk menghasilkan sejumlah cahaya dan warna. Misalnya, ionisasi ini terjadi pada lampu natrium atau merkuri, serta pada lampu neon yang terkenal dengan warna -warna cerah di restoran atau entri toko.
Energi ionisasi
Energi ionisasi, sifat periodik, dipelajari untuk mengkarakterisasi elemen kimia sesuai dengan kemudahan dengan mana atom gas mereka menyumbangkan elektron mereka untuk memuat secara positif. Jadi, misalnya, logam biasanya memiliki energi ionisasi terendah, sedangkan elemen non -metalik dan gas mulia, tertinggi.
Referensi
- Whitten, Davis, Peck & Stanley. (2008). Kimia. (Edisi ke -8.). Pembelajaran Cengage.
- Serway, r., Jewett, J. (2008). Fisika untuk Sains dan Teknik. Volume 1. 7. Edisi. Meksiko. Editor Pembelajaran Cengage.
- Shiver & Atkins. (2008). Kimia anorganik. (Edisi keempat). MC Graw Hill.
- Wikipedia. (2020). Ionisasi. Diperoleh dari: di.Wikipedia.org
- Para editor Eeritlopaedia Britannica. (17 Oktober 2016). Ionisasi. Encyclopædia Britannica. Dipulihkan dari: Britannica.com
- Doug Stewart. (2018). Definisi ionisasi: Apa itu ionisasi? Pulih dari: chemicool.com
- John Zavisa. (1 April 2020). Bagaimana kilat bekerja. Pulih dari: sains.Howstuffwork.com
- « 18 jenis perilaku dan karakteristiknya (dengan contoh)
- Asal Liberalisme Kuning, Karakteristik, Penyebab, Konsekuensi »

