Isomería
- 3735
- 99
- Dewey Runolfsdottir
Apa isomeria?
Isomería adalah fenomena kimia yang ditandai di mana molekul dengan jumlah atom yang sama memiliki sifat kimia atau fisik yang berbeda. Dengan demikian, itu terjadi di isomer, yang pada gilirannya adalah molekul yang formula kimianya sama, tetapi struktur atau ketentuan spasial mereka berbeda secara substansial satu sama lain.
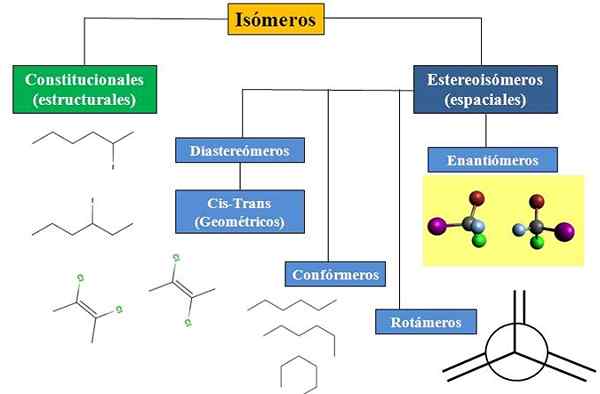
Kami memiliki isomeria konstitusional atau struktural, dan spasi isomería, yang memusatkan banyak perhatian dalam stereokimia. Diagram aliran gambar yang lebih rendah menunjukkan bahwa isomer terutama dibagi menjadi dua jenis isomería yang baru saja disebutkan: konstitusional dan stereoisomer.
 Diagram alir untuk berbagai jenis isomer dalam kimia organik. Sumber: Gabriel Bolívar.
Diagram alir untuk berbagai jenis isomer dalam kimia organik. Sumber: Gabriel Bolívar. Semua isomer, untuk senyawa tertentu, memiliki formula kimia yang sama. Tetapi struktur yang dapat membangun atom -atom ini dan proporsinya unik untuk setiap molekul atau isomer. Juga, bahkan jika struktur itu sendiri sama, atom atau kelompok dapat menempati posisi spasial yang berbeda.
Dalam diagram aliran, beberapa contoh isomer yang akan dibahas di bagian selanjutnya ditampilkan.
Jenis isomer
Konstitusional
Isomer konstitusional atau struktural adalah yang berbeda dalam pemesanan kerangka molekuler. Artinya, atom mereka tidak terkait dengan cara yang sama, sehingga struktur atau kelompok fungsional yang dimaksud dapat menjadi sangat berbeda.
Misalnya, untuk formula kimia yang sama C7H10Atau mungkin ada banyak molekul yang memenuhi jumlah atom itu; Semua akan memiliki atom oksigen tunggal, tetapi disposisi struktural atom lainnya akan unik untuk setiap isomer.
Dan karena itu, sifat kimia dan fisik dari semua isomer konstitusional untuk formula C7H10Atau juga akan sangat berbeda satu sama lain.
Di sisi lain, isomer konstitusional bisa sangat sederhana, hanya bervariasi dalam posisi relatif dari satu atom atau kelompok. Di bagian berikut, contoh dari ini dan di atas akan terlihat.
Stereoisomer
Stereoisomer adalah mereka yang memiliki urutan struktural yang sama, tetapi berbeda dalam posisi spasial dan orientasi atom atau kelompok mereka.
Dapat melayani Anda: amplitudo termodulasiAgar keberadaannya dimungkinkan, molekul -molekul harus mengandung pusat -pusat stereogenik, menjadi yang paling terkenal dalam kimia organik atom karbon asimetris atau kiral; yaitu, dengan empat substituen berbeda.
Selain karbon asimetris, molekul yang dipertimbangkan harus kekurangan elemen simetri. Kalau tidak, tidak mungkin bagi sistem spasial untuk bertambah di stereoisome.
Enantiomer
Enantiomer adalah stereoisomer yang terdiri dari gambar cermin non -superpimposing. Misalnya, tangan kanan dan kiri tidak tumpang tindih, seperti sepatu atau sarung tangan. Di bagian berikut, contoh klasik enantiomeía akan ditangani: bromocloreyodomethane: cbrcli.
Diastreomer
Diastreomer, di sisi lain, juga merupakan stereoisomer tetapi bukan gambar specular. Yaitu, menempatkan satu di depan yang lain bukanlah cerminan dari diri mereka sendiri. Dari diastomer paling terkenal, kami memiliki isomeria CIS-Trans, juga disebut isomer geometris, terutama ketika diterapkan pada alkena.
Conformeros
Konformer, bahkan jika mereka berada dalam spektrum stereoisome, sebenarnya bukan isomer. Ini adalah konfigurasi ruang yang menjadi molekul, pada waktu atau keadaan energi tertentu, memperoleh melalui rotasi beberapa tautannya. Contoh konformer dari N-heksana.
Rotámeros
Akhirnya kami memiliki rotarmers, yang menyerupai konformer dalam arti yang bergantung pada rotasi ikatan kovalen.
Namun, satu hubungan antara dua atom karbon diambil sebagai referensi, dan posisi relatif dibandingkan, dikalahkan atau diganti, substituen untuk kedua karbon. Kemudian contoh rotarmer propilen akan terlihat.
Contoh isomer
Hexane Iodine
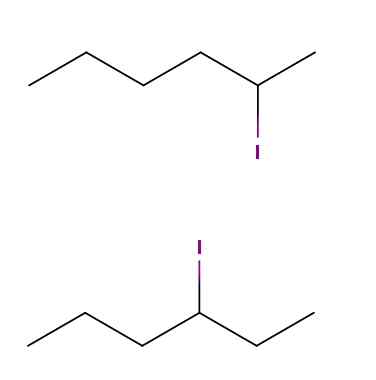 Isomer konstitusional yodium heksana. Sumber: Gabriel Bolívar via Molview.
Isomer konstitusional yodium heksana. Sumber: Gabriel Bolívar via Molview. Di atas kami memiliki dua molekul yang formula kimianya adalah C6H13yo. Pada yang pertama, kami memiliki 2-iodhexan, sedangkan yang kedua 3-iodhexan. Mereka adalah isomer konstitusional posisi, karena kerangka itu sama, dengan perbedaan bahwa posisi atom yodium bervariasi dari satu karbon ke yang lain.
Dapat melayani Anda: gesekan statis: koefisien, contoh, olahragaC3H8SALAH SATU
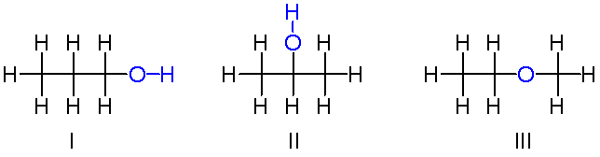 Sumber: V8Rik, CC BY-SA 3.0, via Wikimedia Commons
Sumber: V8Rik, CC BY-SA 3.0, via Wikimedia Commons Up kami memiliki contoh lain isomer konstitusional untuk formula kimia C3H8SALAH SATU. Molekul I dan II masing-masing adalah 1-propanol dan 2-propanol. Keduanya alkohol. Sebaliknya, molekul III adalah etil-metil.
Oleh karena itu, kami berbicara tentang kelompok fungsional lain. Perhatikan bahwa ketiga molekul memiliki jumlah atom yang sama, tetapi strukturnya berbeda.
2,3-Decloro-2-Butene
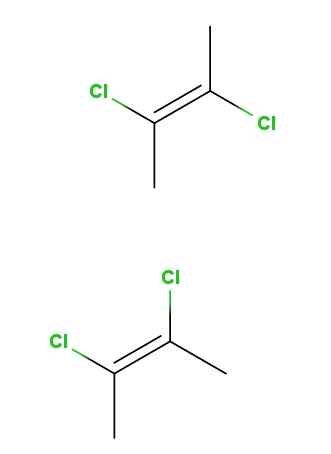 Isomer geometris 2,3-dekloro-2-butene. Sumber: Gabriel Bolívar via Molview.
Isomer geometris 2,3-dekloro-2-butene. Sumber: Gabriel Bolívar via Molview. Up kami memiliki isomer trans-22,3-decloro-2-butene, dan di bawah isomer CIS-2,3-dikloro-2-butene-butene. Pada yang pertama, atom klorin ditemukan pada posisi yang berlawanan mengenai ikatan rangkap, sedangkan pada kedua mereka berbaring di sisi yang sama dari ikatan rangkap.
Kerangka untuk kedua molekul adalah sama, tetapi berbeda dalam posisi spasial atom klorin; Oleh karena itu, mereka adalah stereoisomer, dan bukan gambar specular, mereka menjadi diamereomer.
3-Flúor-2-methylciclohexan
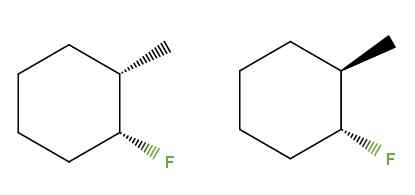 Diastereomer 3-Flúor-2-Methylciclohexano. Sumber: Gabriel Bolívar via Molview.
Diastereomer 3-Flúor-2-Methylciclohexano. Sumber: Gabriel Bolívar via Molview. Kali ini, alih-alih ikatan rangkap, kami memiliki cincin sikloheksan untuk senyawa 3-flúor-2-methylciclohexan. Di isomer di sebelah kiri, kelompok3 dan F terletak di bawah bidang cincin; Saat di sebelah kanan, cho3 naik dan f di bawah.
Oleh karena itu, yang di sebelah kiri akan sesuai dengan isomer cis, dan yang di sebelah kanan akan menjadi isomer trans. Karena itu mereka diamereomer, karena mereka bukan gambar specular lagi.
Conformeros del N-heksana
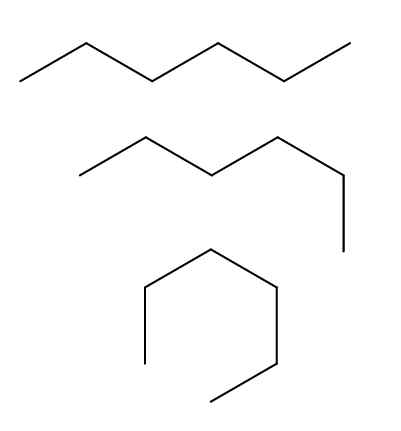 Konformer N-heksana. Sumber: Gabriel Bolívar via Molview.
Konformer N-heksana. Sumber: Gabriel Bolívar via Molview. Kami memiliki tiga konformer dari N-Hexano, yang dihasilkan dari rotasi dan "lipatan" dari rantai berkarbonasi dalam orientasi yang berbeda. Semua sesuai dengan molekul yang sama N-Heksana dengan tingkat lipat yang berbeda, yang akan tergantung pada lingkungan dan energi internal dari masing -masing molekul.
3-bromo-2-penol
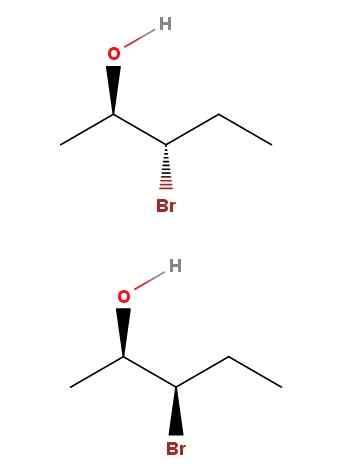 Diastreomer 3-bromo-2-pentanol. Sumber: Gabriel Bolívar via Molview.
Diastreomer 3-bromo-2-pentanol. Sumber: Gabriel Bolívar via Molview. Dalam 3-bromo-2-pantanol kami memiliki contoh lain dari sepasang diastereomer. Perhatikan bahwa sekali lagi, di isomer di atas kita memiliki OH dan BR menunjuk ke arah yang bertentangan dengan bidang kerangka; Sementara di isomer di bawah ini, kedua kelompok menunjuk ke arah pembaca.
Ini dapat melayani Anda: Hukum Kedua Termodinamika: Rumus, Persamaan, Contoh1-bromo-3-chloro-5-ethylciclohexan
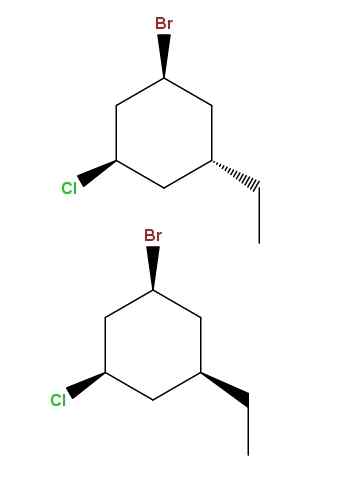 Diastreomer 1-bromo-3-clor-5-ethylciclohexan. Sumber: Gabriel Bolívar via Molview.
Diastreomer 1-bromo-3-clor-5-ethylciclohexan. Sumber: Gabriel Bolívar via Molview. Dan sekali lagi, kami memiliki sepasang diastereomer lain, dengan perbedaan bahwa sekarang perbedaannya terletak pada posisi spasial satu kelompok: etil, -ch2Ch3.
Jenis isomer ini memiliki nama yang sangat spesifik: Epigmers, yang merupakan diastheomer yang variasinya diamati hanya dalam konfigurasi spasial karbon asimetris tunggal; Dalam hal ini, yang terkait dengan -ch2Ch3.
Bromocloreyodomethane
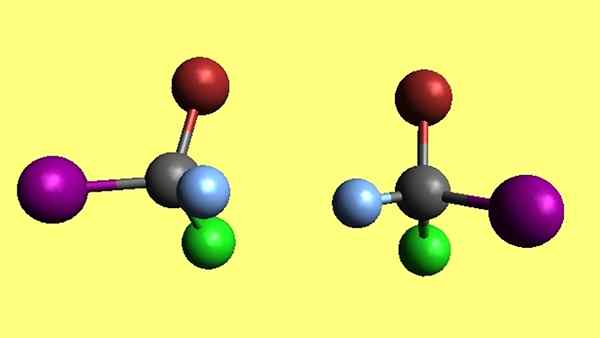 Sepasang enantimer bromocloreyodomethane. Sumber: Gabriel Bolívar.
Sepasang enantimer bromocloreyodomethane. Sumber: Gabriel Bolívar. Perhatikan bahwa dua molekul bromoclloroyodomethane, cbrcli, adalah enansiomer karena satu adalah refleksi yang tidak dapat ditumpuk dari yang lain. Sebanyak yang Anda coba, keempat atom Anda tidak akan pernah bertepatan. Dikatakan bahwa mereka memiliki konfigurasi ruang yang berlawanan.
2-bromo-4-ethylciclohexan
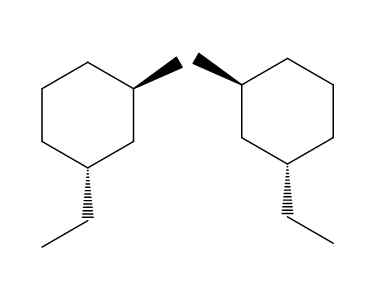 Inantitimer dari 2-bromo-4-ethylciclohexan. Sumber: Gabriel Bolívar via Molview.
Inantitimer dari 2-bromo-4-ethylciclohexan. Sumber: Gabriel Bolívar via Molview. Dalam contoh torsi molekul 2-bromo-4-ethylciclohexan. Jika kami mencoba membalik molekul sayap kanan, kami akan melihat bahwa grup -ch2Ch3 Itu tidak akan terletak di bawah cincin tetapi di atas.
Demikian pula, cho3 Itu tidak akan menunjuk cincin tetapi di bawah. Pengaturan ruang diinvestasikan, mereka berlawanan. Ini adalah fitur lain yang paling penting dari Enatiomeía.
Rotámeros del Propileno
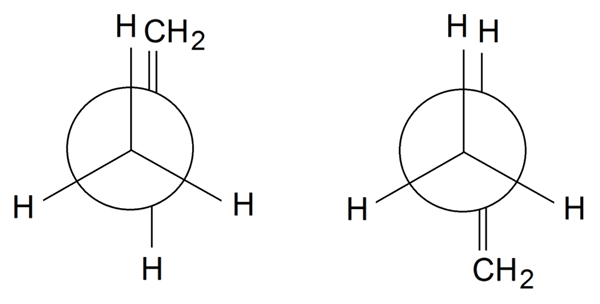 Rotámeros del Propileno. Sumber: Samuele Madini, CC BY-SA 4.0, via Wikimedia Commons
Rotámeros del Propileno. Sumber: Samuele Madini, CC BY-SA 4.0, via Wikimedia Commons Di rotámeros del propileno, untuk menyelesaikan, kami memutar tautan sederhana antara c1 dan C2: H3C-ch = ch2. Grup = ch2 Itu dalam posisi yang dikalahkan dengan salah satu h3 Depan di rotamer di sebelah kiri. Sementara itu, = cho2 Dan h berada dalam posisi bergantian di kanan -hand.
Tergantung pada gerhana atau tidak dari grup, kami akan memiliki hambatan sterik, yang akan mengganggu kestabilan rotamero. Oleh karena itu, rota sayap kanan lebih stabil daripada yang di sebelah kiri.
Referensi
- Graham Solomons t.W., Craig b. Fryhle. (2011). Kimia organik. (10th Edisi.). Wiley Plus.
- Carey f. (2008). Kimia organik. (Edisi Keenam). MC Graw Hill.
- Morrison dan Boyd. (1987). Kimia organik. (Edisi Kelima). Addison-Wesley Iberoamericana.
- Kata. S. Gevorg. (2020). Enantiomer, diastreomer, isomer identik atau konstitusional. Langkah Kimia. Pulih dari: chemistroysteps.com
- Wikipedia. (2020). Isomer. Diperoleh dari: di.Wikipedia.org
- Allison Soult. (13 Agustus 2020). Isomer. Libretteks Kimia. Pulih dari: chem.Librettexts.org
- James Ashenhurst. (2020). Stereokimia dan kiralitas. Dipulihkan dari: Masterorganicchemistry.com

