Definisi Massa Atom, Jenis, Cara Menghitungnya, Contoh
- 5091
- 1504
- Dewey Runolfsdottir
Itu massa atom Ini adalah jumlah materi yang ada dalam atom, yang dapat diekspresikan dalam unit fisik biasa atau dalam unit massa atom (UMA atau U). Atom kosong di hampir seluruh strukturnya; elektron yang kabur di daerah yang disebut orbital, di mana ada kemungkinan tertentu untuk menemukannya, dan nukleus mereka.
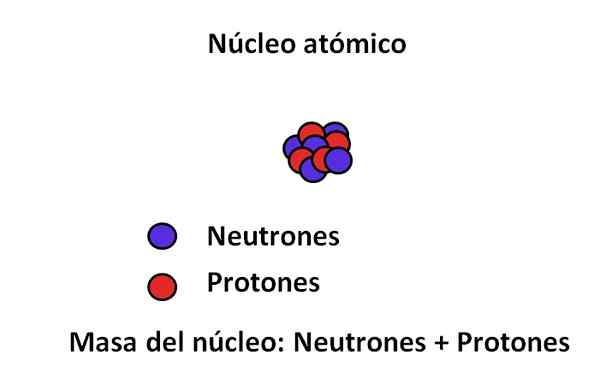
Dalam inti atom adalah proton dan neutron; Yang pertama dengan muatan positif, sedangkan detik dengan beban netral. Kedua partikel subatomik ini memiliki massa yang jauh lebih besar daripada elektron; Oleh karena itu, massa atom diatur oleh nukleusnya dan bukan oleh kekosongan atau elektron.
 Partikel subatomik utama dan massa nukleus. Sumber: Gabriel Bolívar.
Partikel subatomik utama dan massa nukleus. Sumber: Gabriel Bolívar. Massa elektron sekitar 9,1 · 10-31 kg, sedangkan proton 1.67 · 10-27 kg, menjadi rasio massa 1.800; yaitu, proton "menimbang" 1.800 kali lebih banyak dari elektron. Demikian pula hal yang sama terjadi dengan massa neutron dan elektron. Itulah sebabnya kontribusi massa elektron untuk tujuan biasa dianggap dapat diabaikan.
Karena itu, biasanya diasumsikan bahwa massa atom, atau massa atom hanya tergantung pada massa nukleus; yang pada gilirannya, terdiri dari jumlah subjek neutron dan proton. Dari alasan ini dua konsep muncul: jumlah massa dan massa atom, keduanya terkait erat.
Memiliki begitu banyak "kosong" dalam atom, dan karena massanya hampir seluruhnya menjadi inti, diharapkan yang terakhir akan sangat padat.
Jika kami membawa kekosongan ini ke tubuh atau objek apa pun, dimensinya akan secara drastis. Juga, jika kita dapat membangun objek kecil berdasarkan inti atom (tanpa elektron), maka ini akan memiliki massa jutaan ton.
Di sisi lain, massa atom membantu membedakan atom yang berbeda dari elemen yang sama; Ini adalah, isotop. Memiliki isotop yang lebih berlimpah daripada yang lain, rata -rata massa atom untuk elemen tertentu harus diperkirakan; rata -rata yang dapat bervariasi dari planet di planet, atau dari satu wilayah ruang ke yang lain.
[TOC]
Definisi dan konsep

Menurut definisi, massa atom adalah jumlah massa proton dan neutron mereka yang diekspresikan dengan UMA atau U. Angka yang dihasilkan (juga disebut nomor massa) ditempatkan tanpa dimensi di sudut kiri atas dalam notasi yang digunakan untuk nukleid. Misalnya, untuk elemen limabelasX Massa atomnya adalah 15um atau 15u.
Massa atom tidak bisa banyak bicara tentang identitas sebenarnya dari elemen ini x. Sebaliknya, nomor atom digunakan, yang sesuai dengan proton yang menampung inti x. Jika angka ini adalah 7, maka perbedaannya (15-7) akan sama dengan 8; yaitu, x memiliki 7 proton dan 8 neutron, yang jumlahnya 15.
Kembali ke gambar, nukleus memiliki 5 neutron dan 4 proton, sehingga jumlah massanya adalah 9; Dan pada gilirannya 9 Uma adalah massa atomnya. Memiliki 4 proton, dan berkonsultasi dengan tabel periodik, dapat dilihat bahwa nukleus ini sesuai dengan elemen berilium, menjadi (atau 9MENJADI).
Unit Massa Atom
Atom terlalu kecil untuk mengukur massa mereka melalui metode konvensional atau skala biasa. Karena alasan inilah Uma, atau o da (Daltón) ditemukan. Unit -unit ini dirancang untuk atom memungkinkan Anda memiliki gagasan tentang seberapa besar atom suatu unsur dalam kaitannya satu sama lain.
Dapat melayani Anda: kobalt: struktur, sifat, aplikasiTapi apa sebenarnya yang diwakili oleh UMA? Harus ada referensi yang memungkinkan Anda menjalin hubungan massa. Untuk melakukan ini, atom digunakan sebagai referensi 12C, yang merupakan isotop karbon yang paling melimpah dan stabil. Memiliki 6 proton (jumlah atom z), dan 6 neutron, karenanya massa atomnya adalah 12.
Diasumsikan bahwa proton dan neutron memiliki massa yang sama, sehingga setiap kontribusi 1 UMA. Unit massa atom kemudian didefinisikan sebagai dua belas bagian (1/12) dari massa atom karbon-12; Ini, massa proton atau neutron.
Kesetaraan dalam gram
Dan sekarang pertanyaan berikut muncul: Berapa banyak gram yang setara dengan 1 UMA? Seperti pada awalnya tidak ada teknik yang cukup maju untuk mengukurnya, bahan kimia harus puas mengekspresikan semua massa dengan UMA; Namun, ini adalah keuntungan dan bukan kerugian.
Karena? Karena menjadi partikel subatomik kecil, sama seperti seorang anak, itu harus massa yang diekspresikan dalam gram. Faktanya, 1 UMA setara dengan 1.6605 · 10-24 gram. Selain itu, dengan penggunaan konsep mol, itu bukan masalah untuk mengerjakan massa elemen dan isotopnya dengan UMA mengetahui bahwa unit -unit tersebut dapat dimodifikasi menjadi g/mol.
Misalnya, kembali ke limabelasX dan 9Jadilah, kita memiliki massa atom mereka masing -masing adalah 15 UMA dan 9 UMA. Karena unit -unit ini sangat kecil dan tidak mengatakan seberapa penting seseorang harus "menimbang" untuk memanipulasi mereka, mereka berubah menjadi massa molar masing -masing: 15 g/mol dan 9 g/mol (memperkenalkan konsep mol dan bilangan avogadro).
Massa atom rata -rata
Tidak semua atom dari elemen yang sama memiliki massa yang sama. Ini berarti bahwa mereka harus memiliki lebih banyak partikel subatomik dalam nukleus. Menjadi elemen yang sama, jumlah atom atau jumlah proton harus tetap konstan; Oleh karena itu, hanya ada variasi dalam jumlah neutron yang memiliki.
Dengan demikian, tampaknya definisi isotop: atom dari elemen yang sama tetapi dengan massa atom yang berbeda. Misalnya, berilium hampir seluruhnya terdiri dari isotop 9Jadilah, dengan jejak jejak 10Menjadi. Namun, contoh ini tidak membantu banyak membantu untuk memahami konsep rata -rata massa atom; Kami membutuhkan satu dengan lebih banyak isotop.
Contoh
Misalkan elemen itu ada 88J, ini menjadi isotop utama J dengan kelimpahan 60%. J Selain itu memiliki dua isotop lainnya: 86J, dengan berlimpah 20%, dan 90J, dengan kelimpahan juga 20%. Ini berarti bahwa dari 100 J atom yang kami kumpulkan di bumi, 60 di antaranya 88J, dan 40 sisanya campuran 86J dan 90J.
Masing -masing dari tiga isotop J memiliki massa atomnya sendiri; yaitu, jumlah neutron dan protonnya. Namun, massa ini harus dirata -rata untuk dapat memiliki atom massa atom untuk j; Di sini, karena mungkin ada daerah lain di alam semesta di mana kelimpahan 86J adalah 56% dan bukan 60%.
Dapat melayani Anda: Sodium: Sejarah, Struktur, Sifat, Risiko dan PenggunaanUntuk menghitung rata -rata massa atom J, rata -rata tertimbang massa isotop mereka harus diperoleh; yaitu, dengan mempertimbangkan persentase kelimpahan untuk masing -masing. Demikianlah kita memiliki:
Massa rata -rata (j) = (86 UMA) (0,60) + (88 UMA) (0,20) + (90 UMA) (0,20)
= 87.2 UMA
Artinya, massa atom rata -rata (juga dikenal sebagai j adalah 87,2 UMA. Sementara itu, massa molarnya adalah 87,2 g/mol. Perhatikan bahwa 87.2 lebih dekat dari 88 dari 86, dan juga jauh dari 90.
Massa atom absolut
Massa atom absolut adalah massa atom yang diekspresikan dalam gram. Mulai dari contoh elemen hipotetis, kita dapat menghitung massa atom absolutnya (rata -rata) mengetahui bahwa setiap UMA setara dengan 1.6605 · 10-24 gram:
Massa atom absolut (j) = 87.2 UMA * (1.6605 · 10-24 G/ UMA)
= 1.447956 · 10-22 g/atom j
Ini berarti bahwa rata -rata atom J memiliki massa absolut 1,447956 · 10-22 G.
Massa Atom Relatif
Massa atom relatif identik dengan massa atom rata -rata untuk elemen yang diberikan; Namun, tidak seperti yang kedua, yang pertama tidak memiliki persatuan. Oleh karena itu, itu tidak berdimensi. Misalnya, rata -rata massa atom berilium adalah 9.012182 U; sedangkan massa atom relatif hanya 9.012182.
Itulah sebabnya kadang -kadang konsep -konsep ini biasanya salah paham sebagai sinonim, karena mereka sangat mirip dan perbedaan di antara mereka halus. Tapi massa ini relatif? Relatif terhadap dua belas bagian dari massa 12C.
Dengan demikian, elemen dengan massa atom relatif 77 berarti memiliki massa 77 kali lebih besar dari 1/12 bagian dari 12C.
Mereka yang telah mendapatkan elemen dalam tabel periodik dapat melihat bahwa massa mereka diungkapkan secara relatif. Mereka tidak memiliki unit UMA, dan ditafsirkan sebagai: besi memiliki massa atom 55.846, yang berarti bahwa itu adalah 55.846 kali lebih besar daripada massa 1/12 bagian dari 12C, dan itu juga dapat dinyatakan sebagai 55.846 UMA atau 55.846 g/mol.
Cara menghitung massa atom
Secara matematis contoh cara menghitungnya dengan contoh elemen j. Secara umum, formula rata -rata tertimbang harus diterapkan, yang akan menjadi:
P = σ (massa atom isotop) (kelimpahan dalam desimal)
Dengan kata lain, memiliki massa atom (neutron + proton) dari masing -masing isotop (alam biasa) untuk elemen tertentu, serta kelimpahan terestrial masing -masing (atau apa pun yang dipertimbangkan wilayah tersebut), kemudian mengatakan rata -rata tertimbang dapat dihitung.
Dan mengapa tidak sekadar rata -rata aritmatika? Misalnya, massa atom rata -rata J adalah 87,2 UMA. Jika kita menghitung massa ini lagi tetapi dengan cara aritmatika kita akan memiliki:
Massa rata -rata (j) = (88 UMA + 86 UMA + 90 UMA)/3
= 88 UMA
Perhatikan bahwa ada perbedaan penting antara 88 dan 87.2. Ini karena dalam rata -rata aritmatika diasumsikan bahwa kelimpahan semua isotop adalah sama; Ketika ada tiga isotop J, masing -masing harus memiliki kelimpahan 100/3 (33,33%). Tapi itu tidak juga: ada jauh lebih banyak isotop daripada yang lain.
Itu dapat melayani Anda: uretan: struktur, sifat, mendapatkan, menggunakanItulah sebabnya rata -rata tertimbang dihitung, karena dipertimbangkan seberapa berlimpah isotop sehubungan dengan yang lain.
Contoh
Karbon
Untuk menghitung massa atom karbon rata -rata kita membutuhkan isotop alami dengan kelimpahan masing -masing. Dalam hal karbon ini adalah: 12C (98,89%) dan 13C (1,11%). Massa atom relatif masing -masing adalah 12 dan 13, yang pada gilirannya sama dengan 12 UMA dan 13 UMA. Memecahkan:
Massa atom rata -rata (C) = (12 UMA) (0,9889) + (13 UMA) (0,0111)
= 12.0111 UMA
Oleh karena itu, massa atom karbon rata -rata 12,01 UMA. Memiliki jumlah jejak 14C, hampir tidak ada pengaruh pada rata -rata ini.
Sodium
Semua atom natrium terestrial terdiri dari isotop 23Na, jadi kelimpahannya 100%. Itulah sebabnya dalam perhitungan biasa dapat diasumsikan bahwa massanya hanya 23 UMA atau 23 g/mol. Namun, massa yang tepat adalah 22.98976928 UMA.
Oksigen
Tiga isotop oksigen dengan kelimpahan masing -masing adalah: 16O (99.762%), 17Atau (0,038%) dan 18O (0,2%). Kami memiliki segalanya untuk menghitung massa atom rata -rata:
Massa atom rata -rata (O) = (16 UMA) (0,99762) + (17 UMA) (0,00038) + (18 UMA) (0,002)
= 16.00438 UMA
Meskipun massa yang tepat dilaporkan sebenarnya 15.9994 UMA.
Nitrogen
Mengulangi langkah yang sama dengan oksigen yang kami miliki: 14N (99.634%) dan limabelasN (0,366%). Jadi:
Massa atom rata -rata (n) = (14 UMA) (0,99634) + (15 UMA) (0,00366)
= 14.00366 UMA
Perhatikan bahwa massa yang dilaporkan untuk nitrogen adalah 14.0067 UMA, sedikit lebih besar dari yang kami hitung.
Klorin
Isotop klorin dengan kelimpahan masing -masing adalah: 35Cl (75,77%) dan 37Cl (24,23%). Menghitung massa atom rata -rata yang kami miliki:
Massa atom rata -rata (cl) = (35 UMA) (0,7577) + (37 UMA) (0,2423)
= 35.4846 UMA
Sangat mirip dengan laporan (35.453 UMA).
Disposio
Dan akhirnya, massa rata -rata elemen dengan banyak isotop alami akan dihitung: disposio. Ini dan dengan kelimpahan masing -masing adalah: 156Dy (0,06%), 158Dy (0,10%), 160Dy (2,34%), 161Dy (18,91%), 162Dy (25,51%), 163Dy (24,90%) dan 164Dy (28,18%).
Kami melanjutkan seperti contoh sebelumnya untuk menghitung massa atom logam ini:
Rata -rata massa atom (dy) = (156 UMA) (0,0006%) + (158 UMA) (0,0010) + (160 UMA) (0,0234) + (161 UMA) (0,1891) + (162 UMA) (0,2551) + (163 UMA) (0,2490) + (164 UMA) (0,2818)
= 162.5691 UMA
Massa yang dilaporkan adalah 162.500 UMA. Perhatikan bahwa rata -rata ini adalah antara 162 dan 163, karena isotop 156Dy, 158Dy dan 160Dy sedikit berlimpah; sementara mereka yang mendominasi 162Dy, 163Dy dan 164Dy.
Referensi
- Whitten, Davis, Peck & Stanley. (2008). Kimia. (Edisi ke -8.). Pembelajaran Cengage.
- Wikipedia. (2019). Massa atom. Diperoleh dari: di.Wikipedia.org
- Christopher Masi. (S.F.). Massa atom. Dipulihkan dari: WSC.Massa.Edu
- Natalie Wolchover. (12 September 2017). Bagaimana Anda menimbang atom? Ilmu langsung. Dipulihkan dari: LiveScience.com
- Libretteks Kimia. (5 Juni 2019). Menghitung massa atom. Pulih dari: chem.Librettexts.Orks
- Edward Wichers dan H. Steffen Peiser. (15 Desember 2017). Berat atom. Encyclopædia Britannica. Dipulihkan dari: Britannica.com
- « Karakteristik Terapi Elektrokonvulsif, Efek dan Aplikasi
- Sejarah embriologi, bidang studi dan cabang »

