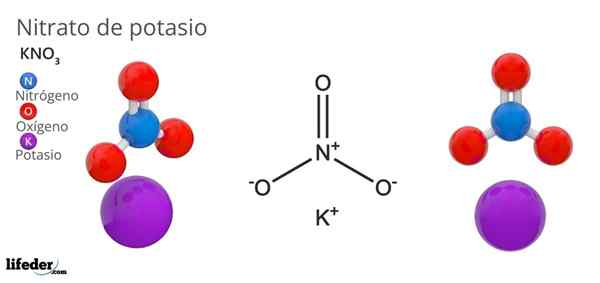
Kalium nitrat (KNO3)
- 3508
- 503
- Miss Wm Hudson
Apa itu kalium nitrat?
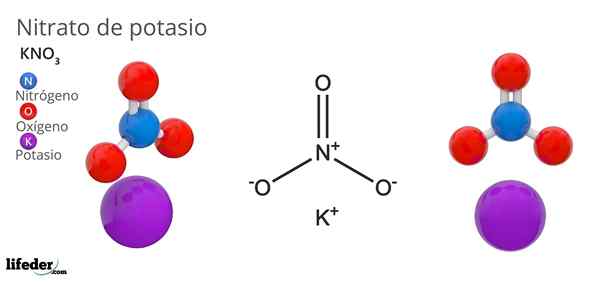
Dia potasium nitrat Ini adalah garam terner yang terdiri dari kalium, logam alkali, dan oxoanion nitrat. Formula kimianya adalah Kno3, Yang berarti bahwa untuk setiap ion k+, Tidak ada ion3-- berinteraksi dengan ini. Oleh karena itu, itu adalah garam ionik dan merupakan salah satu nitrat alkali (lino3, Kakak3, Rbno3...).
Kno3 Ini adalah agen pengoksidasi yang kuat karena adanya anion nitrat. Artinya, ini berfungsi sebagai cadangan ion nitrat padat, tidak seperti, tidak seperti garam yang sangat larut dalam air atau sangat higroskopis. Banyak sifat dan penggunaan senyawa ini disebabkan oleh anion nitrat, daripada kation kalium.
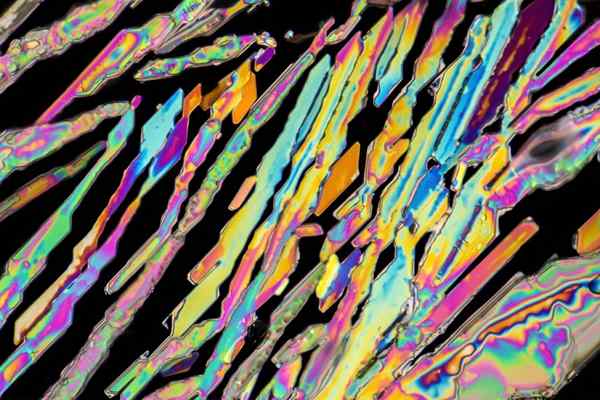 Kristal Kalium Nitrat
Kristal Kalium Nitrat Pada gambar atas beberapa kristal kno diilustrasikan3 dengan bentuk jarum. Sumber Kno Alami3 adalah garam, dikenal sebagai nama Sendawa salah satu Balon, dalam bahasa Inggris. Elemen ini juga dikenal sebagai potassa nitrat atau nitro mineral.
Terletak di daerah gersang atau gurun, serta efflorescences dari dinding gua. Sumber penting lain dari Kno3 Itu adalah guano, kotoran hewan yang menghuni lingkungan kering.
Struktur kimia kalium nitrat
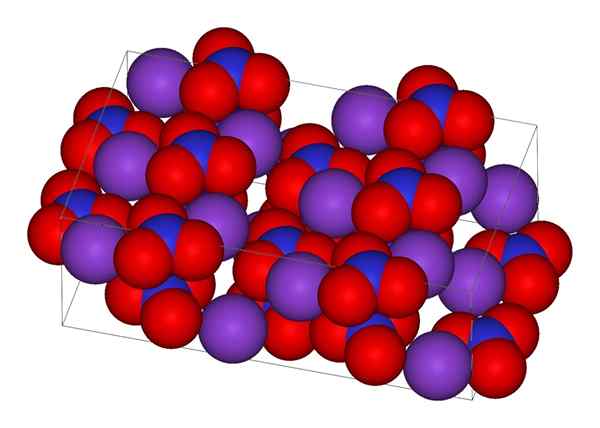 Struktur kristal kalium nitrat
Struktur kristal kalium nitrat Pada gambar atas struktur kristal KNO diwakili3. Bola ungu sesuai dengan ion k+, sedangkan merah dan biru masing -masing adalah atom oksigen dan nitrogen. Struktur kristal adalah ortorombik pada suhu kamar.
Geometri nion no3- Ini adalah bidang trigonal, dengan atom oksigen di simpul segitiga, dan atom nitrogen di tengahnya. Ini menyajikan beban formal positif dalam atom nitrogen, dan dua beban formal negatif dalam dua atom oksigen (1-2 = (-1)).
Dapat melayani Anda: mikroskop sederhanaDua tuduhan negatif ini dari no3- Mereka pindah antara tiga atom oksigen, selalu mempertahankan beban positif dalam nitrogen. Sebagai konsekuensi dari hal di atas, k ion-+ dari kristal yang mereka hindari tepat di atas atau di bawah nitrogen anion bukan3-.
Faktanya, gambar menunjukkan bagaimana ion k+ Mereka dikelilingi oleh atom oksigen, bola merah. Sebagai kesimpulan, interaksi ini bertanggung jawab atas pengaturan kristal.
Fase kristal lainnya
Variabel seperti tekanan dan suhu dapat memodifikasi pengaturan ini dan menyebabkan fase struktural yang berbeda untuk KNO3 (Fase I, II dan III). Sebagai contoh, fase II adalah gambar, sedangkan fase I (dengan struktur kristal trigonal) terbentuk ketika kristal dipanaskan hingga 129 ºC.
Fase III adalah padatan transisional yang diperoleh dari pendinginan fase I, dan beberapa penelitian telah menunjukkan bahwa itu menunjukkan beberapa sifat fisik yang penting, seperti feroelektrik. Dalam fase ini kristal membentuk lapisan kalium dan nitrat, mungkin sensitif terhadap tolakan elektrostatik antara ion.
Di lapisan fase III anion no3- Mereka kehilangan sedikit planaritas mereka (sedikit kurva segitiga) untuk memungkinkan pengaturan ini, yang, sebelum gangguan mekanis, menjadi struktur fase II.
Penggunaan/aplikasi kalium nitrat
Garam sangat penting, karena digunakan dalam berbagai kegiatan manusia, yang bermanifestasi dalam industri, pertanian, makanan, dll. Penggunaan ini termasuk yang berikut:
- Pengawetan makanan, terutama daging. Terlepas dari kecurigaan bahwa itu mengintervensi pembentukan nitrosamin (agen karsinogenik) masih digunakan dalam charcuterie.
- Pupuk, karena kalium nitrat menyediakan dua dari tiga tanaman makronutrien: nitrogen dan kalium. Bersama dengan fosfor, elemen ini diperlukan untuk pengembangan tanaman. Artinya, ini merupakan cadangan penting dan dapat dikelola dari nutrisi ini.
- Mempercepat pembakaran, mampu menghasilkan ledakan jika bahan yang mudah terbakar luas atau jika dibagi dengan halus (luas permukaan yang lebih besar, reaktivitas yang lebih besar). Selain itu, ini adalah salah satu komponen utama bubuk mesiu.
- Memfasilitasi penghapusan sentuhan pohon yang ditebak. Nitrat memasok nitrogen yang diperlukan untuk jamur untuk menghancurkan kayu tunggul.
- Ini mengintervensi pengurangan sensitivitas gigi melalui penggabungannya dalam dentifrices, yang meningkatkan perlindungan sensasi menyakitkan gigi yang dihasilkan oleh dingin, panas, asam, permen atau kontak.
- Campur tangan sebagai hipotensor dalam regulasi tekanan darah pada manusia. Efek ini akan diberikan atau saling terkait dengan perubahan ekskresi natrium. Dosis yang direkomendasikan dalam perawatan adalah 40-80 meq/hari kalium. Dalam hal ini, ditunjukkan bahwa kalium nitrat akan memiliki aksi diuretik.
Perpaduan
Sebagian besar nitrat diproduksi di tambang gurun di Chili. Ini dapat disintesis dengan beberapa reaksi:
NH4TIDAK3 (ac) +koh (ac) => nh3 (Ac) +kno3 (Ac)+h2Atau (l)
Kalium nitrat juga menetralkan asam nitrat dengan kalium hidroksida dalam reaksi yang sangat eksotermik.
Koh (ac) +hno3(conc) => kno3 (Ac) +h2Atau (l)
Pada skala industri, kalium nitrat diproduksi oleh reaksi perpindahan ganda.
Kakak3 (ac) +kcl (ac) => naCl (ac) +kno3 (AC)
Sumber utama KCL adalah dari Silvina Mineral, dan bukan mineral lain seperti Carnalite atau Cainite, yang juga terdiri dari magnesium ionik.
Sifat fisik dan kimia
Kalium nitrat dalam keadaan padat disajikan sebagai putih atau dalam bentuk kristal struktur ortorombik pada suhu sekitar, dan trigonal pada 129 ºC. Ini memiliki berat molekul 101.1032 g/mol, toilet dan memiliki rasa acre saline.
Ini adalah senyawa yang sangat larut dalam air (316-320 g/liter air, pada 20 ° C), karena sifat ioniknya dan kemudahan molekul air untuk menyelesaikan k ion k k+.
Kepadatannya adalah 2,1 g/cm3 pada 25 ºC. Ini berarti sekitar dua kali padat dari air.
Titik lelehnya (334 ºC) dan mendidih (400 ºC) menunjukkan ikatan ionik antara k+ dan tidak3-. Namun, mereka rendah dibandingkan dengan garam lain, karena energi reticular kristal lebih rendah untuk ion monovalen (yaitu, dengan beban ± 1), dan juga tidak memiliki ukuran yang sangat mirip.
Dapat melayani Anda: indikator pHIni terurai pada suhu yang dekat dengan titik didih (400 ° C) untuk menghasilkan kalium dan oksigen molekuler:
Kno3(S) => Kno2(S) + atau2(G)
Referensi
- Pubchem. (2018). Potasium nitrat. Pulih dari pubchem.NCBI.Nlm.Nik.Pemerintah
- Cryst Act. (2009). Pertumbuhan dan penyempurnaan kristal tunggal fase-III kalium nitrat, KNO3. B65, 659-663.
- Marni Wolfe. (3 Oktober 2017). Risiko kalium nitrat. Livestrong pulih.com
- Galeri Amethyst, Inc. (1995-2014). Niter mineral. Galeri pulih.com