Properti Nitrat, Struktur, Nomenklatur, Pelatihan
- 3262
- 880
- Herbert Fritsch
Itu Nitrat Mereka semua senyawa yang tidak mengandung anion3-, Ketika datang ke garam anorganik, atau kelompok nitro, -ono2, Dalam kasus turunan organik. Dalam anorganik, semua nitrat adalah garam logam atau ion amonium, di mana interaksi elektrostatik mendominasiN+TIDAK3-.
Misalnya, natrium nitrat3, Itu dibentuk oleh ion na+ dan tidak3-. Garam ini, bersama dengan kalium nitrat, kno3, adalah spesimen nitrat yang paling berlimpah. Nitrat menemukan di tanah, di jaringan tanaman, dan yang terpenting, di laut dan endapan saline seperti Salitre, yang terletak di Chili.
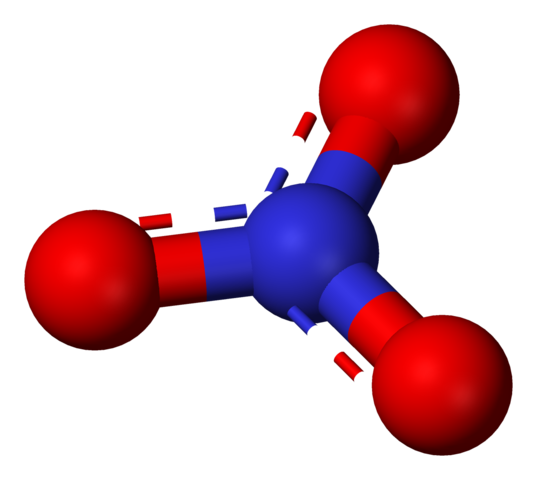
 Anion nitrat diwakili oleh model bola dan batang. Sumber: Benjah-BMM27 / Domain Publik.
Anion nitrat diwakili oleh model bola dan batang. Sumber: Benjah-BMM27 / Domain Publik. Istilah 'nitrat' segera menyinggung garam, pupuk dan bahan peledak. Mereka juga terkait dengan daging dan proses penyembuhannya untuk menghambat pertumbuhan bakteri dan dengan demikian menunda kemundurannya. Nitrat juga sinonim untuk sayuran, karena mengandung banyak garam ini.
dia tidak3- (gambar superior) adalah bentuk nitrogen yang paling teroksidasi, menjadi produk akhir dan asimilasi dari siklus biologisnya. Nitrogen atmosfer menderita beberapa transformasi, baik oleh pekerjaan sinar listrik atau melalui tindakan mikroba, menjadi NH4+ dan tidak3-, keduanya larut dalam air dan dapat diserap oleh tanaman.
Nitrat digunakan sebagai agen pengoksidasi, pupuk, bahan peledak dan obat kardiologis. Penggunaan terakhir ini sangat kontras dengan orang lain, karena mereka memetabolisme atau berinteraksi dengan tubuh sedemikian rupa sehingga mereka melebarkan pembuluh darah dan arteri; Dan karena itu, ada peningkatan dan peningkatan aliran darah, meringankan nyeri jantung.
[TOC]
Properti Nitrat
Kenetralan
Nitrat pada prinsipnya adalah zat netral, karena tidak3- Itu adalah basa terkonjugasi asam nitrat, hno3, Asam yang kuat. Di dalam air, tidak mungkin:
TIDAK3- + H2Atau ⇌ hno3 + Oh-
Faktanya, dapat dikatakan bahwa hidrolisis ini tidak terjadi sama sekali, jumlah OH yang tercela-. Oleh karena itu, larutan nitrat berair netral kecuali ada zat terlarut lainnya.
Penampilan fisik
Nitrat anorganik terdiri dari garam yang formulas umumnya adalah M (tidak3)N, makhluk N Itu adalah valencia atau beban positif dari kation logam. Semua nitrat ini memiliki kecerahan kristal dan memiliki warna keputihan. Namun, transisi logam nitrat bisa berwarna -warni.
Misalnya, tembaga nitrat (II) atau cupric nitrate, Cu (no3)2, Itu adalah padatan kristal kebiruan. Sementara itu, nikel nitrat (ii), atau (tidak3)2, Itu adalah warna zamrud yang solid. Beberapa nitrat lain, seperti besi, warna samar hadir.
Di sisi lain, nitrat organik biasanya merupakan padatan atau padatan yang sangat sensitif dan eksplosif.
Itu dapat melayani Anda: materi hidup: konsep, karakteristik dan contohDekomposisi termal
Nitrat logam sensitif terhadap suhu tinggi, karena mereka mulai rusak sesuai dengan persamaan kimia berikut:
2m (tidak3)2(s) → 2mo+4no2(g)+atau2(G)
Seperti yang diamati, logam nitrat terurai menjadi oksida, MO, dan nitrogen dan oksigen dioksida. Dekomposisi termal ini tidak terjadi pada suhu yang sama untuk semua nitrat; Beberapa menolak lebih dari yang lain.
Sebagai aturan umum, lebih kecil dan lebih kecil beban kation m adalah+, lebih besar akan menjadi suhu di mana nitrat harus dipanaskan untuk rusak. Sebaliknya, saat m+ Ini kecil atau memiliki beban positif yang besar, nitrat terurai pada suhu yang lebih rendah, oleh karena itu lebih tidak stabil.
Misalnya, natrium nitrat3, Ini terurai pada suhu yang lebih rendah dari barium nitrat, BA (tidak3)2, Yah, meskipun BA2+ memiliki beban yang lebih besar dari NA+, Ukurannya jauh lebih besar.
Agen pengoksidasi
dia tidak3- Itu adalah anion yang relatif stabil. Namun, atom nitrogennya sangat teroksidasi, dengan keadaan oksidasi +5 (n5+SALAH SATU32-), Jadi "haus" elektron. Untuk alasan ini, nitrat adalah zat pengoksidasi, yang akan berusaha merebut zat elektron di sekitarnya.
Kurangnya elektron dalam atom nitrogen NO3- Apa yang dilakukan Nano3 Dan Kno3 Agen pengoksidasi yang kuat, digunakan sebagai komponen bubuk mesiu. Menambah karakteristik ini fakta bahwa gas dilepaskan2 SAYA2 Saat membusuk, dipahami mengapa itu adalah bagian dari banyak bahan peledak.
Saat nitrat memperoleh elektron atau berkurang, itu dapat diubah menjadi amonia, NH3, atau dalam oksida nitrat, tidak, tergantung pada reagen dan kondisi.
Kelarutan
Semua nitrat anorganik, atau apa yang sama, logam dan amonium nitrat, NH4TIDAK3, Mereka adalah senyawa yang larut dalam air. Ini karena molekul air memiliki afinitas yang kuat untuk tidak3-, Dan bahwa jaringan kristal nitrat ini tidak terlalu stabil.
Struktur
Anion nitrat
 Struktur resonansi nitrat. Sumber: Benjah-BMM27 / Domain Publik.
Struktur resonansi nitrat. Sumber: Benjah-BMM27 / Domain Publik. Gambar atas menunjukkan struktur resonansi anion nitrat. Seperti dapat dilihat, dua muatan negatif terletak di dua atom oksigen, yang didemokalisasi antara tiga atom oksigen. Oleh karena itu, masing -masing atau memiliki beban -2/3, sedangkan nitrogen memiliki beban +1.
Jadi, tidak3- Interaksi secara elektrostatik, atau membentuk tautan koordinasi, melalui salah satu dari tiga atom oksigennya.
Padatan
Semua nitrat anorganik adalah saline dan ionik. Oleh karena itu, strukturnya kristal, yang berarti ionnya, m+ dan tidak3-, Mereka diatur di luar angkasa berkat interaksi elektrostatik mereka. Tergantung pada interaksi ini, kristal mereka akan menghadirkan struktur yang berbeda.
Dapat melayani Anda: apa itu belah ketupat keamanan dan untuk apa?Misalnya, struktur kristal Nano3 Itu trigonal atau rhomboédica, sedangkan dari kno3 Itu adalah ortorombik.
Nitrat organik
Nitrat organik diwakili dengan formula umum Rono2, dimana r adalah kelompok alkil atau aromatik. Senyawa ini ditandai dengan tautan R-Aon mereka2, dan biasanya terdiri dari turunan nitrat dari polimer dan zat organik lainnya.
Kompleks
dia tidak3- Itu berkoordinasi dengan pusat logam untuk membentuk tautan m+-ATAU TIDAK2-, menjadi interaksi yang berbeda dengan ionik. Kompleks ini pada dasarnya adalah sifat anorganik. Nitrat bahkan dapat dikoordinasikan menggunakan dua atom oksigennya secara bersamaan, m+-SALAH SATU2TIDAK.
Tata nama
Untuk menunjuk nitrat, kata -kata 'nitrat' diikuti dengan nama kation atau kelompok yang menyertainya dalam formula kimia masing -masing harus ditulis terlebih dahulu. Valencia kation ditentukan dalam tanda kurung saat memiliki lebih dari satu. Demikian juga, sufiks dapat digunakan -co dan -oy jika lebih disukai, mengikuti nomenklatur tradisional.
Misalnya, pertimbangkan iman (tidak3)3. Namanya Iron Nitrate (III), karena valensinya +3, atau juga dapat disebut ferric nitrate.
Aturan -aturan ini juga berlaku untuk nitrat organik, asalkan strukturnya sederhana. Misalnya, Cho3ATAU TIDAK2 Itu disebut metil nitrat, karena kelompok -ch3 Itu menjadi kelompok r yang menyertai -ono2.
Pelatihan
Alami
Nitrat terbentuk di alam sebagai bagian dari siklus biologis nitrogen. Karena itu, tanah, lautan, dan beberapa arus air memiliki jumlah nitrat yang signifikan. Bergantung pada ion di sekitarnya, garam nitrat yang berbeda akan dibentuk, menjadi nano3 Dan Kno3 Yang paling umum dan berlimpah.
Industri
Nitrat dibentuk pada skala industri dengan netralisasi asam nitrat, baik dengan logam hidroksida, alkohol, polimer, dll. Misalnya, kalsium nitrat, CA (tidak3)2, Ini dapat disiapkan sesuai dengan persamaan kimia berikut:
CA (OH)2 + 2hno3 → CA (Tidak3)2 + 2h2SALAH SATU
Demikian pula, beberapa zat organik diserang oleh HNO3 dalam kondisi tertentu untuk mempromosikan penggantian beberapa grup mereka oleh -ono2. Inilah yang terjadi dengan reaksi selulosa untuk berubah menjadi nitroselulosa atau selulosa nitrat, bahan polimer dan bahan peledak.
Fotokatalitik
Anion no3-, Dan karena itu nitrat anorganik, dapat dibentuk oleh aksi fotokatalitik limbah titanium oksida, paman2, menggunakan bahan baku yang tidak lebih dari nitrogen dan oksigen udara. Studi ini mengasumsikan bahwa di mana ada kelebihan pria2, akan ada jumlah no yang tidak diinginkan3-, yang mempengaruhi potabilitas air dan dapat mencakup ganggang.
Dapat melayani Anda: aldehydosAplikasi
Curing daging
 Sosis adalah salah satu daging olahan yang mengandung lebih banyak nitrat. Sumber: Pxhere.
Sosis adalah salah satu daging olahan yang mengandung lebih banyak nitrat. Sumber: Pxhere. Nitrat ditambahkan ke beberapa daging, terutama sosis, untuk menghilangkan bakteri dan dengan demikian menunda kemundurannya. Mereka juga bereaksi dengan protein mereka untuk memberi mereka warna yang lebih kemerahan. Masalah daging ini adalah bahwa, dengan memasaknya pada suhu tinggi, mereka menghasilkan nitrosoamina: senyawa yang terkait dengan kanker usus besar.
Reaksi ini sebagian dihindari jika ada vitamin yang ada, seperti halnya dengan sayuran, yang meskipun mereka kaya nitrat, tidak terkait dengan patologi karsinogenik.
Pertanian
Nitrat adalah sumber nitrogen yang larut. Oleh karena itu, itu berfungsi sebagai pupuk untuk menyumbangkan nitrogen untuk tanaman, dan dengan demikian, mendukung pertumbuhannya.
Obat
Nitrat memiliki fungsi khusus di dalam tubuh. Saat mengasimilasi dengan aksi enzimatik, itu direduksi menjadi nitrat oksida, tidak. Molekul ini menempati volume dan melebarkan vena dan arteri, memungkinkan ada aliran darah yang lebih besar. Oleh karena itu, nitrat digunakan sebagai obat untuk memerangi patologi sistem peredaran darah.
Ironis dan anehnya, untuk tujuan ini nitrat organik seperti gliserilo, nitrogliserin, isosorbid mononitrat dan pentaerithritol tetranitrate telah digunakan, semua kandidat yang baik di dunia bahan peledak.
Bahan peledak
Nitrat digunakan dalam formulasi eksplosif, bubuk mesiu menjadi contoh paling simbolis. Menjadi agen pengoksidasi, mereka mendukung pembakaran materi, selain berkontribusi pada ekspansi volume yang tiba -tiba karena pelepasan gas setelah membusuk.
Contoh nitrat
Di seluruh bagian sebelumnya lebih dari satu contoh nitrat telah disebutkan. Akhirnya, beberapa lainnya akan terdaftar bersama dengan formula dan nama masing -masing:
-Linen3: Lithium nitrat
-Rbno3: Rubidio nitrat
-Mg (tidak3)2: Magnesium nitrat
-SC (tidak3)2: Skandi Nitrat
-CR (tidak3)3: Chrome nitrat (III)
-Zn (tidak3)2: seng nitrat
-PB (tidak3)2: timbal nitrat (ii)
-Agno3: perak nitrat
-Ch3Ch2ATAU TIDAK2: Etil nitrat
-Ch3(Ch2)4ATAU TIDAK2: Amilo nitrat
Referensi
- Shiver & Atkins. (2008). Kimia anorganik. (Edisi keempat). MC Graw Hill.
- Carey f. (2008). Kimia organik. (Edisi Keenam). MC Graw Hill.
- Clark J. (5 Juni 2019). Stabilitas termal nitrat dan karbonat. Libretteks Kimia. Pulih dari: chem.Librettexts.org
- Wikipedia. (2020). Nitrat. Diperoleh dari: di.Wikipedia.org
- Angela Dowden. (12 Maret 2019). Kebenaran tentang nitrat dalam makanan Anda. Diperoleh dari: BBC.com
- Elsevier b.V. (2020). Nitrat. Ilmiah. Diperoleh dari: Scientedirect.com
- Kata. Biji s. & Prof. Govindan v. (26 April 2017). Peran nitrat organik dalam manajemen medis optimal angina. Masyarakat Kardiologi Eropa. Dipulihkan dari: Escardio.org
- Yuan, s., Chen, J., Lin, z. et al. (2013). Formasi nitrat dari nitrogen atmosfer dan oksigen difotokatalisasi oleh titanium dioksida nano. NAT COMMUN 4, 2249. doi.org/10.1038/ncomms3249
- « Dasar -dasar Terapi Naratif Michael White, Prosedur, Teknik
- Nomenklatur epoksi, memperoleh, aplikasi, contoh »

