Struktur Nitrobenzene (C6H5NO2), sifat, penggunaan, risiko
- 4675
- 954
- Domingo Gutkowski
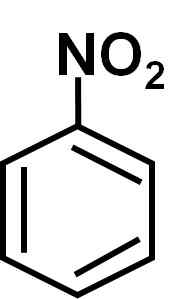
Dia nitrobenzene Ini adalah senyawa organik aromatik yang dibentuk oleh cincin benzenik C6H5- Dan grup nitro -tidak2. Formula kimianya adalah C6H5TIDAK2. Ini adalah cairan berminyak berwarna kuning pucat atau pucat, dengan aroma almond pahit atau sepatu untuk sepatu.
Nitobenzene adalah senyawa yang sangat berguna dalam industri kimia karena memungkinkan untuk mendapatkan serangkaian zat kimia yang memiliki berbagai penggunaan. Ini karena dapat mengalami berbagai jenis reaksi.
 Nitrobencene, c6H5-TIDAK2. Penulis: Marilú Stea.
Nitrobencene, c6H5-TIDAK2. Penulis: Marilú Stea. Di antara reaksi kimia yang penting adalah nitrasi (yang memungkinkan Anda untuk menambahkan lebih banyak grup -Tidak2 dengan molekul) dan reduksi (kebalikan dari oksidasi sebagai dua atom oksigen dari gugus nitro -No dihilangkan2 dan digantikan oleh hidrogen).
Dengan nitrobencene Anda dapat mempersiapkan misalnya anilin dan para-asetaminofenol. Yang terakhir adalah asetaminofen yang diketahui dengan baik yang merupakan antipletik (obat demam) dan analgesik lunak (obat nyeri minor).
Nitobenzene harus dimanipulasi dengan hati -hati karena menjengkelkan dan beracun, dapat menyebabkan jenis anemia, di antara beberapa gejala, dan diyakini bahwa itu dapat menyebabkan kanker. Itu juga berbahaya bagi lingkungan.
[TOC]
Struktur
Nitrobenzene c6H5-TIDAK2 Ini adalah molekul datar yang dibentuk oleh cincin benzenik C6H5- ke mana grup nitro ditautkan -tidak2. Molekulnya datar karena ada interaksi elektronik antara kelompok nitro -tidak2 dan cincin benzena.
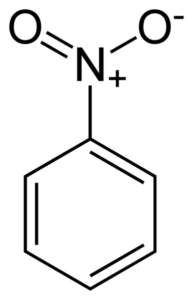 Struktur datar molekul nitrobenzena. Elektron dari tautan cincin Bondyan rangkap cenderung berinteraksi dengan kelompok nitro -tidak2. Penulis: Benjah-BMM27. Sumber: Wikimedia Commons.
Struktur datar molekul nitrobenzena. Elektron dari tautan cincin Bondyan rangkap cenderung berinteraksi dengan kelompok nitro -tidak2. Penulis: Benjah-BMM27. Sumber: Wikimedia Commons. Grup nitro -tidak2 cenderung menarik elektron cincin benzenik c6H5-.
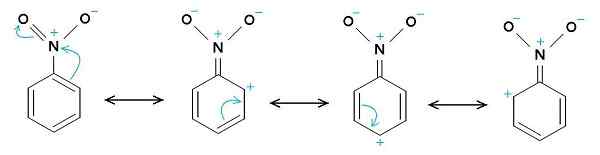 Struktur resonansi nitrobenzene. Cincin benzena cenderung memiliki beban positif, sedangkan kelompok nitro -no2 cenderung memiliki beban negatif. Pengunggah asli adalah Samuele Madini di Italia Wikipedia. [Area publik]. Sumber: Wikimedia Commons.
Struktur resonansi nitrobenzene. Cincin benzena cenderung memiliki beban positif, sedangkan kelompok nitro -no2 cenderung memiliki beban negatif. Pengunggah asli adalah Samuele Madini di Italia Wikipedia. [Area publik]. Sumber: Wikimedia Commons. Itulah sebabnya molekul memiliki sisi yang sedikit lebih negatif (di mana oksigen -tidak ada2) dan sisi yang sedikit lebih positif (cincin benzena).
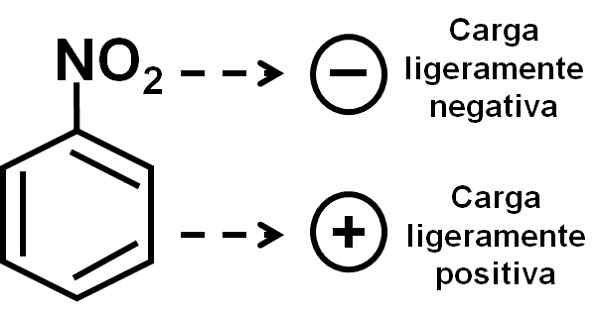 Oksigen dari kelompok nitro memiliki beban yang sedikit negatif dibandingkan dengan cincin benzenik. Penulis: Marilú Stea.
Oksigen dari kelompok nitro memiliki beban yang sedikit negatif dibandingkan dengan cincin benzenik. Penulis: Marilú Stea. Tata nama
- Nitrobenzene.
- Nitrobenze.
- Nitrobenzole.
- Minyak atau esensi mirbano atau mirbana (istilah bekas).
Properti
Keadaan fisik
Cairan berminyak berwarna -warni menjadi kuning pucat.
Berat molekul
123.11 g/mol.
Titik lebur
5.7 ºC.
Titik didih
211 ºC.
Itu dapat melayani Anda: kobalt klorida (cocl2 (: struktur, nomenklatur, sifatTitik nyala
88 ºC (metode cangkir tertutup).
Suhu self -rection
480 ° C.
Kepadatan
1.2037 g/cm3 pada 20 ºC.
Kelarutan
Little Water Soluble: 0,19 g/100 g air pada 20 ° C. Benar -benar larut dengan alkohol, benzena dan dialyl eter.
Sifat kimia
Nitrobencene stabil hingga sekitar 450 ° C suhu di mana ia mulai membusuk pembentukan (tanpa adanya oksigen) tidak, tidak2, Benzene, Biphenyl, Aniline, Dibenzofurano dan Naphthalene.
Di antara reaksi penting nitrobencene adalah pengurangan, nitrasi, halogenasi dan sulfonasi.
Nitrobenzene Nitration awalnya menghasilkan meta-nitrobenzene dan dengan waktu reaksi yang lama, 1,3,5-nitobenzene diperoleh.
Bereaksi bromin atau klorin dengan nitrobenzena dengan adanya katalis yang sesuai diperoleh 3-bromo-nitrobenzene (meta-bromonitrobencene) atau 3-cllor-nitrobenzene (meta-chloronitrobenzene)).
Contoh reduksi adalah bahwa ketika berhadapan dengan timah (SN) dalam asam klorida (HCl), meta-halogenonitobenzen diperoleh dengan meta-halogenoanilin.
Sulfonasi nitrobenzene dilakukan dengan merokok asam sulfat pada 70-80 ° C dan produknya adalah meta-nitrobenzeulfonic meta-nitrobenze. Ini dapat dikurangi dengan zat besi dan HCl untuk memberikan asam metanil.
Formasi dimmer
Dalam solusi benzena c6H6 Molekul nitrobencene dikaitkan satu sama lain dengan pasangan yang membentuk diameter atau pasangan molekul. Pada pasangan ini, salah satu molekul berada dalam posisi terbalik sehubungan dengan yang lain.
Pembentukan diameter nitrobenzene dengan molekul satu dalam posisi terbalik sehubungan dengan yang lain mungkin disebabkan oleh fakta bahwa masing -masing dari mereka memiliki sisi yang sedikit lebih positif dan sisi yang berlawanan dengan beban yang sedikit lebih negatif lebih negatif.
Di dimer sisi dengan beban yang sedikit lebih positif dari salah satu molekul mungkin terletak dekat dengan beban yang sedikit negatif dari molekul lainnya, karena beban yang berlawanan tertarik, dan karenanya terjadi dengan dua sisi lainnya.
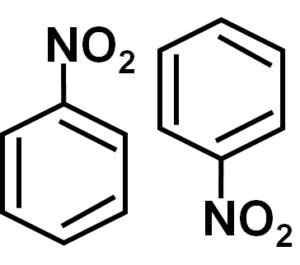 Jumlah nitrobencene, yaitu, dua molekul yang cenderung bersama dalam beberapa pelarut. Penulis: Marilú Stea.
Jumlah nitrobencene, yaitu, dua molekul yang cenderung bersama dalam beberapa pelarut. Penulis: Marilú Stea. Properti lainnya
Itu menyajikan bau yang mirip dengan almond atau untuk memoles sepatu. Dengan menurunkan suhu yang kokoh dalam bentuk kristal kuning kehijauan.
Memperoleh
Anda merawat benzena C6H6 Dengan campuran asam nitrat HNO3 dan asam sulfat h2Sw4. Proses ini disebut nitrasi dan melibatkan pembentukan ion nitronium tidak2+ Berkat adanya asam sulfat h2Sw4.
- Nitronio ion no2+:
Hno3 + 2 h2Sw4 ⇔ h3SALAH SATU+ + 2 hso4- + TIDAK2+ (Nitronio ion)
- Nitronio Ion menyerang benzena:
Dapat melayani Anda: Kesalahan sistematis: Cara menghitungnya, dalam kimia, dalam fisika, contohC6H6 + TIDAK2+ → c6H6TIDAK2+
- Nitrobencene terbentuk:
C6H6TIDAK2+ + Hso4- → c6H5TIDAK2 + H2Sw4
Kesimpulan:
C6H6 + Hno3 → c6H5TIDAK2 + H2SALAH SATU
Reaksi nitrasi benzena sangat eksotermik, yaitu, sangat panas dihasilkan, jadi sangat berbahaya.
Aplikasi
Dalam memperoleh anilin dan asetaminofen
Nitrobencene terutama digunakan untuk mensintesis anilin C6H5NH2, yang merupakan senyawa yang banyak digunakan untuk persiapan pestisida, gusi, pewarna, bahan peledak dan obat -obatan.
Memperoleh anilin terjadi dengan mengurangi nitrobenzene dalam medium asam di hadapan zat besi atau timah, yang dilakukan sesuai dengan langkah -langkah berikut:
Nitrobenzene → Nitrosobenzene → Phenylhydroxylamine → Anilin
C6H5TIDAK2 → c6H5Tidak → c6H5NHOH → C6H5NH2
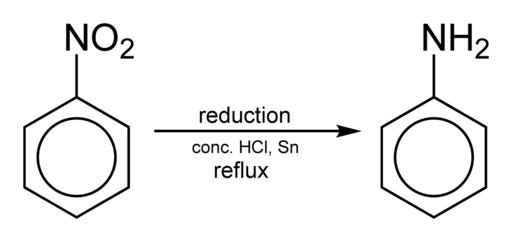 Pengurangan nitrobencene untuk mendapatkan anilin. Benjah-BMM27 [Domain Publik]. Sumber: Wikimedia Commons.
Pengurangan nitrobencene untuk mendapatkan anilin. Benjah-BMM27 [Domain Publik]. Sumber: Wikimedia Commons. Bergantung pada kondisinya, prosesnya dapat dihentikan dalam salah satu langkah perantara misalnya dalam fenilhidroksilamin. Mulai dari phenylhydroxylamine dalam lingkungan yang sangat asam, para-aminofenol dapat disiapkan:
Phenylhdroxylamine → P-Aminofenol
C6H5NHOH → Hoc6H4NH2
Yang terakhir ini diobati dengan anhidrida asetat untuk mendapatkan parasetamol (acetaminophen) analgesik antipletik dan lunak yang lembut, yaitu obat untuk mengobati demam dan rasa sakit dan rasa sakit dan nyeri dan rasa sakit dan rasa sakit dan nyeri dan rasa sakit.
 Terkadang dimungkinkan untuk mengobati dengan acetaminophen untuk anak -anak dengan demam. Asetaminofen adalah turunan nitrobenzene. Penulis: Augusto Ordonez. Sumber: Pixabay.
Terkadang dimungkinkan untuk mengobati dengan acetaminophen untuk anak -anak dengan demam. Asetaminofen adalah turunan nitrobenzene. Penulis: Augusto Ordonez. Sumber: Pixabay.  Pil asetaminofen, turunan nitrobenzene. Parasetamol_acetaminophen_500_mg_pils.JPG: Suku Michelle dari Ottawa, Canadaderivative Work: Anrie [CC oleh (https: // CreativeCommons.Org/lisensi/oleh/3.0)]. Sumber: Wikimedia Commons.
Pil asetaminofen, turunan nitrobenzene. Parasetamol_acetaminophen_500_mg_pils.JPG: Suku Michelle dari Ottawa, Canadaderivative Work: Anrie [CC oleh (https: // CreativeCommons.Org/lisensi/oleh/3.0)]. Sumber: Wikimedia Commons. Cara lain untuk mendapatkan anilin adalah dengan mengurangi nitrobenzene dengan karbon monoksida (CO) dalam media berair di hadapan partikel yang sangat kecil (nanopartikel) paladium (PD) sebagai katalis sebagai katalis sebagai.
C6H5-TIDAK2 + 3 Co + H2O → c6H5-NH2 + 3 co2
Dalam memperoleh senyawa kimia lainnya
Nitobenzene adalah titik awal untuk mendapatkan berbagai macam senyawa yang digunakan seperti pewarna, pestisida, obat -obatan dan kosmetik.
 Beberapa pewarna diperoleh berkat nitrobenzene. Penulis: Edith Lüthi. Sumber: Pixabay.
Beberapa pewarna diperoleh berkat nitrobenzene. Penulis: Edith Lüthi. Sumber: Pixabay. Misalnya, ini memungkinkan untuk mendapatkan 1,3-dinitrobencene bahwa dengan klorinasi (penambahan klorin) dan reduksi (eliminasi atom oksigen) menghasilkan 3-kloroanilin. Ini digunakan sebagai perantara untuk pestisida, pewarna dan obat -obatan.
Nitobenzene digunakan untuk menyiapkan benchidine yang merupakan pewarna. Selain itu, nitrobenzene berfungsi untuk menyiapkan quinoline, azobenzene, asam metanil, dyitobenzene, isokianat atau piroksilin di antara banyak senyawa lainnya.
Dalam beberapa aplikasi
Nitobenzene digunakan atau digunakan sebagai:
Dapat melayani Anda: hidrokarbon tak jenuh- Pelarut ekstraksi untuk pemurnian minyak pelumas yang digunakan dalam mesin
- Pelarut untuk eter selulosa
- Bahan campuran untuk memoles logam
- Dalam sabun
- Dalam campuran untuk sepatu Polandia
- Konservator cat semprot
- Komponen campuran pemolesan lantai
- Pengganti Essence Almond
- Di industri parfum
- Dalam produksi karet sintetis
- Pelarut dalam berbagai proses
 Nitobenzene adalah bagian dari beberapa campuran untuk memoles sepatu. D-Kuru [CC BY-SA 3.0 at (https: // createveCommons.Org/lisensi/by-sa/3.0/at/deed.di dalam)]. Sumber: Wikimedia Commons.
Nitobenzene adalah bagian dari beberapa campuran untuk memoles sepatu. D-Kuru [CC BY-SA 3.0 at (https: // createveCommons.Org/lisensi/by-sa/3.0/at/deed.di dalam)]. Sumber: Wikimedia Commons. Risiko
Nitobenzene beracun dengan inhalasi, konsumsi dan penyerapan melalui kulit.
Mengiritasi kulit, mata, dan saluran pernapasan. Ini dapat menyebabkan jenis anemia yang disebut methemoglobinemia yang terdiri dalam mengurangi kemampuan sel darah merah untuk melepaskan oksigen dalam jaringan dan menghasilkan kelelahan.
Selain itu, nitrobencene menyebabkan dispnea, pusing, penglihatan kesal, kurangnya napas, runtuh dan kematian. Ini juga merusak sistem hati, limpa, ginjal dan saraf pusat.
Diperkirakan itu bisa menjadi mutagen dan mungkin menyebabkan kanker manusia, karena telah menyebabkannya pada hewan.
Juga nitrobencene tidak boleh dibuang di lingkungan. Toksisitasnya terhadap hewan, tumbuhan dan mikroorganisme membuatnya sangat berbahaya bagi ekosistem.
Toksisitas terhadap mikroorganisme mengurangi biodegradabilitasnya.
Perawatan untuk penghapusan lingkungannya
Polusi lingkungan dengan nitrobencene dapat terjadi melalui pemborosan berbagai industri yang menggunakannya, seperti industri mewarnai atau bahan peledak.
Nitobenzene adalah yang sangat beracun dan sulit untuk dirusak dalam kondisi alami, karena alasan ini dapat menyebabkan kontaminasi yang dapat diminum dan menabur sistem irigasi.
Karena stabilitas dan toksisitasnya yang tinggi terhadap mikroorganisme, ia sering dipilih sebagai model dalam studi pengolahan limbah.
Berbagai cara sedang diselidiki untuk menghilangkan nitrobenzene air yang terkontaminasi. Salah satunya adalah melalui degradasi fotokatalitik, yaitu, menggunakan sinar matahari sebagai akselerator reaksi degradasi di hadapan titanium dioksida titanium2.
 Dengan reaktor sinar matahari, dimungkinkan untuk menghilangkan polusi air dengan nitrobencene. Mihai-Cosmin Pascariu [CC BY-SA (https: // CreativeCommons.Org/lisensi/by-sa/4.0)]. Sumber: Wikimedia Commons.
Dengan reaktor sinar matahari, dimungkinkan untuk menghilangkan polusi air dengan nitrobencene. Mihai-Cosmin Pascariu [CC BY-SA (https: // CreativeCommons.Org/lisensi/by-sa/4.0)]. Sumber: Wikimedia Commons. Metode mikroelektrolisis juga telah berhasil diuji dengan katalis besi (iman) dan tembaga (Cu) dalam keramik. Mikroelektrolisis memungkinkan nitrobenzene untuk menguraikan melalui arus listrik.
Referensi
- ATAU.S. Perpustakaan Kedokteran Nasional. (2019). Nitrobenzene. Pulih dari pubchem.NCBI.Nlm.Nih.Pemerintah.
- Morrison, r.T. dan Boyd, R.N. (2002). Kimia organik. Edisi ke -6. Prentice-Hall.
- Moldoveanu, s.C. (2019). Pirolisis senyawa hitungan nitrogen lainnya. Dalam pirolisis molekul organik (edisi kedua). Pulih dari scientedirect.com.
- Smith, hlm.W.G. et al. (1969). Senyawa nitrasi-nitro aromatik. Substitusi elektrofilik. Dalam kimia aromatik. Pulih dari scientedirect.com.
- Windholz, m. et al. (Editor) (1983). Indeks Merck. Eneritedia bahan kimia, obat -obatan, dan biologis. Edisi kesepuluh. Merck & Co., Inc.
- Ensiklopedia Kimia Industri Ullmann. (1990). Edisi Kelima. Volume A22. Vch verlagsgellschaft mbh.
- Whang, t.-J. et al. (2012). Degradasi fotokatalitik nitrobenzene UV oleh Titania mengikat pada tabung kuarsa. International Journal of Photoenergy, Volume 2012, Artikel ID 681941. Hyndawi pulih.com.
- Shikata, t. et al. (2014). Pembentukan dimer anti-paralel nitrobenzena dalam pelarut non-polar. AIP Advances 4, 067130 (2014). Pulih dari doaj.org.
- Krogul-Obczak, a. et al. (2019). Pengurangan nitrobenzene menjadi anilin oleh CO/H2Atau sebagai saksi nanopartikel paladium. Catalysts 2019, 9, 404. MDPI pulih.com.
- Yang, b. et al. (2019). Produksi skala percontohan, sifat dan penerapan Fe/Cu Catalytic-Ceramic-Filler untuk Senyawa Nitrobenzene Pengolahan Air Limbah. Catalysts 2019, 9, 11. MDPI pulih.com.
- « Formula Keuntungan Mekanik, Persamaan, Perhitungan dan Contoh
- 110 frasa cinta abadi untuk pacar dan suami »

