Struktur Kimia Pencanona, Properti, Sintesis, Penggunaan
- 829
- 101
- Joseph Nader PhD
Itu Pentanona Itu adalah senyawa organik, milik keluarga keton, yang formulanya kimia c5H10SALAH SATU. Itu tetap menjadi salah satu keton yang paling sederhana, dan terdiri dari cairan tidak berwarna dengan aroma yang mirip dengan aseton. Dari sana mulai sekarang, sehubungan dengan jumlah karbon kerangka mereka, keton menyajikan isomer posisi.
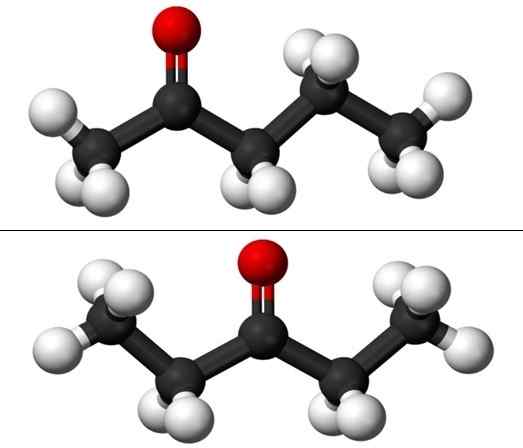
Saat berbicara tentang posisi isomeria mengacu pada di mana kelompok karbonil berada, c = o. Dengan demikian, Puntanona sebenarnya terdiri dari dua senyawa dengan sifat fisik yang berbeda hampir satu sama lain: 2-penon dan 3-penon (gambar bawah). Keduanya cair, tetapi titik didihnya sama, sehingga mereka tidak dapat dipisahkan dengan distilasi.
 Molekul dari Posisi Isomer untuk Pentanona. Sumber: Jynto & Ben Mills via Wikipedia.
Molekul dari Posisi Isomer untuk Pentanona. Sumber: Jynto & Ben Mills via Wikipedia. Namun, masing -masing dari dua pentanon memiliki rute sintesisnya sendiri, sehingga tidak mungkin ada campuran dari mereka; campuran yang mungkin layak untuk dipisahkan dengan membekukan.
Penggunaannya dibatasi terutama sebagai pelarut organik; Alternatif untuk aseton di media di mana Anda bekerja dengan suhu yang lebih tinggi dari titik didihnya yang rendah. Mereka juga merupakan bahan pemula untuk sintesis organik lainnya, karena kelompok C = O mereka dapat mengurangi atau menderita penambahan nukleofilik.
[TOC]
Struktur kimia
Posisi isomer
Dalam gambar kami memiliki struktur molekuler dari dua isomer posisi untuk Puntanona, diwakili oleh model bola dan batang. Bola hitam sesuai dengan kerangka berkarbonasi, atom putih hingga hidrogen, dan atom oksigen merah pada kelompok C = O.
2-Pintanone
2-Ponanona (di atas) memiliki kelompok C = atau dalam karbon kedua, yang setara dengan jika ada di dalam ruangan; Artinya, 2-Ponanona dan 4-Pantanona setara, karena cukup untuk memutar mereka 180º sehingga struktur mereka sama.
Dapat melayani Anda: karbon tetrachloride (CCL4)Di sebelah kiri c = o Anda memiliki radikal metil, cho3-, Dan di sebelah kanannya, propil radikal. Itulah sebabnya Cetona ini juga menerima nama (kurang digunakan) dari Metil Propil Cetona (MPK dalam Bahasa Inggris). Anda dapat melihat asimetri struktur ini pada pandangan pertama.
3-penon
3-péntanona (di bawah) memiliki grup c = o dalam karbon ketiga. Perhatikan bahwa isomer ini adalah versi aseton yang lebih besar, dan juga sangat simetris; Dua radikal di sisi kelompok C = O adalah sama: dua radikal etil, ch3Ch2-. Itulah sebabnya 3-pananona juga disebut Cetona Diestil (atau Dimethyl Acetone).
Interaksi antarmolekul
Kehadiran kelompok karbonil, baik di 2-pantanone dan di 3-penon, memberikan polaritas kepada molekul.
Oleh karena itu, kedua isomer pentanona mampu berinteraksi satu sama lain melalui dipol-dipol.
Demikian juga, kekuatan dispersi London antara karbon dan kerangka terhidrogenasi campur tangan ke tingkat yang lebih rendah.
Dengan memiliki Puntanona, area molekul yang lebih besar dan massa dibandingkan dengan aseton, kontribusi ini menambah momen dipolnya dan memungkinkan titik didih yang lebih tinggi (102 ºC> 56 ºC) untuk memiliki titik didih yang lebih tinggi). Bahkan, kedua isomer menguap pada 102 ºC; sementara mereka membeku pada suhu yang berbeda.
Kristal
Mungkin dalam kristalisasi simetri memainkan peran penting. Misalnya, titik fusi 2 -pantanona adalah -78 ºC, sedangkan 3 -péntanona, -39 ºC.
Dapat melayani Anda: Hukum AvogadroIni berarti bahwa kristal 3-Pantanona lebih stabil terhadap suhu; Molekulnya lebih kohesif dan membutuhkan lebih banyak panas untuk terpisah dalam fase cair.
Jika ada campuran kedua isomer, 3-penon akan menjadi yang pertama mengkristal, akhirnya menjadi 2-pananona pada suhu yang lebih rendah. Molekul-molekul 3-pantanon, lebih simetris, lebih mudah diorientasikan daripada 2-ponanona: asimetris dan pada saat yang sama lebih dinamis.
Properti
Penampilan fisik
Cairan tidak berwarna dengan aroma yang mirip dengan aseton.
Masa molar
86.13 g/mol
Kepadatan
0,81 g/ml (3-ponanona)
0,809 g/ml (2-Ponanona)
Titik lebur
-78 ºC (2-Ponanona)
-39 ºC (3-Ponanona)
Titik didih
102 ºC (untuk kedua isomer)
Kelarutan air
35 g/l (3-ponenona)
60 g/l (2-ponenona)
Tekanan uap
35 mmHg (3-ponenona)
270 mmHg (2-pantanon) pada 20 ºC
Nilai -nilai ini tidak berguna untuk secara langsung membandingkan tekanan uap dari kedua isomer, karena yang pertama dilaporkan tanpa suhu di mana ia diukur.
Titik nyala
12.78 ºC (3-Ponanona)
10 ºC (2-Ponanona)
Stabilitas
Dua isomer pentanona sangat mudah terbakar, jadi mereka harus tetap jauh dari sumber panas mana pun. Titik nyala menunjukkan bahwa nyala api dapat mengatur uap kedua pentanas bahkan pada suhu 10 ºC.
Perpaduan
Meskipun dua isomer pentanona secara fisik dan kimia sangat mirip, rute sintetis mereka tidak tergantung pada yang lain, sehingga tidak mungkin keduanya diperoleh dalam sintesis yang sama.
2-Pintanone
Mulai dari reagen 2-penol, alkohol sekunder, ini dapat dioksidasi menjadi 2-ponanon menggunakan asam hipoklor yang terbentuk di situ, HCLO, sebagai agen pengoksidasi. Oksidasi adalah:
Itu dapat melayani Anda: tidak ada elektrolit: karakteristik dan contoh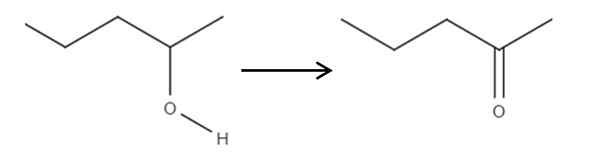 Oksidasi 2-pantanol di 2-pantanona. Sumber: Gabriel Bolívar.
Oksidasi 2-pantanol di 2-pantanona. Sumber: Gabriel Bolívar. Cukup tautan c-oh menjadi c = o. Ada metode lain untuk mensintesis 2 penon, tetapi ini adalah yang paling sederhana untuk dipahami.
3-penon
3-Pintanon dapat disintesis dengan cara3Ch2Cooh. Rute sintetis ini menghasilkan keton simetris, dan merupakan molekul cho3COOH akan kehilangan kelompok COOH dalam bentuk CO2, Sementara yang lain grup Anda oh dalam bentuk h2SALAH SATU:
2ch3Ch2Cooh => ch3Ch2Coch2Ch3 + BERSAMA2 + H2SALAH SATU
Rute lain yang sedikit lebih kompleks adalah bereaksi langsung campuran etilen, cho2= Ch2, BERSAMA2 dan H2 Untuk membentuk 3-ponanona.
Aplikasi
Kecuali aplikasi ini sangat ketat, itu adalah sintesis spesifik, atau juga telah ditunjukkan bahwa kedua isomer tidak menyebabkan hasil yang sama, tidak relevan untuk memilih antara menggunakan 2-penon atau 3-penon dalam salah satu dari itu penggunaan.
Yaitu, "tidak masalah" jika Anda ingin menggunakan 2-ponanona atau 3-penon sebagai pelarut lukisan atau resin, atau sebagai sengsara, karena kriteria yang paling penting akan menjadi harga dan ketersediaannya. 3-penon digunakan dalam industri otomotif untuk mempelajari perilaku gas di dalam mesin pembakaran internal.
Referensi
- Morrison, r. T. dan boyd, r, n. (1987). Kimia organik. Edisi ke -5. Editorial Addison-Wesley Inter-American.
- Carey f. (2008). Kimia organik. (Edisi Keenam). MC Graw Hill.
- Graham Solomons t.W., Craig b. Fryhle. (2011). Kimia organik. Amina. (Edisi ke -10.). Wiley Plus.
- Wikipedia. (2019). 3-sakit. Diperoleh dari: di.Wikipedia.org
- Pusat Nasional Informasi Bioteknologi. (2019). 2-pontenone. Database pubchem. CID = 7895. Pulih dari: pubchem.NCBI.Nlm.Nih.Pemerintah
- Royal Society of Chemistry. (2019). 3-sakit. Pulih dari: chemspider.com
- Profesor T. Nalli. (2013). Oksidasi 2-Pintanol dan Distilasi Produk. Pulih dari: kursus1.Winona.Edu

