Ester
- 3053
- 833
- Joseph Nader PhD
 Ester adalah senyawa organik yang memiliki komponen asam karboksilat dan alkohol lainnya
Ester adalah senyawa organik yang memiliki komponen asam karboksilat dan alkohol lainnya Apa itu ester?
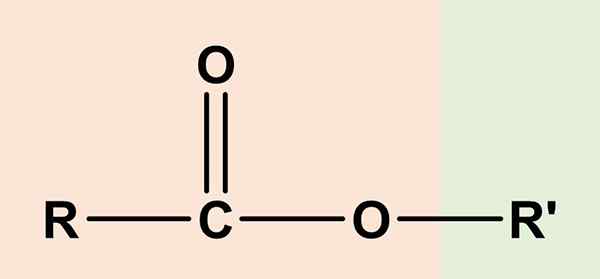
Itu ester Mereka adalah senyawa organik yang memiliki komponen asam karboksilat dan alkohol lainnya. Formula kimianya yang umum adalah RCO2R' atau rcoor'. Sisi kanan, rcoo, sesuai dengan kelompok karboksil, sedangkan kanan, atau' Itu alkohol. Keduanya berbagi atom oksigen dan berbagi kesamaan tertentu dengan eter (ROR ').
Karena alasan ini asetat etil, ch3Cooch2Ch3, Ester yang paling sederhana, dianggap sebagai Eter asam asetat atau cuka, Dan dari sana asal etimologis nama 'ester'. Sehingga ester terdiri dari penggantian hidrogen asam dari gugus COOH, dengan sewa alkohol dari alkohol.
Dimana esternya?
Dari tanah kimia organik, ada banyak sumber alami. Bau buah -buahan yang menyenangkan, seperti pisang, pir dan apel, adalah produk dari interaksi ester dengan banyak komponen lainnya. Mereka juga ditemukan dalam bentuk trigliserida dalam minyak atau lemak.
Tubuh kita memproduksi trigliserida dari asam lemak, yang memiliki rantai berkarbonasi panjang, dan alkohol gliserol. Apa yang membedakan beberapa ester dari yang lain terletak baik di R, rantai komponen asam, seperti pada R ', komponen alkoholik.
Ester berat molekul rendah harus memiliki beberapa karbon di R dan R ', sementara yang lain, seperti lilin, memiliki banyak karbon terutama di R', komponen alkohol, dan karenanya berat molekul tinggi.
Namun, tidak semua ester benar -benar organik. Jika atom kelompok karbon dari kelompok karbonil digantikan oleh salah satu fosfor, maka rpoor akan memiliki '. Ini dikenal sebagai ester fosfat, dan sangat penting dalam struktur DNA.
Dengan demikian, setiap kali atom dapat dihubungkan secara efisien dengan karbon atau oksigen, seperti sulfur (rsoor '), akibatnya dapat membentuk ester anorganik.
Properti estres
Ester bukan asam atau alkohol, jadi mereka tidak berperilaku seperti itu. Titik meleleh dan mendidih, misalnya, lebih rendah dari yang memiliki bobot molekul yang sama, tetapi lebih dekat dengan nilai dengan nilai -nilai aldehida dan keton.
Asam butanoat, cho3Ch2Ch2Cooh, memiliki titik didih 164º C, sedangkan etil asetat, ch3Cooch2Ch3, dari 77.1 c.
Terlepas dari contoh baru-baru ini, titik didih 2-metilbutane3Ch (ch3) Ch2Ch3, Metil asetat, cho3Cooch3, dan 2-butanol, cho3,Ch (oh) ch2Ch3, Mereka adalah sebagai berikut: 28, 57 dan 99º C. Tiga senyawa memiliki berat molekul 72 dan 74 g/mol.
Ester peso molekul rendah cenderung volatil dan memiliki bau yang menyenangkan, itulah sebabnya konten mereka dalam buah -buahan memberi mereka wewangian keluarga mereka. Di sisi lain, ketika bobot molekulnya tinggi, mereka adalah padatan kristal yang tidak berwarna dan tidak berbau, atau tergantung pada strukturnya, mereka dapat menunjukkan karakteristik berlemak.
Kelarutan air
Asam dan alkohol karboksilat biasanya larut dalam air, kecuali jika mereka memiliki karakter hidrofobik yang tinggi dalam struktur molekulnya. Hal yang sama berlaku untuk ester. Ketika R atau R 'adalah rantai pendek, ester dapat berinteraksi dengan molekul air melalui dipol-dipolo dan kekuatan pasukan London.
Dapat melayani Anda: senyawa kimiaIni karena ester adalah akseptor jembatan hidrogen. Sebagai? Untuk dua atom oksigen rcoor '. Molekul air dapat membentuk jembatan hidrogen dengan oksigen ini. Tetapi ketika rantai R atau R sangat panjang, mereka mengusir air di lingkungan mereka, sehingga tidak mungkin untuk pembubaran mereka.
Contoh yang jelas terjadi dengan ester trigliserid. Rantai samping mereka panjang dan membuat minyak dan lemak tidak larut di dalam air, kecuali jika mereka bersentuhan dengan pelarut yang kurang polar, lebih terkait dengan rantai ini.
Reaksi hidrolisis
Ester juga dapat bereaksi dengan molekul air dalam apa yang dikenal sebagai reaksi hidrolisis. Namun, mereka membutuhkan asam atau lingkungan basa untuk mempromosikan mekanisme reaksi tersebut:
Rcoor ' + H2SALAH SATU RcoOh + R'oH
(Setengah asam)
Molekul air ditambahkan ke kelompok karbonil, c = o. Hidrolisis asam dirangkum dalam penggantian masing -masing r 'komponen alkohol dengan air dari air. Perhatikan juga bagaimana ester "pecah" dalam dua komponennya: asam karboksilat, alkohol rcooh dan r'oh.
Rcoor ' + Oh- => RcoSALAH SATU- + R'oH
(Media dasar)
Saat hidrolisis dilakukan dalam media dasar, reaksi ireversibel terjadi yang dikenal sebagai saponifikasi. Ini sangat dipekerjakan dan merupakan landasan dalam elaborasi sabun artisanal atau industri.
Rcoo- Itu adalah anion karboksilat, stabil, yang terkait secara elektrostatik dengan kation dominan di tengah.
Jika dasar yang digunakan adalah NaOH, garam terbentuk. Saat ester adalah trigliserida, yang menurut definisi memiliki tiga rantai sisi R, tiga garam asam lemak, rcoone, dan alkohol gliserol terbentuk.
Reaksi reduksi
Ester adalah senyawa yang sangat teroksidasi. Itu berarti memiliki beberapa ikatan kovalen dengan oksigen. Dengan menghilangkan ikatan C-O, terjadi istirahat yang akhirnya memisahkan komponen asam dan alkohol; Dan bahkan lebih lagi, asam dikurangi menjadi cara yang kurang teroksidasi, menjadi alkohol:
Rcoor '=> rch2Oh + r'oh
Ini adalah reaksi reduksi. Diperlukan zat pereduksi yang kuat, seperti lithium dan aluminium hidrida, lialh4, dan dari media asam yang mempromosikan migrasi elektron. Alkohol adalah bentuk terkecil, yaitu, yang memiliki ikatan kovalen lebih sedikit dengan oksigen (hanya satu: c-oh).
Dua alkohol, RCH2Oh + r'oh, berasal dari dua rantai masing -masing ester rcoor asli '. Ini adalah metode sintesis alkohol yang ditambahkan nilai dari esternya.
Misalnya, jika Anda ingin memproduksi alkohol ester eksotis, ini akan menjadi rute yang baik untuk tujuan itu.
Reaksi transerifikasi
Ester dapat diubah menjadi orang lain jika mereka bereaksi menjadi media asam atau basa dengan alkohol:
Rcoor ' + R "Oh RcoAtau " + R'oH
Struktur ester
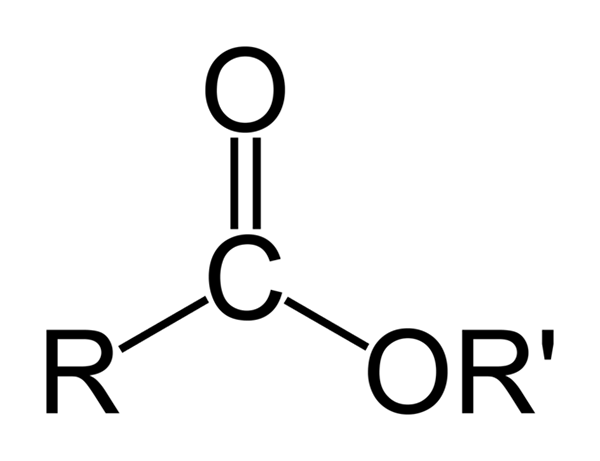 Struktur Kimia Umum Ester Organik. Sumber: Ben Mills via Wikipedia
Struktur Kimia Umum Ester Organik. Sumber: Ben Mills via Wikipedia Gambar superior mewakili struktur umum semua ester organik. Perhatikan bahwa r, grup karbonil c = o, dan atau ', membentuk segitiga datar, produk hibridisasi SP2 atom karbon pusat. Namun, atom lain dapat mengadopsi geometri lain, dan strukturnya tergantung pada sifat intrinsik r atau r '.
Dapat melayani Anda: nitrat: properti, struktur, nomenklatur, pelatihanJika R atau R 'adalah rantai alqulicas sederhana, misalnya, dari jenisnya (pilih2)NCh3, Anda akan melihat Zigzagueada di luar angkasa. Ini adalah kasus Pentilo Butanoat3Ch2Ch2Cooch2Ch2Ch2Ch2Ch3.
Tetapi di salah satu karbon dari rantai tersebut, cabang atau tidak jenuh dapat ditemukan (C = C, CHC), yang akan memodifikasi struktur global ester. Dan karena alasan ini sifat fisiknya, seperti kelarutan dan titik mendidih dan fusi, bervariasi dengan masing -masing senyawa.
Misalnya, lemak tak jenuh memiliki hubungan ganda dalam rantai R mereka, yang secara negatif mempengaruhi interaksi antar molekul. Akibatnya, titik leleh mereka turun, sampai cairan, atau minyak, pada suhu kamar.
Akseptor Jembatan Hidrogen
Meskipun citra kerangka ester lebih menonjol, itu adalah rantai R dan R yang bertanggung jawab atas keragaman dalam struktur mereka.
Namun, karakteristik struktural ester pantas untuk segitiga: mereka adalah akseptor jembatan hidrogen. Sebagai? Oleh oksigen dari gugus karbonil dan alkohol (-or ').
Ini memiliki pasangan elektron gratis, yang dapat menarik sebagian atom hidrogen positif dari molekul air.
Oleh karena itu, ini adalah jenis khusus interaksi dipol-dipol. Molekul air mendekati ester (jika rantai r o r tidak mencegah dan jembatan terbentuk c = o-h2Atau, atau oh2-ATAU '.
Nomenklatur ester
Untuk menyebutkan nama ester dengan tepat, itu perlu. Juga, cabang yang mungkin, substituen atau tidak jenuh.
Setelah ini selesai, nama r 'dari grup alkitab -atau' akhiran ditambahkan -ilo, Sedangkan rantai grup carboxilo -coor r, sufiks -Ato. Pertama, Bagian R disebutkan, diikuti oleh kata 'dari' dan kemudian nama bagian R '.
Misalnya, Cho3Ch2Ch2Cooch2Ch2Ch2Ch2Ch3 Ini memiliki lima karbon di sisi kanan, yaitu mereka yang sesuai dengan R '. Dan di sisi kiri ada empat atom karbon (termasuk kelompok karbonil C = O).
Oleh karena itu, R 'adalah kelompok pentil, dan r a butana (untuk memasukkan karbonil dan mempertimbangkan rantai utama). Kemudian, untuk memberi nama pada kompleks, itu cukup untuk menambahkan sufiks yang sesuai dan beri nama dalam urutan yang tepat: butanaAto dari Pentilo.
Cara memberi nama senyawa berikut: ch3Ch2Cooc (ch3)3? Rantai -c (cho3)3 sesuai dengan substituen alquilis recto-butyl. Karena sisi kiri memiliki tiga karbon, itu adalah "propana". Namanya: PropanaAto dari tert-tapiilo.
Bagaimana ester terbentuk?
Esterifikasi
Ada banyak rute untuk mensintesis ester, beberapa di antaranya bahkan bisa menjadi novel. Namun, mereka semua bertemu dalam fakta bahwa segitiga gambar struktur harus dibentuk, yaitu, tautan co-o. Untuk itu, ia harus mulai dari senyawa yang sebelumnya memiliki gugus karbonil: sebagai asam karboksilat.
Dan apa yang seharusnya dihubungkan dengan asam karboksilat? Untuk alkohol, jika tidak, ia tidak akan memiliki komponen alkohol yang menjadi ciri ester. Namun, asam karboksilat membutuhkan panas dan keasaman untuk memungkinkan mekanisme reaksi melanjutkan. Persamaan kimia berikut mewakili hal di atas:
Dapat melayani Anda: aluminium hydride (ALH3): Struktur, sifat, penggunaanRcooh + r'oh rcoor ' + h2SALAH SATU
(Setengah asam)
Ini dikenal sebagai esterifikasi.
Misalnya, asam lemak dapat diesterifikasi dengan metanol, cho3Oh, untuk mengganti asam mereka dengan gugus metil, jadi reaksi ini juga dapat dianggap sebagai metilasi. Ini adalah langkah penting ketika menentukan profil asam lemak dari minyak atau lemak tertentu.
Ester dari asam klorida
Cara lain untuk mensintesis ester adalah dari asil klorida, RCOCL. Di dalamnya, alih -alih mengganti gugus hidroksil OH, atom CL diganti:
Rcocl + r'oh => rcoor ' + hcl
Dan tidak seperti sterifikasi asam karboksilat, air tidak dilepaskan tetapi asam klorida.
Metode lain tersedia di dunia kimia organik, seperti oksidasi Baeyer-Villiger, yang menggunakan asam peroksi (RCOOOH).
Penggunaan Estres
 Esteres digunakan untuk berbagai hal, seperti pembuatan lilin
Esteres digunakan untuk berbagai hal, seperti pembuatan lilin Di antara penggunaan utama ester adalah:
- Dalam lilin atau lilin elaborasi, seperti gambar superior. Untuk tujuan ini, ester rantai samping yang sangat panjang digunakan.
- Sebagai pengawet obat atau makanan. Ini karena aksi paraben, yang tidak lebih dari ester dari asam para-hydroxibenzoic. Meskipun mereka mempertahankan kualitas produk, ada penelitian yang mempertanyakan efek positifnya pada tubuh.
- Mereka melayani untuk pembuatan wewangian buatan yang meniru bau dan rasa banyak buah atau bunga. Sehingga ester hadir dalam suguhan, es krim, parfum, kosmetik, sabun, sampo, di antara produk komersial lainnya yang pantas untuk aroma atau rasa yang menarik.
- Ester juga dapat memberikan efek farmakologis yang positif. Karena alasan ini industri farmasi telah mendedikasikan dirinya untuk mensintesis ester yang berasal dari asam yang ada di dalam tubuh untuk mengevaluasi kemungkinan peningkatan dalam pengobatan penyakit. Aspirin adalah salah satu contoh paling sederhana dari ester ini.
- Ester cair, seperti etil asetat, adalah pelarut yang memadai untuk jenis polimer tertentu, seperti nitroselulosa dan berbagai resin.
Contoh ester
Beberapa contoh ester tambahan adalah sebagai berikut:
- Butanato de pentilo, ch3Ch2Ch2Cooch2Ch2Ch2Ch2Ch3, yang berbau seperti albicoque dan pir.
- Vinyl Acetate, Cho3Cooch2= Ch2, dari mana polimer polivinil asetat terjadi.
- Isopentilo pentanoato, ch3Ch2Ch2Ch2Cooch2Ch2Ch (ch3)2, yang meniru rasa apel.
- Etil propanoat, ch3Ch2Cooch2Ch3.
- Propyl metanoate, hcooch2Ch2Ch3.
Referensi
- T.W. Graham Solomons, Craight B. Fryhle. Kimia organik. (Edisi Kesepuluh, hal 797-802, 820) Wiley Plus.
- Carey, f. KE. Organic Chemistry (2006) Edisi Keenam. Editorial MC Graw Hill-
- Libretteks Kimia. Nomenklatur Esers. Pulih dari: chem.Librettexts.org
- Admin. (19 September 2015). Ester: Sifat kimianya, sifat dan penggunaannya. Diambil dari: murni-kimia.com
- Kimia organik dalam kehidupan sehari -hari kita. (9 Maret 2014). Apa saja penggunaan ester? Diperoleh dari: Gen2Chemistassignment.Weebly.com
- Kimia.Net (2018). Contoh ester. Pulih dari: kimia.bersih
- Paz María de Lourdes Cornejo Arteaga. Aplikasi utama ester. Diambil dari: uaeh.Edu.MX
- Jim Clark. (Januari 2016). Pendahuluan Ester. Diambil dari: ChemGuide.bersama.Inggris

