Efek substitusi nukleofilik aromatik, contoh
- 2524
- 720
- Ray Thiel
Itu Substitusi nukleofilik aromatik (SNAR) adalah reaksi yang terjadi dalam kimia organik, yang terdiri dari perpindahan kelompok keluar yang baik oleh nukleofil yang masuk. Dari sudut pandang mekanismenya dan aspek elektronik, itu adalah wajah berlawanan dari substitusi elektrofilik aromatik (sear).
Umumnya kelompok yang keluar adalah halogen, yang keluar sebagai haluro x anion-. Reaksi ini hanya dapat terjadi jika cincin aromatik (kebanyakan benzena) kekurangan elektron; yaitu, jika Anda memiliki kelompok substituen penarik elektron.
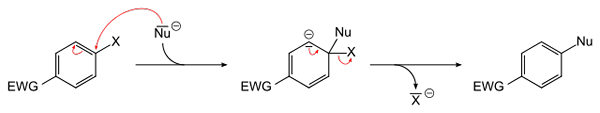
 Persamaan Umum untuk Substitusi Nukleofilik Aromatik. Sumber: Sponk [Domain Publik]
Persamaan Umum untuk Substitusi Nukleofilik Aromatik. Sumber: Sponk [Domain Publik] Gambar superior merencanakan apa yang dikatakan di paragraf sebelumnya. Kelompok Penarik Elektron EWG (untuk akronimnya dalam bahasa Inggris: Grup Penarikan Elektron), mengaktifkan cincin aromatik untuk serangan nukleofilik dari spesies Nu negatif-. Dapat dilihat bahwa perantara terbentuk (di tengah), dari mana haluro x dilepaskan atau dilepaskan-.
Perhatikan bahwa dalam istilah x sederhana itu digantikan oleh Nu di cincin aromatik. Reaksi ini sangat fleksibel dan diperlukan dalam sintesis obat baru, serta dalam studi kimia organik sintetis.
[TOC]
Fitur Umum
Cincin aromatik dapat "diisi" atau "unduh" dari elektron tergantung pada apa substituen mereka (mereka yang menggantikan tautan C-H asli).
Ketika substituen ini dapat menyumbangkan kepadatan elektronik ke cincin, dikatakan bahwa mereka memperkaya dari elektron; Jika sebaliknya mereka adalah penarik kepadatan elektronik (EWG yang disebutkan di atas), kemudian dikatakan bahwa mereka memiskinkan cincin elektron.
Dalam kasus apa pun, cincin diaktifkan untuk reaksi aromatik tertentu, saat dinonaktifkan untuk yang lain.
Misalnya, cincin aromatik yang kaya elektron dikatakan aktif untuk substitusi elektrofilik aromatik; Yaitu, Anda dapat menyumbangkan elektron Anda ke spesies elektrofilasi, dan+. Namun, itu tidak akan menyumbangkan elektron ke spesies NU-, karena tuduhan negatif akan saling mengusir.
Dapat melayani Anda: teori orbital molekulerSekarang, jika cincinnya buruk dalam elektron, ia tidak memiliki bagaimana memberikannya kepada spesies dan+ (Sear tidak terjadi); Sebaliknya, ketersediaan untuk menerima elektron spesies NU- (SNAR berkembang).
Perbedaan dengan substitusi elektrofilik aromatik
Mengklarifikasi aspek umum entri, beberapa perbedaan antara SNAR dan sear sekarang dapat terdaftar:
- Cincin aromatik bertindak sebagai elektrofil (elektron yang buruk) dan diserang oleh nukleofil.
- Grup X yang keluar diganti dari ring; Bukan h+
- Tidak ada karbokation yang terbentuk, tetapi perantara dengan muatan negatif yang dapat dipindahkan dengan resonansi
- Kehadiran kelompok yang lebih menarik di ring mempercepat substitusi alih -alih memperlambatnya
- Akhirnya, kelompok -kelompok ini tidak menggunakan sutradara di mana (di mana karbon) pengganti akan terjadi. Penggantian akan selalu terjadi pada karbon yang terkait dengan kelompok X yang keluar.
Poin terakhir juga diilustrasikan dalam gambar: tautan C-X rusak untuk membentuk tautan C-NU baru.
Efek
Dari jumlah substituen
Secara alami, semakin miskin dalam elektron adalah cincin, semakin cepat snar dan paling tidak drastis akan menjadi kondisi yang diperlukan untuk itu terjadi. Pertimbangkan contoh berikut yang diwakili dalam gambar bawah:
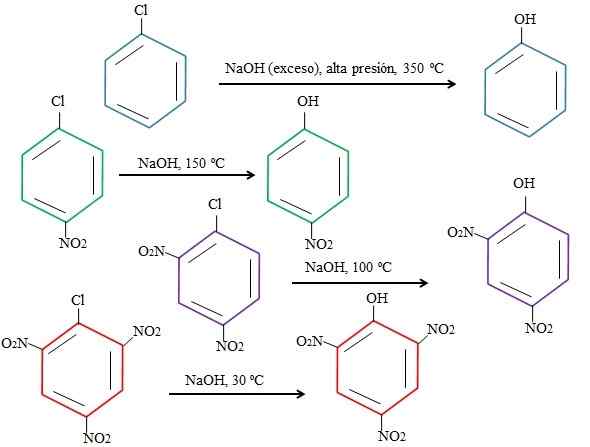 Efek substituen pada substitusi 4-nitroclorobenzene. Sumber: Gabriel Bolívar.
Efek substituen pada substitusi 4-nitroclorobenzene. Sumber: Gabriel Bolívar. Perhatikan bahwa 4-nitroclorobenzene (cincin biru) membutuhkan kondisi drastis (tekanan tinggi dan suhu 350 ºC) ke penggantian CL dengan. Dalam hal ini, klorin adalah kelompok keluar (CL-), dan hidroksida nukleofil (oh-).
Itu dapat melayani Anda: 4 periode kimia: dari prasejarah hingga hari iniSaat grup tidak muncul2, yang merupakan penarik elektron (cincin hijau), substitusi dapat dilakukan pada suhu 150 ºC pada tekanan sekitar. Karena jumlah kelompok meningkat tidak2 Hadir (cincin ungu dan merah), penggantian terjadi pada suhu yang semakin rendah (masing -masing 100 ºC dan 30ºC).
Oleh karena itu, kelompok tidak2 Mereka mempercepat jerat dan melepaskan dari elektron ke ring, membuatnya lebih rentan terhadap serangan OH-.
Posisi relatif CL tidak akan dijelaskan di sini sehubungan dengan tidak2 dalam 4-nitroclorobenzene, dan bagaimana mereka mengubah kecepatan reaksi; Sebagai contoh, kecepatan reaksi 2-nitroclorobenzene dan 3-nitrochlorobenzene berbeda, yang terakhir adalah yang paling lambat dibandingkan dengan isomer lainnya.
Dari kelompok yang keluar
Kembali ke 4-nitroclorobenzene, reaksi substitusi lebih lambat jika Anda membandingkan rekannya yang terfluorored:
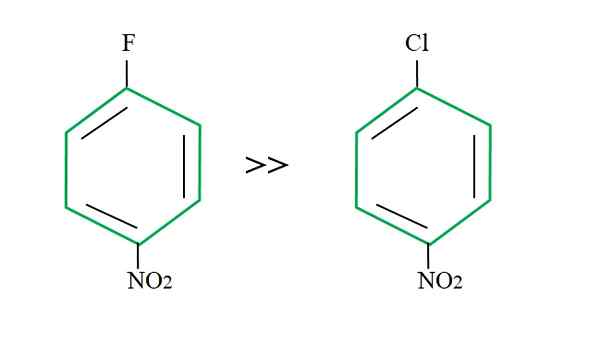 Efek kelompok keluar pada reaksi SNAR. Sumber: Gabriel Bolívar.
Efek kelompok keluar pada reaksi SNAR. Sumber: Gabriel Bolívar. Penjelasan ini tidak dapat terletak pada variabel lain bahwa perbedaan antara F dan CL. Fluorine adalah kelompok keluar yang buruk, karena tautan C-F lebih sulit untuk dipecahkan daripada tautan C-CL. Oleh karena itu, kerusakan tautan ini bukanlah langkah penentu kecepatan untuk SNAR, tetapi penambahan NU- ke cincin aromatik.
Fluor untuk menjadi lebih elektronegatif daripada klorin, atom karbon yang terkait dengannya memiliki defisiensi elektronik yang lebih besar (cδ+-Fδ-). Akibatnya, karbon dari tautan C-F jauh lebih mungkin diserang oleh NU- dari tautan C-CL. Itulah sebabnya penggantian f oleh oh jauh lebih cepat daripada cl oleh oh.
Dapat melayani Anda: tembaga sulfida: struktur, sifat, penggunaanContoh
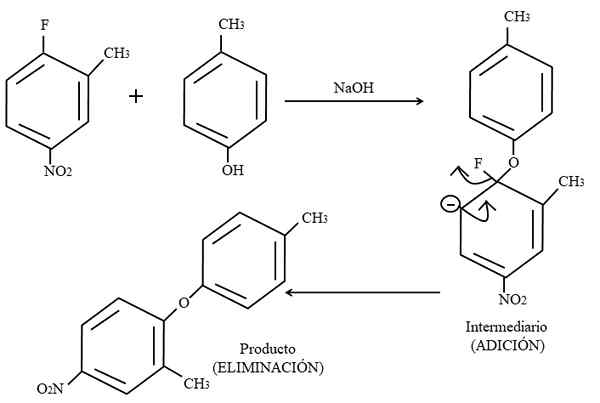 Ganti elektrofilik aromatik. Sumber: Gabriel Bolívar.
Ganti elektrofilik aromatik. Sumber: Gabriel Bolívar. Akhirnya, contoh jenis reaksi organik ini pada gambar yang lebih tinggi ditunjukkan di bawah ini. Para-Coresol tidak memberikan penampilan menjadi nukleofil; Tetapi memiliki media dasar, kelompok OH-nya tidak terlindungi, meninggalkan anion fenoksida, yang menyerang 2-metil-4-nitrofluorzene.
Ketika serangan ini terjadi, dikatakan bahwa nukleofil ditambahkan ke elektrofil. Langkah ini dapat dilihat di sebelah kanan gambar, di mana senyawa perantara dengan kedua substituen milik cincin terbentuk.
Dengan menambahkan para-coresol, beban negatif muncul yang merelokasi resonansi di dalam cincin (perhatikan bahwa berhenti aromatik).
Pada gambar, struktur resonansi terbaru hampir tidak ditampilkan, dari mana fluoride selesai sebagai f-; Tetapi pada kenyataannya beban negatif ini menjadi terpencil bahkan dalam atom oksigen kelompok2. Setelah penambahan eliminasi, yang terakhir, yaitu saat produk akhirnya terbentuk.
Komentar Akhir
Grup no2 Sisa dapat direduksi menjadi kelompok NH2, Dan dari sana dimungkinkan untuk membuat lebih banyak reaksi sintesis untuk memodifikasi molekul akhir. Ini menunjukkan potensi sintetis dari SNAR, dan bahwa mekanismenya, selain itu, terdiri dari dua langkah: salah satu penambahan dan salah satu dari eliminasi.
Saat ini, bagaimanapun, ada bukti eksperimental dan komputasi bahwa dalam kenyataannya reaksi terjadi mengikuti mekanisme bersama, di mana kedua langkah terjadi secara bersamaan melalui kompleks yang diaktifkan dan bukan perantara.
Referensi
- Morrison, r. T. dan boyd, r, n. (1987). Kimia organik. Edisi ke -5. Editorial Addison-Wesley Inter-American.
- Carey f. (2008). Kimia organik. (Edisi Keenam). MC Graw Hill.
- Graham Solomons t.W., Craig b. Fryhle. (2011). Kimia organik. Amina. (Edisi ke -10.). Wiley Plus.
- Wikipedia. (2019). Substitusi aromatik nukleofilik. Diperoleh dari: di.Wikipedia.org
- James Ashenhurst. (6 September 2019). Substitusi Aromatik Nukleofilik (NAS). Dipulihkan dari: Masterorganicchemistry.com
- Libretteks Kimia. (5 Juni 2019). Substitusi aromatik nukleofilik. Pulih dari: chem.Librettexts.org

