Struktur triethilamine, sifat, penggunaan dan risiko

- 1645
- 335
- Miss Marion Graham
Itu triethilamine Ini adalah senyawa organik, lebih tepatnya amina alifatik, yang formula kimianya adalah n (ch2Ch3)3 atau net3. Seperti amina cair lainnya, ia menghadirkan aroma yang mirip dengan amonia yang dicampur dengan ikan; Uapnya membuat yang membosankan dan berbahaya memanipulasi zat ini tanpa ekstraktor atau pakaian yang tepat.
Selain formula masing -masing, biasanya disingkat terhadap senyawa ini sebagai ASD; Namun, ini dapat menyebabkan kebingungan dengan amina lain, seperti trietanolamine, n (ethoh)3, atau tetraetilamonium, amina kuaterner, net4+.
 Kerangka triethylamine. Sumber: Campuran [CC BY-SA 3.0 (http: // createveCommons.Org/lisensi/by-sa/3.0/]]
Kerangka triethylamine. Sumber: Campuran [CC BY-SA 3.0 (http: // createveCommons.Org/lisensi/by-sa/3.0/]] Dari kerangka (gambar superior), dapat dikatakan bahwa triethylamine sangat mirip dengan amonia; Sedangkan yang kedua memiliki tiga hidrogen, NH3, Yang pertama memiliki tiga gugus etil, n (ch2Ch3)3. Sintesisnya dimulai dari pengobatan amonia cair dengan etanol, terjadi alkilasi.
Jaring3 Anda dapat membentuk garam higroskopis dengan HCl: triethilamine hydrochloride, net3· HCl. Selain itu, ia berpartisipasi sebagai katalis homogen dalam sintesis ester dan amidas, sehingga merupakan pelarut yang diperlukan di laboratorium organik.
Juga, bersama dengan reagen lain, memungkinkan oksidasi alkohol primer dan sekunder menjadi aldehida dan keton, masing -masing. Seperti amonia adalah dasar, dan oleh karena itu, ia dapat membentuk garam organik melalui reaksi netralisasi.
[TOC]
Struktur triethylamine
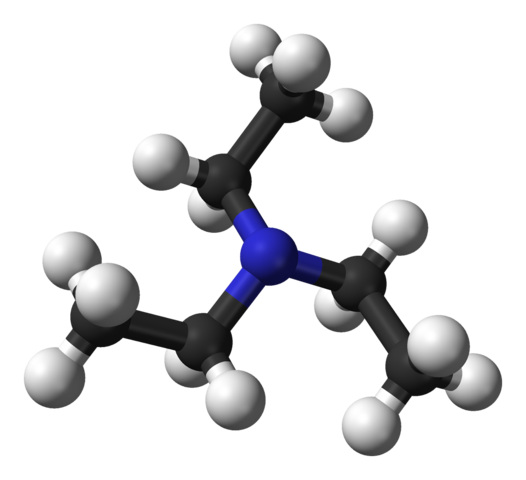 Struktur triethylamine. Sumber: Benjah-BMM27 [Domain Publik].
Struktur triethylamine. Sumber: Benjah-BMM27 [Domain Publik]. Gambar atas menunjukkan struktur triethylamine dengan model bola dan batang. Di tengah molekul atom nitrogen terletak, diwakili oleh bola kebiruan; Dan terkait dengannya, tiga kelompok etil, seperti cabang kecil bola hitam dan hitam.
Meskipun mereka tidak dengan mata telanjang, pada atom nitrogen ada beberapa elektron yang tidak dibagikan. Dua elektron ini dan tiga kelompok -ch2Ch3 mereka mengalami penolakan elektronik; Tetapi di sisi lain, mereka berkontribusi untuk menentukan momen dipol molekul.
Dapat melayani Anda: sikloalcanos: sifat, reaksi, penggunaan, contohNamun, momen dipol seperti itu lebih rendah dari pada, misalnya, dietilamine, nhet2; Dan juga, tidak ada kemungkinan untuk membentuk jembatan hidrogen.
Ini karena dalam triethylamine tidak ada ikatan N-H, dan akibatnya, fusi kecil dan titik didih diamati dibandingkan dengan amina lain yang berinteraksi sedemikian rupa.
Sementara ada sedikit momen dipol, kekuatan dispersi antara gugus etil molekul bersih tidak dapat dikesampingkan3 tetangga. Menambahkan efek ini, itu dibenarkan mengapa, meskipun triethylamine volatil, mendidih sekitar 89ºC, berkat massa molekulnya yang relatif besar.
Properti
Penampilan fisik
Cairan tidak berwarna dengan aroma amonia dan ikan yang tidak menyenangkan.
Masa molar
101.193 g/mol.
Titik didih
89ºC.
Titik lebur
-115ºC. Perhatikan betapa lemahnya kekuatan antarmolekul yang menyatukan molekul triethylamine dalam padatan mereka.
Kepadatan
0.7255 g/ml.
Kelarutan
Relatif larut dalam air, 5,5 g/100g pada 20ºC. Di bawah 18,7 ºC, menurut PubChem, bahkan tidak dapat dilihat dengan ini.
Selain "bergaul" dengan air, itu juga larut dalam aseton, benzena, etanol, eter, dan parafin.
Kepadatan uap
3.49 dalam kaitannya dengan udara.
Tekanan uap
57.07 mmHg pada 25ºC.
Henry Constant
66 μmol/pa · kg.
titik pengapian
-15ºC.
Suhu self -rection
312ºC.
Kapasitas panas
216.43 kJ/mol.
Panas pembakaran
10.248 kapur/g.
Panas penguapan
34.84 kJ/mol.
Tegangan permukaan
20.22 N/M A 25ºC.
Indeks bias
1.400 hingga 20ºC.
Zat yang lengket dan kental
0,347 MPa · S pada 25ºC.
Konstanta Basa Konstanta
Trietilamine memiliki PKB yang sama dengan 3,25.
Basa
Basa untuk amina ini dapat diekspresikan dengan persamaan kimia berikut:
Dapat melayani Anda: polimer sintetisBersih3 + Ha nhet3+ + KE-
Dimana itu spesies asam lemah. Pasangan nhet3+KE- Itu membentuk apa yang menjadi garam amonium tersier.
Asam Konjugat NET3+ Itu lebih stabil dari amonium, NH4+, karena tiga kelompok etil menyumbangkan bagian dari kepadatan elektronik mereka untuk mengurangi beban positif pada atom nitrogen; Oleh karena itu, triethylamine lebih mendasar daripada amonia (tapi kurang mendasar dari OH-).
Aplikasi
 Reaksi yang dikatalisis oleh triethylamine. Sumber: Tachymètre [domain publik].
Reaksi yang dikatalisis oleh triethylamine. Sumber: Tachymètre [domain publik]. Basisitas, dalam hal ini, nukleofilisitas triethylamine digunakan untuk mengkatalisasi sintesis ester dan amida dari substrat umum: asil klorida, RCOCL (gambar superior).
Di sini pasangan bebas elektron nitrogen menyerang kelompok karbonil, membentuk perantara; yang, secara berurutan, diserang oleh alkohol atau amina untuk membentuk ester atau amida, masing -masing.
Pada baris pertama gambar, mekanisme yang mengikuti reaksi untuk menghasilkan ester divisualisasikan, sedangkan baris kedua sesuai dengan Amida. Perhatikan bahwa dalam kedua reaksi triethylamine hydrochloride terjadi, bersih3· HCl, dari mana katalis pulih untuk memulai siklus lain.
Polimer
Nukleofilisitas triethylamine juga digunakan untuk menambahkan polimer tertentu, menyembuhkannya dan memberi mereka massa yang lebih besar. Sebagai contoh, ini adalah bagian dari sintesis resin polikarbonasi, busa poliuretan dan resin epoksi.
Kromatografi
Amfifilitas dan volatilitas jarak jauhnya memungkinkan garam yang diturunkan untuk digunakan sebagai reagen dalam kromatografi pertukaran ion. Penggunaan trietilemin lainnya implisit adalah bahwa beberapa garam amina tersier dapat diperoleh darinya, seperti triethylamine bikarbonat, NET3HCO3 (atau teh).
Dapat melayani Anda: kalorimetri: studi dan aplikasi apaProduk komersial
Ini telah digunakan sebagai aditif dalam formulasi rokok dan tembakau, pengawet makanan, lantai, penyedap, pestisida, pewarna, dll.
Risiko
Uap triethylamine tidak hanya tidak menyenangkan tetapi berbahaya, karena mereka dapat mengiritasi hidung, tenggorokan, dan paru -paru menyebabkan edema paru atau bronkitis. Demikian juga, menjadi lebih padat dan berat dari udara, mereka tetap di permukaan tanah, pindah ke sumber panas yang mungkin untuk meledak kemudian.
Wadah cairan ini harus jauh dari api karena mewakili bahaya ledakan yang akan terjadi.
Selain itu, kontak dengan spesies atau reagen seperti: logam alkali, asam trikloroasetat, nitrat, asam nitrat (seperti yang akan membentuk nitrosoamin, senyawa karsinogenik), asam kuat, peroksida dan permanganat.
Anda tidak boleh menyentuh aluminium, tembaga, seng atau paduannya, karena ia memiliki kemampuan untuk mengoreksi mereka.
Mengenai kontak fisik, itu dapat menyebabkan alergi dan ruam kulit jika paparannya akut. Selain paru -paru, itu dapat mempengaruhi hati dan ginjal. Dan mengenai kontak mata, itu menyebabkan iritasi, yang bahkan dapat merusak mata jika tidak dirawat atau dibersihkan tepat waktu.
Referensi
- Morrison, r. T. dan boyd, r, n. (1987). Kimia organik. Edisi ke -5. Editorial Addison-Wesley Inter-American.
- Carey f. (2008). Kimia organik. (Edisi Keenam). MC Graw Hill.
- Graham Solomons t.W., Craig b. Fryhle. (2011). Kimia organik. Amina. (Edisi ke -10.). Wiley Plus.
- Wikipedia. (2019). Triethylamine. Diperoleh dari: di.Wikipedia.org
- Merck. (2019). Triethylamine. Pulih dari: sigmaaldrich.com
- Pusat Nasional Informasi Bioteknologi. (2019). Triethylamine. Database pubchem. CID = 8471. Pulih dari: pubchem.NCBI.Nlm.Nih.Pemerintah
- Jaringan Data Toksikologi. (S.F.). Triethylamine. Pulih dari: Toxnet.Nlm.Nih.Pemerintah
- Departemen Kesehatan New Jersey. (2010). Triethylamine. Pulih dari: NJ.Pemerintah
- « 10 keingintahuan tentang Abad Pertengahan yang akan mengejutkan Anda
- Struktur alkohol isoamilico, sifat, penggunaan dan risiko »

