Sifat klorin oksida (III), struktur, penggunaan
- 1540
- 437
- Mr. Darrell Streich
Dia klorin oksida (III) Itu adalah senyawa anorganik yang formula kimianya adalah cl2SALAH SATU3. Sesuai dengan anhidrida asam kloro, HCLO2. Ini adalah padatan coklat gelap, sangat eksplosif bahkan pada suhu di bawah 0ºC, dan kurang ditandai. Itulah mengapa itu tunduk pada minat untuk studi komputer.
Secara kimia itu adalah oksida kovalen, jadi ada ikatan CL-O dan molekul diskrit dari CL2SALAH SATU3 (gambar bawah). Molekul ini mungkin membentuk dehidrasi HCLO2, atau dengan tunduk pada suhu rendah. Detailnya adalah membusuk memproduksi CL2, SALAH SATU2, atau oksida klorin yang lebih stabil secara termodinamika lainnya.
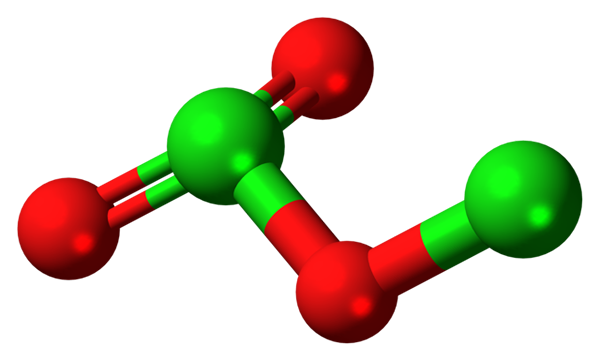
 Molekul dicloro trioksida. Sumber: Jynto [CC0].
Molekul dicloro trioksida. Sumber: Jynto [CC0]. Karena ikatan CL-O sedikit kutub, email CL2SALAH SATU3 Ini memiliki momen dipol kecil; Oleh karena itu, itu tidak larut dengan baik dalam air atau berinteraksi dengan pelarut kutub lainnya. Ketidakstabilannya sedemikian rupa sehingga tidak diketahui penggunaan komersial atau potensial (atau sebagai peledak penerapannya akan layak).
Alasan utama ketidakstabilannya mungkin karena karakteristik elektronik dari dugaan CL3+ (dengan asumsi karakter ion yang murni). Faktanya, keadaan oksidasi +1 dan +5 adalah yang paling stabil ketika klorin membentuk senyawa dengan oksigen.
[TOC]
Properti
Karena karakterisasinya buruk dan tidak terdokumentasi, tidak banyak yang bisa dikatakan tentang propertinya kecuali poin -poin berikut:
-Ini memiliki massa molekul 118.903.
-Itu berwarna coklat gelap; Meskipun Anda dapat membahayakan gas klorin, mengatakan uap hijau kekuningan.
-Tidak memiliki titik mendidih dan fusi, karena pada 0ºC meledak (dan pada suhu yang lebih dingin juga).
Dapat melayani Anda: Dihydroxyacetone phosphate (DHAP): Karakteristik dan Aplikasi-Kelarutannya dalam air diperkirakan sekitar 3,42 g/100 ml, yang membuktikan bahwa itu adalah molekul kovalen dari polaritas rendah.
-Bereaksi dengan air (sedikit yang larut) menjadi HCLO2:
Cl2SALAH SATU3 + H2Atau 2hclo2
Struktur oksida klorin (III)
Dalam gambar struktur molekul CL ditampilkan2SALAH SATU3 Dengan model bola dan batang. Meskipun tampaknya tidak telanjang, implikasi diam -diam dari tautan spasial dan pengaturannya lebih rumit daripada yang terlihat. Struktur ini sesuai dengan salah satu dari banyak isomer yang mungkin untuk senyawa ini.
Bola merah sesuai dengan atom oksigen, dan yang hijau ke atom klorin. Klorin di sebelah kiri menyajikan geometri piramida trigonal, dengan beberapa elektron bebas; Jadi dapat diasumsikan bahwa hibridisasi Anda harus SP3. Atom oksigen bertindak sebagai jembatan antara dua kloro, cl-o-cl.
Isomer
Apa isomer lainnya? Secara teori sembilan dihitung, di mana empat adalah yang paling stabil (termasuk gambar). Tiga lainnya akan memiliki struktur seperti:
-Clclo3. Sangat mirip dengan yang dijelaskan, tetapi dengan tautan CL-Cl.
-CLOOOCL (1). Dalam isomer ini ada jembatan tiga oksigen yang memisahkan dua atom klorin (ingat geometri sudut H2Atau untuk memvisualisasikannya).
-CLOOOCL (2). Jembatan teroksigenasi yang sama juga ada di isomer ini, dengan pengecualian dari dua atom klorin dikalahkan di ruang; satu di depan yang lain, sedangkan di isomer sebelumnya mereka jauh.
Itu bisa melayani Anda: alquinosTata nama
Namanya, klorin oksida (III), sesuai dengan yang ditugaskan sesuai dengan nomenklatur stok. Di sini diasumsikan bahwa klorin memiliki keadaan oksidasi +3; Tetapi itu tidak berarti bahwa kation klasik3+ mungkin ada. Itu adalah molekul, bukan jaringan ion.
Nama lain yang dengannya CL juga dikenal2SALAH SATU3 Ini adalah dicloro trioksida, menurut nomenklatur sistematis.
Dan final. Nama ini disebabkan oleh fakta bahwa, seperti yang sudah dijelaskan, CL2SALAH SATU3 Itu terjadi saat hclo2 Itu mengembun air menyiram.
Aplikasi
Karena itu adalah klorin oksida, penggunaan paling langsung yang dapat dipikirkan CL2SALAH SATU3 Ini seperti zat pengoksidasi, yang mampu menetralkan kotoran dan mikroba organik. Namun, ini sangat tidak stabil, selain bahan peledak, sehingga untuk tujuan ini dianggap berguna.
Pasti tidak ada informasi bahkan bagaimana CL akan berperilaku2SALAH SATU3 di bawah tekanan besar (jika tidak meledak dalam proses). Dalam kondisi normal, tampaknya tidak lebih dari perantara yang relatif stabil dan dapat dibedakan di antara oksida klorin yang lebih stabil lainnya.
Namun, secara komputasi, telah diteliti untuk menentukan mekanisme dengan radikal bebas yang melibatkan beberapa spesies klorin dan oksigen.
Referensi
- Shiver & Atkins. (2008). Kimia anorganik. (Edisi keempat). MC Graw Hill.
- Wikipedia. (2019). Dichlorine trioksida. Diperoleh dari: di.Wikipedia.org
- Beri dia l. Perry. (2011). Buku Pegangan Senyawa Anorganik. (Edisi kedua). CRC Press Taylor & Francis Group.
- Richard c. Ropp. (2013). Encyclopedia dari senyawa bumi alkali. Elsevier.
- Kim K. H., Han dan.K., dan baca dan. S. (1999). Efek set basis pada stabilitas isomer CL2O3 menggunakan metode B3P86 dan B3LYP dari teori fungsional kepadatan. Jurnal Struktur Molekul Theochem 460 (1-3): 19-25.
- « Struktur besi hidroksida (II), sifat, penggunaan
- Struktur tetrodotoxin, karakteristik, penggunaan, efek »

