Struktur besi hidroksida (II), sifat, penggunaan
- 3085
- 412
- Irvin Reichel
Dia besi hidroksida (II), Juga disebut besi hidroksida, ini adalah senyawa anorganik dari formula kimia iman (OH)2. Jika kemurniannya tinggi, padatannya hanya terdiri dari ion iman2+ dan oh- Dalam hubungan 2: 1; Namun, molekul air dan spesies ionik yang berbeda dapat mengandung, mengubah posisi.
Mewakili bentuk "tereduksi" dari karat yang terkenal, permukaan kemerahan yang terdiri dari ion agama3+; Saat berada dalam karat kehijauan, iman mendominasi2+, di sebelah oh- dan jumlah anion lainnya: CO32-, Sw42-, TIDAK3- dan haluros (f-, Cl-,… ), Misalnya. Hasilnya, meskipun basis karat hijau ini adalah iman (OH)2, adalah bahwa berbagai padatan diperoleh.
 Oksida hijau pada permukaan besi: Sumber bahan dari jenis hidroksida ini. Sumber: Pixabay.
Oksida hijau pada permukaan besi: Sumber bahan dari jenis hidroksida ini. Sumber: Pixabay. Dalam kehidupan sehari -hari hidroksida ini dapat direnungkan di tempat umum. Misalnya, kapal gambar atas memiliki permukaan karat hijau yang tertutup (bukan patina). Ada iman (oh)2, tetapi disertai dengan banyak ion dari gelombang laut.
Berbicara secara kimia, sifat dan penggunaan materi ini bergantung pada kation iman2+ dan kecenderungannya untuk mengoksidasi untuk berubah menjadi iman3+. Ini adalah zat pereduksi, yang bereaksi dengan cepat dengan oksigen dalam kondisi dasar. Oleh karena itu harus digunakan dalam atmosfer inert dan larutan asam.
[TOC]
Struktur besi hidroksida (II)
Tautan
Mempertimbangkan hanya iman (oh)2 Murni, tidak ada lagi ion imun2+ dan oh-.
Interaksi di antara mereka harus, secara teori, bersifat ionik; Setiap iman iman2+ menarik dua anion oh-, yang objek wisata non -langsungnya akhirnya menetapkan tatanan struktural dan berulang yang mendefinisikan kristal; Itu pada gilirannya, memunculkan debu karat hijau.
Ini dapat melayani Anda: seng hidroksida (Zn (OH) 2)Masalahnya adalah bahwa ada karakter kovalen tertentu antara kedua ion, dan oleh karena itu, tautan ionik Fe-OH tidak dapat diabaikan. Mempertimbangkan tautan fe-oh ionik sebagian, dapat dipahami bahwa mereka dikelompokkan menjadi semacam lapisan polimer.
Lapisan hidroksida ganda
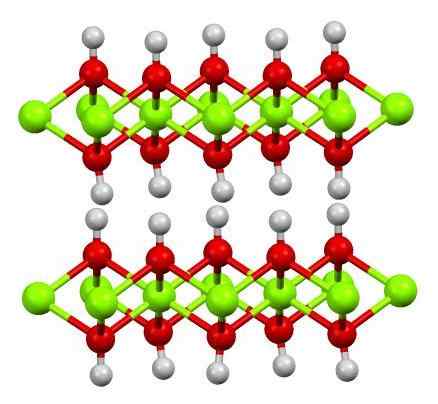
 Struktur Iman (OH) 2. Sumber: Smokefoot [CC BY-SA 4.0 (https: // createveCommons.Org/lisensi/by-sa/4.0)]
Struktur Iman (OH) 2. Sumber: Smokefoot [CC BY-SA 4.0 (https: // createveCommons.Org/lisensi/by-sa/4.0)] Struktur hidroksida besi murni dengan model bola dan batang ditunjukkan di atas. Kation fe2+ Mereka diwakili oleh bola hijau chillón, sementara oh anion- Untuk bidang merah dan putih. Perhatikan bagaimana ion iman diselaraskan2+ Berkat interaksi (ionik-kovalen) dengan OH-.
Mengapa struktur ini lapisan ganda hidroksida? Gambar itu sendiri menawarkan jawabannya: Ada dua baris atau lapisan OH- Untuk setiap iman2+; yaitu, proporsi 2: 1 dari iman (OH) dipertahankan2 disebutkan di awal.
Unit Struktural untuk Iman (OH)2 Mereka kemudian adalah sandwich ini, di mana lapisan oh- Mereka akan datang untuk mewakili roti; Roti yang dimuat secara negatif dan, oleh karena itu, gagal memperbaiki kristal coklat yang mencolok.
Tapi, di sisi lain, atom H juga menyelaraskan dan melampaui satu sama lain. Mengingat konsep polaritas dan elektronegativitas, hidrogen ini memiliki sedikit beban parsial positif, Δ+; yang, meskipun lemah, dapat memiliki area positif di mana anion atau molekul lain ditempatkan.
Melembabkan
Saat iman (oh)2 Itu larut dalam air, molekulnya berkoordinasi dengan pusat logam iman2+ Untuk membentuk ACU yang kompleks: [iman (h2SALAH SATU)4(OH)2]. Kompleks ini memiliki geometri oktahedral untuk memiliki enam ligan: empat molekul air dan dua oh-. Namun, dalam hidroksida besi panorama sedikit berbeda.
Dapat melayani Anda: hukum tentang konservasi materiDalam hidrat, formula hipotetis Fe (OH)2· NH2Atau, molekul air ditempatkan tepat di antara dua lapisan hidroksida; yaitu, mereka berinteraksi melalui gaya ion dipol dengan hidrogen atau bola putih. Seolah -olah dua pertandingan Ohfeoh diraih dan air diselingi untuk mengelompokkannya: ohfeoh (h2O) Ohfeah.
Molekul air sangat dinamis, mencegah partikel hidrat memperoleh ukuran yang cukup besar dan, akibatnya, membentuk koloid atau jeli padat.
Karat Hijau dan Merah
Dalam hidrat, lapisan hidroksida memiliki molekul air yang diselingi; Namun, mereka dapat memiliki anion lain (sudah disebutkan), menyebabkan berbagai herrbles hijau. Mereka juga dapat "menangkap" molekul sebesar DNA, atau obat.
Ion iman tidak hanya bisa hadir2+, tetapi juga iman3+, Produk oksidasi internal yang disebabkan oleh oksigen yang diselingi. Terlihat akan diamati bahwa karat hijau (u oksida) mulai menjadi kemerahan karena konsentrasi iman meningkat3+.
Properti
 Tabung reaksi dengan hidroksida besi dalam air. Sumber: ChemicalInterest [domain publik]
Tabung reaksi dengan hidroksida besi dalam air. Sumber: ChemicalInterest [domain publik] Iman (OH) ditunjukkan di atas2 mengendap dalam tabung reaksi. Berada di dalam air yang berlimpah, ACU kompleks harus mendominasi di atas struktur yang baru disebutkan. Perhatikan bahwa permukaannya terlihat seperti warna oranye, sebagai akibat dari oksidasi iman2+ untuk iman3+ untuk oksigen udara; Artinya, hidroksida ini adalah agen peredam:
Keyakinan2+ Keyakinan3+ + Dan-
Penampilan fisik senyawa ini dalam keadaan paling murni adalah padatan coklat:
 Hidroksida besi murni. Sumber: Ondřej Mangl [domain publik]
Hidroksida besi murni. Sumber: Ondřej Mangl [domain publik] Yang, tergantung pada tingkat kelembabannya, dapat disajikan sebagai jeli -green padat. Cukup tidak larut dalam air (ksp= 8 · 10-16 dan kelarutan = 0,72 g/100ml pada 25ºC), dan memiliki massa molar 89,86 g/mol dan kepadatan 3,4 g/ml.
Itu dapat melayani Anda: 20 jenis kimia dan denifikasi merekaTidak ada titik mendidih atau fusi untuk senyawa ini dilaporkan; Mungkin karena fakta bahwa, sebelum sumber panas, itu menjadi dehidrasi dan diubah menjadi ferro oksida, jelek:
Iman (oh)2 => Jelek + h2SALAH SATU
Aplikasi
Analisis Kualitatif Organik
Kekuatan reduksi digunakan untuk menentukan keberadaan senyawa nitro, RNO2. Reaksi yang diperoleh tes positif diwakili dengan persamaan kimia berikut:
Rno2 + 6fe (oh)2 + 4H2O => rnh2 + 6fe (oh)3
Iman (oh)3 mengendap sebagai padatan coklat -redizo, yang mengesahkan keberadaan kelompok nitro, -tidak2.
Reduser Selenium Oxoanions
The Reduksi Kekuatan Iman (OH)2 Itu juga digunakan untuk mengurangi anion SEO32- (selenito) dan SEO42- (selenate) ke selenium dasar,. Secara praktis, memungkinkan penghapusan anion semacam itu, berbahaya bagi kesehatan, dalam bentuk padatan selenium yang tidak dapat dilepas dan mudah dilepas.
Bahan lapisan ganda
Struktur murni, dan karat hijau, adalah sumber inspirasi untuk desain bahan baru karakteristik mineralogi.
Diperkirakan bahwa fungsi ini adalah memungkinkan pengangkutan spesies tertentu di antara lapisan -lapisannya, sedemikian rupa sehingga pembebasannya dapat dikontrol atau dikurangi ke situs aktif (tanah, sel, permukaan logam, dll.).
Referensi
- Shiver & Atkins. (2008). Kimia anorganik. (Edisi keempat). MC Graw Hill.
- Wikipedia. (2019). Besi (ii) hidroksida. Diperoleh dari: di.Wikipedia.org
- Pusat Nasional Informasi Bioteknologi. (2019). Hidroksida besi. Database pubchem. CID = 10129897. Pulih dari: pubchem.NCBI.Nlm.Nih.Pemerintah
- Nick Doe. (S.F.). Tes untuk Fenol dan Grup Nitro. Kimia 211. Diperoleh dari: akademisi.Wellesley.Edu
- Clark Jim. (27 April 2019). Kimia Besi. Libretteks Kimia. Pulih dari: chem.Librettexts.org
- Perangkat Lunak Teknis Kingston. (2019). Kimia karat. Dokter Korosi. Pulih dari: dotor korosi.org
- Zingaro, Ralph A. et al. (1997). Pengurangan anion oksoselenium oleh zat besi (II) hidroksida. Lingkungan Internasional. 23 (3): 299-304. Doi: 10.1016/S0160-4120 (97) 00032-9

