Oksida besi

- 4120
- 219
- Irvin Reichel
 Besi oksida adalah senyawa kimia antara besi dan oksigen
Besi oksida adalah senyawa kimia antara besi dan oksigen Apa itu besi oksida?
Dia oksida besi Itu adalah salah satu senyawa yang terbentuk antara besi dan oksigen. Mereka ditandai dengan menjadi ionik dan kristal, dan mereka berbaring tersebar sebagai akibat dari erosi mineral mereka, menyusun tanah, massa tanaman dan bahkan bagian dalam organisme hidup.
Itu adalah salah satu keluarga senyawa yang mendominasi di kerak bumi. Oksida besi diketahui sampai saat ini, kebanyakan dari mereka berasal dari alami dan disintesis lainnya di bawah tekanan ekstrem atau kondisi suhu.
Pada gambar atas, bagian dari bubuk oksida besi ditampilkan. Karakteristik warna merahnya mencakup besi dari beberapa elemen arsitektur dalam apa yang dikenal sebagai karat. Demikian juga, diamati di lereng, gunung atau tanah, dicampur dengan banyak mineral lainnya, seperti debu kuning goethita (α-feooh).
Oksida besi paling terkenal adalah hematit (α-Fe2SALAH SATU3) dan maghemita (ϒ-faith2SALAH SATU3), kedua polimorf oksida besi; Dan paling tidak, magnetit (iman3SALAH SATU4).
Struktur polimorfiknya dan area superfisial yang besar dibuat oleh bahan -bahan menarik seperti sorbentes, atau untuk sintesis nanopartikel dengan aplikasi yang luas.
Struktur besi oksida
Gambar atas adalah representasi dari struktur kristal yang jelek, salah satu oksida besi di mana besi memiliki valensi +2. Bola merah sesuai dengan anion atau2-, Sedangkan kation kuning ke iman2+.
Perhatikan bahwa setiap iman2+ dikelilingi oleh enam atau2-, membentuk unit koordinasi oktahedral.
Oleh karena itu, struktur jelek dapat "hancur" dalam unit jelek6, Dimana atom pusat adalah iman2+. Dalam kasus oxihydroxides atau hidroksida, unit oktahedral jelek3(OH)3.
Dapat melayani Anda: kalsium peroksida (cao2): sifat, risiko dan penggunaanDalam beberapa struktur, bukan octahedron, ada unit tetrahedral, jelek4. Untuk alasan ini, oksida besi biasanya diwakili dengan oktur atau tetrahedra dengan pusat besi.
Struktur oksida besi tergantung pada kondisi tekanan atau suhu, pada rasio iman/atau (yaitu, berapa banyak oksigen yang ada untuk zat besi dan sebaliknya), dan Valencia del Hierro (+2, +3 dan, sangat jarang dalam oksida sintetis oksida sintetis sintetis , +4).
Secara umum, anion besar atau2- Mereka menyelaraskan lembaran pembentukan yang lubangnya menjadi tuan rumah kation iman2+ atau iman3+. Dengan demikian, ada oksida (seperti magnetit) yang memiliki setrika dengan kedua valensi.
Polimorfisme
Oksida besi memiliki polimorfisme, yaitu, struktur yang berbeda atau pengaturan kristal untuk senyawa yang sama. Oksida besi, iman2SALAH SATU3, memiliki hingga empat polimorf yang memungkinkan. Hematit, α-fe2SALAH SATU3, Ini adalah yang paling stabil; diikuti oleh Maghemita, ϒ-Faith2SALAH SATU3, dan untuk β- iman sintetis2SALAH SATU3 dan ε- iman2SALAH SATU3.
Semuanya memiliki jenis struktur dan sistem kristal sendiri. Namun, proporsi 2: 3 tetap konstan, jadi ada tiga anion atau2- untuk setiap dua kation iman3+.
Perbedaannya terletak pada bagaimana unit oktahedral jelek berada6 di luar angkasa dan bagaimana mereka berkumpul.
Tautan Struktural
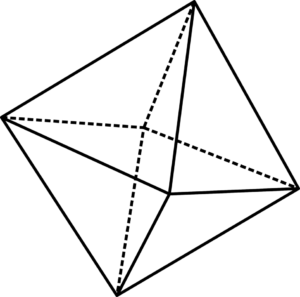 Unit oktahedral yang jelek6
Unit oktahedral yang jelek6 Unit oktahedral yang jelek6 dapat divisualisasikan dengan bantuan gambar superior. Di sudut -sudut octaedro adalah atau2-, Sementara di tengahnya keyakinan2+ atau iman3+(Dalam kasus iman2SALAH SATU3). Cara di mana octahedra ini diatur di ruang angkasa mengungkapkan struktur karat.
Namun, mereka juga memengaruhi cara mereka terhubung. Misalnya, dua octahedra dapat bergabung dengan dua simpul mereka, yang diwakili dengan jembatan oksigen: fe-o-fe. Demikian pula, Octahedra dapat bergabung melalui tepi mereka (berdekatan satu sama lain). Itu kemudian akan diwakili dengan dua jembatan oksigen: fe- (o)2-Keyakinan.
Dapat melayani Anda: klorin oksida (v): sifat, struktur, penggunaanDan akhirnya, Octahedra dapat berinteraksi melalui wajah mereka. Dengan demikian, representasi sekarang dengan tiga jembatan oksigen: fe- (o)3-Keyakinan. Cara di mana octahedra terkait, jarak internuclear fe -fe akan bervariasi dan, oleh karena itu, sifat fisik oksida.
Sifat oksida besi
Oksida besi adalah senyawa dengan sifat magnetik. Ini bisa anti, ferro atau ferrimagnetik, dan bergantung pada valensi iman dan bagaimana kation berinteraksi dalam padatan.
Karena struktur padat sangat bervariasi, dengan cara yang sama sifat fisik dan kimianya.
Misalnya, polimorf dan hidrat iman2SALAH SATU3 Mereka memiliki nilai titik leleh yang berbeda (yang berkisar antara 1.200 dan 1.600 ° C) dan kepadatan. Namun, mereka memiliki sedikit kelarutan mengikuti iman3+, Massa molekul yang sama adalah warna coklat dan hampir tidak tersentum dalam larutan asam.
Nomenklatur oksida besi
IUPAC menetapkan tiga cara untuk memberi nama besi oksida. Ketiganya sangat berguna, meskipun untuk oksida kompleks (seperti iman7SALAH SATU9) Sistematika mengatur yang lain karena kesederhanaannya.
Nomenklatur sistematis
Bilangan oksigen dan zat besi dipertimbangkan, menamai mereka dengan awalan mono-mono-, di-, tri-, dll. Menurut nomenklatur ini keyakinan2SALAH SATU3 disebut: Trioksida telah memberibesi. Dan untuk iman7SALAH SATU9 Namanya adalah: heptahierro nonaxide.
Nomenklatur stok
Ini menganggap Valencia del Hierro. Jika itu iman2+, Besi oksida ditulis ... dan valensinya dengan angka Romawi terkunci dalam tanda kurung. Untuk iman2SALAH SATU3 Namanya: Iron Oxide (III).
Dapat melayani Anda: Tekanan uap: konsep, contoh dan latihan diselesaikanPerhatikan iman itu3+ Itu dapat ditentukan dengan jumlah aljabar. Ya2- Ini memiliki dua muatan negatif, dan ada tiga di antaranya, tambahkan -6. Untuk menetralkan -6 ini mereka membutuhkan +6, tetapi ada dua iman, sehingga mereka harus dibagi dengan dua, +6/2 = +3:
2x (logam valencia) + 3 (-2) = 0
Cukup membersihkan valensi iman dalam oksida. Tetapi jika x bukan bilangan bulat (seperti halnya hampir semua oksida yang tersisa), maka ada campuran iman2+ dan iman3+.
Nomenklatur tradisional
Akhiran -ICO diberikan kepada awalan ferr- ketika iman memiliki valencia +3, dan -jadi ketika valencia -nya adalah 2+. Dengan demikian, iman2SALAH SATU3 disebut: ferric oxide.
Besi oksida menggunakan
Nanopartikel
Oksida besi memiliki energi kristalisasi tinggi, yang memungkinkan untuk membuat kristal yang sangat kecil tetapi dengan luas permukaan yang besar.
Karena alasan ini mereka sangat menarik di bidang nanoteknologi, di mana mereka merancang dan mensintesis nanopartikel oksida (NP) untuk tujuan tertentu:
- Sebagai katalis.
- Sebagai reservoir obat atau gen di dalam tubuh.
- Dalam desain permukaan sensorik untuk berbagai jenis biomolekul: protein, gula, lemak.
- Untuk menyimpan data magnetik.
Pigmen
Karena beberapa oksida sangat stabil, mereka berfungsi untuk mewarnai tekstil atau memberikan warna -warna cerah pada permukaan bahan apa pun. Dari mosaik lantai -lukisan merah, kuning dan oranye (bahkan hijau) -, plastik, kulit ke karya arsitektur.
Referensi
- Wali Amanat Dartmouth College (18 Maret 2004). Stoikiometri oksida besi. Diambil dari: Dartmouth.Edu
- Ryosuke Sinmyo et al. (8 September 2016). Penemuan Fe7SALAH SATU9: Oksida besi baru dengan struktur monoklinik yang kompleks. Pulih dari: alam.com
- M. Cornell, u. Schwertmann. Oksida besi: struktur, sifat, reaksi, kejadian dan penggunaan [pdf]. Wiley-VCH. Diambil dari: EPSC511.Wustl.Edu

