Emas oksida (III) (AU2O3) Apa itu, struktur, sifat, penggunaan
- 3602
- 370
- Dewey Runolfsdottir
Dia Gold Oxide (III) Itu adalah senyawa anorganik yang formula kimianya adalah au2SALAH SATU3. Secara teoritis, sifatnya bisa diharapkan di luar tipe kovalen. Namun, keberadaan karakter ionik tertentu dalam padatannya tidak dapat sepenuhnya dikesampingkan; atau apa yang sama, asumsikan tidak adanya kation3+ di sebelah anion atau2-.
Mungkin tampak bertentangan bahwa emas, menjadi logam yang mulia, dapat mengoksidasi. Dalam kondisi normal, potongan emas tidak dapat teroksidasi melalui kontak dengan oksigen atmosfer; Namun, ketika mereka diiradiasi dengan radiasi ultraviolet di hadapan ozon, atau3, Panorama adalah yang lain.
Jika bintang emas mengalami kondisi ini, mereka akan menjadi warna coklat kemerahan, karakteristik AU2SALAH SATU3.
Metode lain untuk mendapatkan oksida ini akan menyiratkan pengobatan kimia dari bintang -bintang ini; Misalnya, mengubah adonan emas menjadi klorida masing -masing, AUCL3.
Kemudian ke AUCL3, Dan sisa garam emas yang mungkin terbentuk, media dasar yang kuat ditambahkan; Dan dengan ini, hidrasi atau hidroksida oksida diperoleh, Au (OH)3. Akhirnya, senyawa yang terakhir mengalami dehidrasi secara termal untuk mendapatkan Au2SALAH SATU3.
Struktur oksida emas (III)
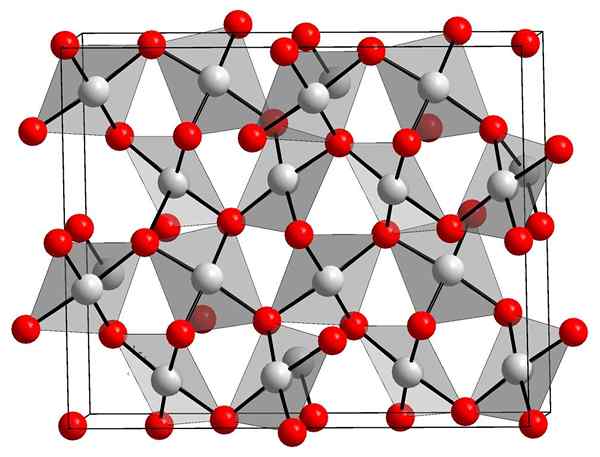
 Struktur kristal oksida emas. Orci, Wikimedia Commons.
Struktur kristal oksida emas. Orci, Wikimedia Commons. Gambar atas menunjukkan struktur kristal oksida emas (III). Disposisi atom emas dan oksigen dalam padatan ditunjukkan, baik mempertimbangkan atom netral (padatan kovalen), atau ion (padatan ionik). Secara bergantian, hilangkan saja atau tempatkan tautan AU-O dalam kasus apa pun.
Menurut gambar, diasumsikan bahwa karakter kovalen mendominasi (yang akan logis). Untuk alasan itu, atom dan tautan yang diwakili dengan bola dan batang ditampilkan, masing -masing. Bola putih sesuai dengan atom emas (AUAKU AKU AKU-O), dan atom oksigen kemerahan.
Dapat melayani Anda: hidroksiapatitJika diamati dengan hati -hati, akan terlihat bahwa ada unit AUO4, yang mengikat dengan atom oksigen. Cara lain untuk memvisualisasikannya adalah dengan mempertimbangkan bahwa setiap au3+ dikelilingi oleh empat atau2-; Tentu saja, dari perspektif ionik.
Struktur ini kristal karena atom diperintahkan dengan mematuhi pola panjang yang sama. Dengan demikian, sel kesatuannya sesuai dengan sistem kristal rhombohedral (sama seperti gambar atas). Oleh karena itu, semua au2SALAH SATU3 Itu bisa dibangun jika semua bidang sel unit didistribusikan di luar angkasa.
Aspek elektronik
Emas adalah logam transisi, dan diharapkan bahwa orbital 5D -nya berinteraksi langsung dengan orbital 2p dari atom oksigen. Tumpang tindih orbitalnya secara teoritis harus menghasilkan pita penggerak, yang akan membuat AU2SALAH SATU3 Dalam semikonduktor padat.
Oleh karena itu, struktur Au yang sebenarnya2SALAH SATU3 bahkan lebih kompleks dalam pikiran ini.
Melembabkan
Oksida emas dapat menahan molekul air di dalam kristal rhomboédicanical, yang menimbulkan hidrat. Ketika hidrat seperti itu terbentuk, strukturnya menjadi amorf, yaitu, tidak teratur.
Formula kimia untuk hidrat semacam itu bisa menjadi salah satu dari yang berikut, yang sebenarnya tidak diklarifikasi secara mendalam: AU2SALAH SATU3∙ Zh2O (z = 1, 2, 3, dll.), Au (oh)3, atau auXSALAH SATUDan(OH)z.
Formula AU (OH)3 mewakili penyederhanaan komposisi sebenarnya dari hidrat ini. Ini karena di dalam emas hidroksida (III), para peneliti juga menemukan keberadaan Au2SALAH SATU3; Dan oleh karena itu, ia kehilangan makna untuk memperlakukannya secara terpisah sebagai hidroksida logam transisi "sederhana".
Dapat melayani Anda: keseimbangan uap cairDi sisi lain, dari padatan dengan formula AuXSALAH SATUDan(OH)z Struktur amorf bisa diharapkan; Karena ini tergantung pada koefisiennya X, Dan Dan z, yang variasinya akan menghasilkan semua jenis struktur yang hampir tidak bisa menunjukkan pola kristal.
Properti
Penampilan fisik
Itu adalah padatan coklat kemerahan.
Massa molekul
441.93 g/mol.
Kepadatan
11.34 g/ml.
Titik lebur
Itu meleleh dan terurai pada 160ºC. Tidak memiliki titik mendidih, jadi oksida ini tidak pernah mendidih.
Stabilitas
Au2SALAH SATU3 Secara termodinamik tidak stabil karena, seperti yang disebutkan di awal, emas tidak cenderung teroksidasi dalam kondisi suhu normal. Sehingga mudah direduksi menjadi emas mulia.
Semakin tinggi suhunya, semakin cepat reaksi ini, yang dikenal sebagai dekomposisi termal. Jadi, AU2SALAH SATU3 Pada 160ºC rusak untuk menghasilkan emas logam dan melepaskan oksigen molekuler:
2 au2SALAH SATU3 => 4 au + 3 o2
Reaksi yang sangat mirip dapat terjadi dengan senyawa lain yang mendukung reduksi ini. Mengapa Pengurangan? Karena emas memperoleh elektron yang dihilangkan oksigen; Apa yang sama dengan kehilangan tautan ke oksigen.
Kelarutan
Itu adalah padatan yang tidak larut dalam air. Namun, itu larut dalam asam klorida dan asam nitrat, karena pembentukan emas klorida dan nitrat.
Tata nama
Gold Oxide (III) adalah nama yang diatur oleh nomenklatur stok. Cara lain untuk menyebutkannya adalah:
-Nomenklatur Tradisional: Auric Oxide, karena Valencia 3+ adalah yang terbesar untuk emas.
-Nomenklatur Sistematik: Dioro Trioxide.
Aplikasi
Warna kaca
Salah satu kegunaannya yang paling terkemuka adalah memberikan warna kemerahan pada bahan -bahan tertentu, seperti kacamata, selain memberikan sifat -sifat tertentu yang melekat pada atom emas.
Dapat melayani Anda: Hydrogen bromide (HBR)Sintesis aurat dan emas fulminan
Jika AU ditambahkan2SALAH SATU3 Ke media di mana ia larut, dan di hadapan logam, ia dapat mengendap setelah penambahan basis yang kuat aurat; yang dibentuk oleh anion auo4- Di perusahaan kation logam.
Juga, AU2SALAH SATU3 bereaksi dengan amonia untuk membentuk senyawa emas fulminan, au2SALAH SATU3(NH3)4. Namanya berasal dari fakta bahwa itu sangat eksplosif.
Manipulasi Monocapas yang Dipicu Diri
Pada emas dan oksida, senyawa tertentu tidak teradsorpsi dengan cara yang sama, seperti dialil disulfur, RSSR. Ketika adsorpsi ini terjadi, ikatan Au-s terbentuk secara spontan, di mana atom sulfur menunjukkan dan mendefinisikan karakteristik kimia permukaan tersebut tergantung pada kelompok fungsional yang dihubungkannya.
RSSR tidak dapat diadsorpsi lebih dari AU2SALAH SATU3, Tapi tentang emas logam. Oleh karena itu, jika permukaan emas dan tingkat oksidasi dimodifikasi, serta ukuran partikel atau lapisan Au2SALAH SATU3, Permukaan yang lebih heterogen dapat dirancang.
Permukaan ini au2SALAH SATU3-AUSR berinteraksi dengan oksida logam dari perangkat elektronik tertentu, sehingga mengembangkan permukaan yang lebih pintar di masa depan.
Referensi
- Oksida emas. Dipulihkan dari: 911Metalurgiist.com
- Shi, r. Asahi dan c. Stampfl. (2007). Sifat au oksida emas2SALAH SATU3 dan au2O: Penelitian prinsip pertama. Masyarakat Fisik Amerika.
- « Chigualcan apa itu, karakteristik, habitat, kegunaan, sifat
- Hemidesmosom apa itu, deskripsi, struktur, fungsi »

