Struktur akrilonitril, sifat, produksi, penggunaan

- 3222
- 421
- Pete Lesch
Dia akrilonitril Itu adalah senyawa organik yang formula kentalnya co2Chcn. Itu adalah salah satu nitril paling sederhana yang ada. Kimia dan secara struktural tidak lebih dari produk persatuan antara kelompok vinil, Cho2= Ch-, dan nitril, kelompok sianida, copn. Ini adalah zat dengan dampak industri yang hebat di dunia plastik.
Secara fisik, ini adalah cairan yang tidak berwarna, dengan aroma bawang tertentu, dan yang dalam keadaan tidak murni menghadirkan nada kekuningan. Ini sangat mudah terbakar, beracun, dan mungkin karsinogenik, sehingga diklasifikasikan sebagai zat yang sangat berbahaya. Ironisnya, dengan itu mereka diproduksi plastik dan mainan kehidupan sehari -hari, seperti blok Tupperware dan Lego.
 Polimer akrilonitril ada di plastik Tupperware. Sumber: Stebulus via Wikipedia.
Polimer akrilonitril ada di plastik Tupperware. Sumber: Stebulus via Wikipedia. Di Skala Industri, Acrilonitril. Hampir semua jumlah yang dihasilkan dimaksudkan untuk pembuatan plastik, berdasarkan homopolimer, seperti poliakrilonitril, atau dalam kopolimer, seperti akrilonitril-butadien-styrene.
[TOC]
Struktur akrilonitril
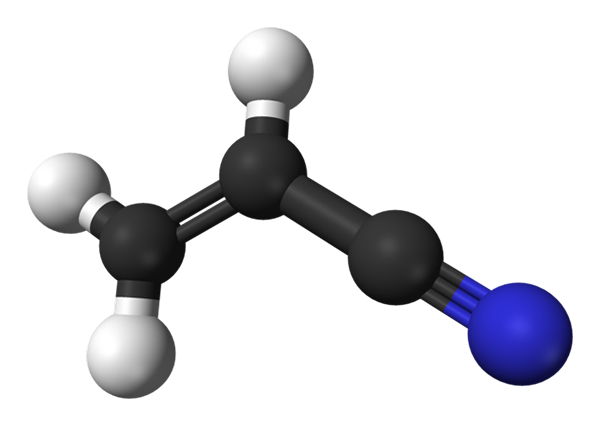 Struktur molekul akrilonitril. Sumber: Benjah-BMM27 / Domain Publik
Struktur molekul akrilonitril. Sumber: Benjah-BMM27 / Domain Publik Di gambar atas kita memiliki molekul akrilonitril yang diwakili dengan model bola dan batang. Bola hitam sesuai dengan atom karbon, sedangkan atom putih dan biru hingga hidrogen dan nitrogen, masing -masing. Kiri, ch2= Ch- sesuai dengan kelompok vinil, dan kanan, ke gugus cyano, copnn.
Seluruh molekulnya datar, karena karbon dari kelompok vinil memiliki hibridisasi SP2. Sementara itu, karbon kelompok ciano memiliki hibridisasi SP, berada di sebelah atom nitrogen dalam garis yang bertumpu pada bidang yang sama dengan sisa molekul.
Kelompok CN berkontribusi polaritas pada molekul, jadi molekul cho2CHCN membentuk dipol permanen di mana kepadatan elektronik tertinggi diarahkan ke atom nitrogen. Oleh karena itu, dipol-dipol.
Dapat melayani Anda: apa itu periodisitas kimia?Molekul ch2CHCN datar, bisa berharap bahwa dalam kristal mereka (dipadatkan pada -84 ºC) mereka tersedia satu sama lain seperti lembaran kertas, sehingga dipol mereka tidak mengusir.
Properti
Penampilan fisik
Cairan tidak berwarna tetapi dengan nada kekuningan saat menghadirkan beberapa kotoran. Ketika demikian, mereka merekomendasikan penyulingan sebelum penggunaannya. Itu mudah berubah dan juga memiliki aroma intens yang mirip dengan bawang.
Masa molar
53.064 g/mol
Titik lebur
-84 ºC
Titik didih
77 ºC
Titik nyala
-5 ºC (cangkir tertutup)
0 ºC (cangkir terbuka)
Suhu self -rection
481 ºC
Kepadatan
0,81 g/cm3
Kepadatan uap
1.83 dalam hubungan udara.
Tekanan uap
109 mmHg pada 25 ºC
Kelarutan
Di dalam air ia memiliki kelarutan 74 g/L hingga 25 ºC. Akrilonitril juga sangat larut dalam aseton, minyak, etanol, etil asetat dan benzena etanil.
Penguraian
Ketika secara termal melepaskan hidrogen sianida beracun, karbon oksida dan nitrogen oksida.
Produksi
Proses sohio
Acryonitrile dapat terjadi pada skala besar melalui berbagai reaksi dan proses kimia. Dari semuanya, proses SOHIO adalah yang paling banyak digunakan, yang terdiri dari amaxidasi katalitik propilen. Dalam reaktor bed terfluidisasi, propilen dicampur dengan udara dan amonia pada suhu sekitar 400 dan 510 ºC, di mana mereka bereaksi pada katalis padatan.
Reaktan memasuki reaktor sekali, terjadi reaksi berikut:
2ch3−ch = ch2 + 2 nh3 + 3 o2 → 2 ch2= Ch-cop + 6 h2SALAH SATU
Perhatikan bahwa oksigen direduksi menjadi air, sedangkan propilen mengoksidasi akrilonitril. Karenanya nama 'amoksidasi', karena itu adalah oksidasi yang melibatkan partisipasi amonia.
Dapat melayani Anda: mendidih: konsep, jenis dan contohProses alternatif
Selain proses SOHIO, reaksi lain dapat disebutkan yang memungkinkan memperoleh akrilonitril. Jelas, tidak semuanya dapat diskalakan, atau setidaknya dengan cara yang cukup menguntungkan, atau menghasilkan produk dengan kinerja tinggi atau kemurnian.
Acrylonitrile disintesis, sekali lagi dari propilen, tetapi membuatnya bereaksi dengan oksida nitrat pada katalis PBO2-Zro2 Airgel -berbentuk. Reaksinya adalah sebagai berikut:
4 ch3−ch = ch2 + 6 Tidak → 4 Cho2= Ch-cop + 6 h2Atau + n2
Reaksi yang tidak melibatkan propilen adalah pola yang dimulai dengan etilena oksida, yang bereaksi dengan hidrogen sianida untuk berubah menjadi etilena cyanohydrin; Dan kemudian, menjadi dehidrasi pada suhu 200 ºC di akrilonitril:
ETO + HCN → CH2Ohch2Cn
Ch2Ohch2CN + Q (200 ºC) → CH2= Ch-cop +h2SALAH SATU
Reaksi lain yang jauh lebih langsung adalah penambahan hidrogen sianida pada asetilena:
Hcuaranch + hcn → ch2= Ch-cop
Namun, banyak produk sekunder terbentuk, sehingga kualitas akrilonitril lebih rendah dibandingkan dengan proses SOHIO.
Selain zat yang disebutkan di atas, lactonitrile, propionitril.
Aplikasi
 Lego terutama diproduksi dengan plastik ABS, kopolimer di mana akrilonitril adalah bagian. Sumber: Pxhere.
Lego terutama diproduksi dengan plastik ABS, kopolimer di mana akrilonitril adalah bagian. Sumber: Pxhere. Akrilonitril adalah zat yang sangat diperlukan untuk industri plastik. Beberapa plastik yang diturunkan sangat dikenal. Begitulah kasus kopolimer acrilonitrilo-butadiene-styrene (ABS), yang dengannya potongan-potongan orang awam diproduksi. Kami juga memiliki serat akrilik, diuraikan dengan homopolimer poliacrylonitrile (PAN).
Dapat melayani Anda: saponifikasiDi antara plastik lain yang mengandung akrilonitril sebagai monomer, atau yang bergantung padanya untuk pembuatannya, kami memiliki: peregangan akrilen (san), butadiene acrylonitrile (NBR), akrilonitril acrylate (ASA), polyacrylamide, dan rarent -karet sintetis dan resin nitril nitrile, polyacrylamide, dan sintetis dan nitrile resin nitrile nitrile, nitrile nitrile nitrile, nitrile.
Secara praktis, polimer alami apa pun, seperti kapas, dapat dimodifikasi dengan memasukkan struktur molekulnya ke dalam akrilonitril. Dengan demikian, turunan nitril diperoleh, yang membuat kimia akrilonitril yang sangat luas.
Salah satu kegunaannya di luar dunia plastik adalah seperti pestisida yang dicampur dengan karbon tetrachloride. Namun, karena dampaknya yang mengerikan pada ekosistem laut, pestisida semacam itu telah melarang diri mereka sendiri atau tunduk pada pembatasan yang kuat.
Risiko
Akrilonitril adalah zat berbahaya, jadi harus dimanipulasi dengan sangat hati -hati. Setiap paparan yang tidak pantas atau terlalu lama pada senyawa ini bisa mematikan, baik dengan inhalasi, asupan atau kontak fisik.
Itu harus dipertahankan sejauh mungkin dari sumber panas apa pun, karena itu adalah cairan yang mudah menguap dan sangat mudah terbakar. Dia juga tidak boleh berhubungan dengan air, karena dia bereaksi keras terhadapnya.
Selain itu, ini adalah zat karsinogenik yang mungkin, yang telah dikaitkan dengan kanker hati dan paru -paru. Mereka yang telah terpapar zat ini mengalami peningkatan kadar tiocyanate yang diekskresikan dalam urin, dan sianida darah.
Referensi
- Morrison, r. T. dan boyd, r, n. (1987). Kimia organik. Edisi ke -5. Editorial Addison-Wesley Inter-American.
- Carey f. (2008). Kimia organik. (Edisi Keenam). MC Graw Hill.
- Graham Solomons t.W., Craig b. Fryhle. (2011). Kimia organik. (Edisi ke -10.). Wiley Plus.
- Wikipedia. (2020). Acrylonitrile. Diperoleh dari: di.Wikipedia.org
- Pusat Nasional Informasi Bioteknologi. (2020). Acrylonitrile. Database pubchem., CID = 7855. Pulih dari: pubchem.NCBI.Nlm.Nih.Pemerintah
- Elsevier b.V. (2020). Acrylonitrile. Ilmiah. Diperoleh dari: Scientedirect.com
- Korry Barnes. (2020). Apa itu Acrylonitrile? - Gunakan & Properti. Belajar. Pulih dari: belajar.com
- Pajonk, g.M., Manzalji, t. (1993). Sintesis akrilonitril dari campuran propilena dan nitrat oksida pada PBO2-Zro2 Katalis Airgel. LETT CATAL dua puluh satu, 361-369. doi.org/10.1007/BF00769488
- « Karakteristik pemrograman dinamis, contoh, kelebihan, kerugian
- Apa proses isotermal? (Contoh, latihan) »

