Melatih anion, karakteristik dan jenis
- 4994
- 596
- Leland Robel
A anion Ini semua adalah spesies kimia dengan beban negatif, selain menjadi salah satu dari dua jenis ion yang ada. Beban negatifnya berasal dari fakta bahwa ia menyajikan kelebihan elektron dibandingkan dengan bentuk netral spesies; Untuk setiap elektron tambahan, beban negatifnya meningkat dalam suatu unit.
Beban negatif dapat ditempatkan di satu atau lebih atom, serta menutupi pengaruhnya pada molekul secara keseluruhan. Sebagai penyederhanaan, terlepas dari di mana beban itu (-), itu dianggap sebagai anion untuk seluruh spesies, senyawa atau molekul.
 Anion. Sumber: Gabriel Bolívar.
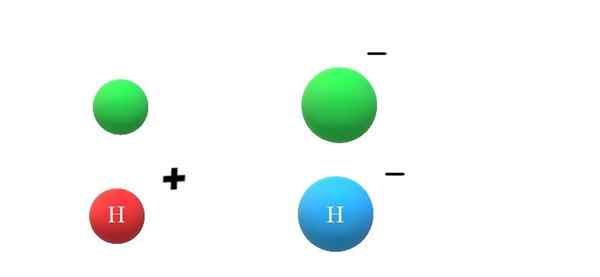
Anion. Sumber: Gabriel Bolívar. Jika spesies netral memenangkan elektron, beban negatif berlebih akan bermanifestasi dalam pembentukan anion x-, yang juga akan membawa peningkatan jari -jari atomnya (gambar superior, dengan bola hijau). X dan x- mereka sangat berbeda dalam sifat mereka dan bagaimana mereka berinteraksi dengan lingkungan mereka.
Jika sekarang seharusnya+ atau h-, masing -masing. Kation h+ Ion hidrogen, juga disebut proton; dan H- Itu adalah anion hidrida, yang paling "sederhana" dari semua anion yang diketahui.
[TOC]
Pelatihan Anion
Pembentukan anion dapat dengan mudah dijelaskan dalam teori; Meskipun, secara eksperimental, itu bisa menjadi tantangan, terutama jika Anda menginginkan murni, tanpa biaya positif yang tertarik pada biaya negatif Anda.
Beban formal dan lebih sedikit tautan
Anion akan dibentuk ketika ada kelebihan atau gain elektron dalam atom. Keuntungan ini dapat ditentukan dengan menggunakan beban formal dalam struktur Lewis. Juga, melalui metode sebelumnya, Anda dapat mengetahui persis atom atau kelompok apa yang datang dari beban negatif.
Dapat melayani Anda: asetonitril (C2H3N)Saat atom membentuk ikatan kovalen, meskipun distribusi elektron adil, mungkin ada sebagian kehilangan elektron. Dalam hal ini, semakin sedikit tautan membentuk pasangan bebas elektron yang paling elektron yang akan dimiliki dan karenanya menampilkan beban negatif.
Pertimbangkan misalnya molekul amonia, NH3. NH3 Itu netral dan karenanya tidak memiliki muatan listrik. Jika H dihapus, yaitu, tautan N-H rusak, anion NH akan diperoleh2-. Menggambar struktur lewis dan menghitung beban formal n Anda dapat memeriksa ini.
Mengikuti pecahnya lebih banyak tautan N-H, sekarang Anda memiliki NH Anion2-; dan menghilangkan h terakhir, anion n akhirnya diperoleh3-, disebut anion nitruro. Nitrogen tidak lagi memiliki cara mendapatkan lebih banyak elektron, dan beban -3 adalah yang paling negatif yang dapat dicapai; Orbitalnya tidak memberi lebih banyak.
Pengurangan
Anion dapat membentuk produk pengurangan: memperoleh elektron yang mengoksidasi spesies lain, yang kehilangan mereka. Oksigen, misalnya, mewakili jenis reaksi kimia ini dengan sangat baik.
Saat oksigen berkurang, teroksidasi menjadi spesies lain, dan menjadi anion oksida, atau2-; hadir dalam mineral yang tak terhitung banyaknya dan senyawa anorganik.
Fisik
Atom dapat memperoleh elektron jika berada dalam fase gas:
X (g) + e- => X-(G)
Cara pembentukan anion ini menyiratkan pengetahuan luas tentang teknik fisik, sementara anion gas tidak mudah dipelajari, juga semua spesies tidak diuapkan atau di atomisasi dengan kesederhanaan pada fase gas.
Karakteristik
Secara umum, karakteristik khas suatu anion akan disebutkan di bawah ini sebelum membahas jenis dan contohnya:
-Lebih besar dari atom netral.
Dapat melayani Anda: klorin dioksida (clo2): struktur, penggunaan, mendapatkan, risiko, sifat-Ini bisa lebih atau kurang stabil, meskipun ada penolakan elektronik yang tumbuh di antara elektronnya sendiri.
-Jika anion berasal dari atom elektronegatif kecil, seperti karbon, itu sangat reaktif.
-Atur momen dipol yang kuat.
-Lebih lanjut meningkatkan interaksinya dengan pelarut kutub.
-Anion monoatomik adalah isolektronik untuk gas mulia periode; yaitu, ia memiliki lapisan valensi dengan jumlah elektron yang sama.
-Itu dapat mempolarisasi awan elektronik atom tetangga, mengusir elektron eksternalnya.
Teman-teman
Monoatomik
Seperti namanya, itu adalah anion yang terdiri dari satu atom: beban negatif terletak dengan baik. Setiap kelompok dalam tabel periodik memiliki muatan negatif yang khas; Dan karena mereka anion, mereka adalah non -logam yang terletak di blok p. Beberapa contoh dan namanya di bawah ini:
-Cl-, khlorida.
-yo-, Saya terakhir.
-F-, fluor.
-Br-, bromida.
-SALAH SATU2-, oksida.
-S2-, sulfida.
-DIA2-, Seleniuro.
-teh2-, Telururo.
-PO2-, polioniuro.
-N3-, Nitruro.
-P3-, fosfur.
-Kartu as3-, Arseniuro.
-SB3-, Antimoniuro.
-C4-, karbit.
-Ya4-, Siliciuro.
-B3-, Boruro.
Oxoanion
Oxoanion ditandai dengan memiliki ikatan x = o, di mana x dapat berupa elemen non -metalik (kecuali fluoride), atau logam (krom, mangan, dll.). Mereka juga dapat memiliki satu atau lebih tautan X-O sederhana.
Beberapa oxoanion dengan nama masing -masing adalah:
-Clo-, hipoklorit.
-Kawan-, Hipobromito.
-Io-, hipoyodite.
-Clo2-, Klorit.
-Clo3-, Klorat.
-Io3-, Yodato.
-Clo4-, perklorat.
-PO43-, fosfat.
-BERSAMA32-, karbonat.
-Cro42-, kromat.
-Cr2SALAH SATU72-, Dicromato.
-Sw42-, sulfat.
-S2SALAH SATU32-, Tiosulfat.
-TIDAK3-, nitrat.
-TIDAK2-, nitrit.
-Bo33-, borate.
-Aso43-, Arseniato.
-PO33-, fosfit.
-Mne4-, permanganat.
Organik
Molekul organik memiliki gugus fungsional yang dapat diisi secara elektrik. Sebagai? Dengan pembentukan atau pecahnya ikatan kovalen, sangat mirip dengan contoh molekul NH3.
Dapat melayani Anda: besi (elemen): karakteristik, struktur kimia, penggunaanBeberapa anion organik adalah:
-Ch3Mendekut-, asetat.
-Hcoo-, Format.
-C2SALAH SATU42-, Oksalat.
-Rcoo-, Karboksilat.
-Ch3Conh-, Amidato.
-Ro-, Alkohol.
-R3C-, Carbanion.
-Ch3SALAH SATU-, Metoksida.
Poliatomik
Oxoanion juga merupakan anion poliatomik, yaitu, mereka terdiri dari lebih dari satu atom. Hal yang sama berlaku untuk anion organik. Namun, Poliatomik tidak memasukkan klasifikasi sebelumnya. Beberapa dari mereka adalah:
-Cn-, sianida (memiliki triple link, cop).
-OCN-, Sianat.
-Scn-, Tiocianato.
-NH2-, Amuraturo.
-Oh-, hidroksil, hidroksida atau oksidrillo.
-SALAH SATU2-, superoksida.
-SALAH SATU22-, peroksida.
Molekuler atau kompleks
Dalam anion organik beberapa kelompok fungsional yang dimuat negatif disebutkan. Kelompok -kelompok ini dapat menjadi bagian dari molekul besar, dan dengan demikian anion dapat menjadi senyawa yang kuat dan banyak tautan. Jenis anion yang paling sederhana adalah molekul h hipotetis2-.
Di antara contoh lain dari anion ini adalah polisulfuros, sN2-, yang terdiri dari rantai dengan beberapa tautan S-S. Demikian juga, senyawa koordinasi logam dengan beban negatif dapat dihitung, seperti [cocl4(NH3)2]- dan [CUCL4]2-.
Referensi
- Whitten, Davis, Peck & Stanley. (2008). Kimia. (Edisi ke -8.). Pembelajaran Cengage.
- Wikipedia. (2019). Anion. Pulih dari: is.Wikipedia.org
- Helmestine, Anne Marie, PH.D. (21 Maret 2019). Daftar tabel dan formula anion umum. Pulih dari: thinkco.com
- Yayasan CK-12. (29 Juni 2016). Pembentukan anion. Libretteks Kimia. Pulih dari: chem.Librettexts.org
- Francis e. (2002). Anion. Clackamas Community College. Diperoleh dari: DL.Clackamas.Edu
- Masyarakat Fisik Amerika. (3 November 2011). Sinopsis: Anion molekul paling sederhana. Pulih dari: fisika.APS.org
- « Fernando del Paso Biografi, Gaya, Pekerjaan dan Frasa
- Struktur anisol, sifat, nomenklatur, risiko dan penggunaan »

