Struktur, sifat, penggunaan dan risiko butanal
- 3150
- 668
- Dewey Runolfsdottir
Dia Butanal Ini adalah aldehida rantai terbuka, yang terdiri dari empat atom karbon, dan analog dengan butana; Itu sebenarnya adalah bentuk hidrokarbon butana yang paling teroksidasi kedua setelah asam butirat. Formula molekulnya adalah Cho3Ch2Ch2Cho, di mana -cho adalah grup formil.
Aldehida ini, salah satu yang paling ringan, terdiri dari cairan yang transparan, mudah terbakar, dan kurang padat daripada air. Selain itu, larut dalam air dan larut dengan sebagian besar pelarut organik; Oleh karena itu, dapat digunakan untuk memiliki campuran organik satu fase.
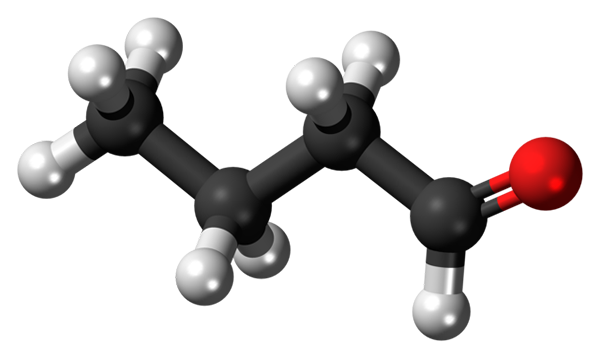
 Molekul butanal atau butiraldehyde. Sumber: Jynto [CC0]
Molekul butanal atau butiraldehyde. Sumber: Jynto [CC0] Kehadiran gugus karbonil (dari bola merah, gambar superior) memberikan polaritas kimia pada molekul butanal, dan oleh karena itu kemampuan untuk mengalami interaksi dipol-dipolo antara molekulnya; Meskipun tidak ada jembatan hidrogen yang terbentuk di antara mereka.
Ini membawa konsekuensi bahwa butanal saat ini mendidih dan poin fusi lebih besar dari butana, tetapi kurang dari yang disajikan oleh n-boutil alkohol.
Butanal digunakan sebagai pelarut dan perantara untuk mendapatkan banyak produk; seperti akselerator vulkanisasi karet, resin, produk farmasi dan agrokimia.
Butanal adalah senyawa beracun yang inhalasi dapat menyebabkan peradangan saluran pernapasan atas, bronkus dan edema paru yang, bahkan, dapat memiliki konsekuensi yang fatal.
[TOC]
Struktur Butanal
Baru saja disebutkan bahwa grup formil, -ch. Sebagai akibatnya, molekul mereka dapat berinteraksi satu sama lain melalui gaya dipol-dipolo.
Dapat melayani Anda: Rotary Dryer: Operasi, untuk apa, bagian, aplikasiPada gambar atas ditampilkan, dengan model bola dan batang, bahwa molekul butanal memiliki struktur linier. Group's Carbon -Cho memiliki hibridisasi SP2, Sedangkan karbon yang tersisa3.
Tidak hanya itu, tetapi juga fleksibel, dan tautannya dapat berputar pada sumbu mereka sendiri; Dan dengan demikian, konformasi atau konformer yang berbeda dihasilkan (senyawa yang sama, tetapi dengan tautan yang diputar).
Conformeros
Gambar berikut paling jelas menjelaskan poin ini:
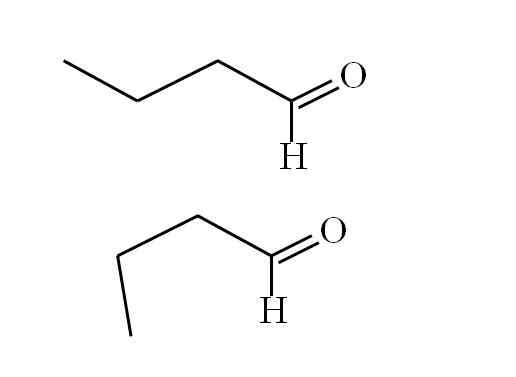 Butanal kesesuaian. Sumber: Gabriel Bolívar.
Butanal kesesuaian. Sumber: Gabriel Bolívar. Konformer pertama (superior) sesuai dengan molekul gambar pertama: gugus metil di sebelah kiri, -ch3, dan grup -cho, berada dalam posisi anti paralel; satu poin naik, dan yang lainnya turun, masing -masing.
Sementara itu, konformer kedua (yang lebih rendah) sesuai dengan molekul dengan -ch3 dan -ho dalam posisi yang dikalahkan; yaitu, keduanya menunjuk ke arah yang sama.
Kedua konformer dengan cepat dipertukarkan, dan oleh karena itu molekul butanal berputar dan terus bergetar; Dan menambahkan fakta bahwa ia memiliki dipol permanen, ini memungkinkan interaksinya menjadi cukup kuat untuk mendidih pada 74,8ºC.
Properti
Nama Kimia
-Butanal
-Butiraldehyde
-1-butanal
-Butiral
-N-butiraldehyde.
Formula molekul
C4H8Atau ch3Ch2Ch2Cho.
Penampilan fisik
Itu adalah cairan yang jernih dan transparan.
Bau
Bau karakteristik, acre, aldehyde.
Titik didih
167 ºF pada 760 mmHg (74,8 ºC).
Titik lebur
-146 ºF (-96,86 ºC).
titik pengapian
-8 ºF (-22 ºC) Kaca tertutup.
Kelarutan air
7 g/100 ml pada 25 ºC.
Kelarutan dalam pelarut organik
Lembar dengan etanol, eter, etil asetat, aseton, toluena dan banyak pelarut organik lainnya.
Kepadatan
0,803 g/cm3 pada 68 ºF.
Dapat melayani Anda: nitrat: properti, struktur, nomenklatur, pelatihanKepadatan uap
2,5 (dalam hubungan udara diambil sama dengan 1).
Tekanan uap
111 mmHg pada 25 ºC.
Pengarahan diri sendiri
446 ºF. 425 ºF (21,8 ºC).
Zat yang lengket dan kental
0,45 cpoise pada 20 ºC.
Panas pembakaran
2479,34 kJ/mol pada 25 ° C.
Panas penguapan
33,68 kJ/mol pada 25 ° C.
Tegangan permukaan
29,9 Dina/cm A 24 ºC.
Ambang bau
0,009 ppm.
Indeks bias
1.3843 hingga 20 ºC.
Momen dipolar
2.72 d.
Panjang gelombang (λ) dari penyerapan maksimum dalam air
225 nm dan 282 nm (lampu ultraviolet).
Polimerisasi
Butanal Can Polimerized dalam kontak dengan alkalis atau asam, menjadi polimerisasi berbahaya.
Reaktivitas
Saat terkena udara teroksidasi, membentuk asam butirat. Pada suhu 230ºC, Butanal secara spontan meradang dengan udara.
Kondensasi aldolik
Dua molekul butanal dapat bereaksi satu sama lain, di hadapan KOH dan suhu 6-8 ºC, untuk membentuk senyawa 2-etil-3-hidroksigeksanol. Jenis senyawa ini disebut aldol, karena memiliki kelompok aldehida dan kelompok alkohol dalam strukturnya.
Perpaduan
Butanal dapat terjadi dengan dehidrogenasi katalitik alkohol N-butil; hidrogenasi katalitik crotonaldehyde; dan hidroformilasi propilen.
Aplikasi
Industrialis
-Butanal adalah pelarut industri, tetapi juga perantara dalam sintesis pelarut lain; Misalnya 2-ethylhexanol, n-butanol dan trimethylpropane.
-Ini juga digunakan sebagai perantara dalam elaborasi resin sintetis, di antaranya, butiral polyvinil; akselerator vulkanisasi karet; pembuatan produk farmasi; produk untuk perlindungan tanaman; pestisida; antioksidan; Asisten Brinking.
-Butanal digunakan sebagai bahan baku untuk elaborasi aroma sintetis. Selain itu, digunakan sebagai agen penyedaman makanan.
Ini dapat melayani Anda: Sodium bromide (NABR)Yang lain
-Pada manusia, butanal digunakan sebagai biomarker yang menunjukkan kerusakan oksidasi, dialami oleh lipid, protein dan asam nukleat.
-Itu digunakan secara eksperimental, bersama dengan formalin dan gluterdehyde, untuk mencoba mengurangi pelunakan yang dialami oleh helm daging sapi, karena paparan air, urin dan kotoran sapi sendiri. Hasil eksperimen positif.
Risiko
Butanal destruktif untuk selaput jaringan lendir dari saluran pernapasan atas, serta untuk jaringan kulit dan mata.
Dengan kontak dengan kulit menghasilkan kemerahan dan luka bakar. Di mata, lesi yang sama diproduksi, disertai dengan rasa sakit dan kerusakan pada jaringan mata.
Inhalasi butanal dapat memiliki konsekuensi serius, karena dapat diproduksi dalam laring dan peradangan dan bronkial edema; Saat berada di paru -paru, ia menghasilkan pneumonia kimia dan edema paru.
Tanda -tanda yang berlebihan terdiri dari: sensasi ardor pada saluran pernapasan atas, batuk, mengi, yaitu emisi peluit saat bernafas; laringitis, kurang napas, sakit kepala, mual dan juga muntah.
Inhalasi bisa berakibat fatal karena kejang jalan perbaikan.
Konsumsi butanal menyebabkan sensasi "pembakaran" pada jalur pencernaan: rongga oral, faring, kerongkongan dan lambung.
Referensi
- Morrison, r. T. Dan Boyd, R. N. (1987). Kimia organik. (5ta Edisi.). Editorial Addison-Wesley Iberoamericana.
- Carey f. (2008). Kimia organik. (Edisi Keenam). MC Graw Hill.
- Pubchem. (2019). Butanal. Pulih dari: pubchem.NCBI.Nim.Nih.Guv
- Wikipedia. (2019). Butanal. Pulih dari: is.Wikipedia.org
- Buku Kimia. (2017). Butanal. Dipulihkan dari: Chemicalbook.com
- BASF. (Mei 2017). N-Butyaldehyde. [PDF]. Diperoleh dari: pelarut.BASF.com
- « Karakteristik, jenis dan contoh karbon primer
- Karakteristik pendidikan integral dan cara mencapainya »

