Konsep panas sensitif, formula dan latihan diselesaikan

- 843
- 28
- Ray Thiel
Dia Panas sensitif Itu adalah energi termal yang dipasok ke objek yang menyebabkan suhunya meningkat. Ini adalah kebalikan dari panas laten, di mana energi termal tidak meningkatkan suhu tetapi meningkatkan perubahan fase, misalnya dari padatan ke cairan.
Contohnya mengklarifikasi konsep tersebut. Misalkan kita memiliki pot dengan suhu air 20 ° C. Saat kami meletakkannya di tanduk, panas yang disediakan meningkatkan suhu air secara perlahan hingga 100 ° C (suhu mendidih air di permukaan laut). Panas yang disediakan disebut panas sensitif.
 Panas yang memanaskan tangan Anda adalah panas yang sensitif. Sumber: Pixabay
Panas yang memanaskan tangan Anda adalah panas yang sensitif. Sumber: Pixabay Setelah air mencapai suhu mendidih, panas yang dipasok oleh hornilla tidak lagi meningkatkan suhu air, yang tetap pada 100 ° C. Dalam hal ini, energi termal yang disediakan diinvestasikan dalam air penguapan. Panas yang disediakan laten karena tidak menaikkan suhu, tetapi menyebabkan perubahan fase cair ke fase gas.
Ini adalah fakta eksperimental bahwa panas sensitif yang diperlukan untuk mencapai variasi suhu tertentu berbanding lurus dengan variasi tersebut dan massa objek.
[TOC]
Konsep dan formula
Telah diamati bahwa terlepas dari perbedaan massa dan suhu, panas sensitif juga tergantung pada material. Untuk alasan ini, konstanta proporsionalitas antara panas sensitif dan produk massa dengan perbedaan suhu disebut panas spesifik.
Jumlah panas sensitif yang disediakan juga tergantung pada bagaimana proses dilakukan. Misalnya, berbeda jika proses dilakukan pada volume konstan dari tekanan konstan.
Formula untuk panas sensitif dalam suatu proses isobarik, Artinya tekanan konstan, itu adalah sebagai berikut:
Q = CP . m (tF - Tyo)
Dalam persamaan sebelumnya Q Itu adalah panas sensitif yang dipasok ke objek massa M, yang telah meningkatkan suhu awalnya Tyo Sampai nilai akhir Tf. Dalam persamaan sebelumnya juga muncul CP, yang merupakan panas spesifik bahan pada tekanan konstan karena proses telah dilakukan dengan cara ini.
Perhatikan bahwa panas sensitif adalah positif ketika diserap oleh objek dan menyebabkan kenaikan suhu.
Dalam hal gas yang tertutup dalam wadah kaku disediakan, prosesnya akan isocoric, yaitu, pada volume konstan; Dan formula panas sensitif akan ditulis seperti ini:
Dapat melayani Anda: Gerakan bergelombang: Karakteristik, jenis gelombang, contohQ = cv. M . (TF - Tyo)
Koefisien adiabatik γ
Rasio antara panas spesifik pada tekanan konstan dan panas spesifik pada volume konstan untuk bahan atau zat yang sama disebut Koefisien adiabatik, yang umumnya dilambangkan dengan huruf gamma gamma γ.
Dia Koefisien adiabatik lebih besar dari unit. Panas yang diperlukan untuk menaikkan suhu tubuh gram massa ke tingkat lebih besar dalam proses isobarik daripada di isokoris.
Ini karena dalam kasus pertama bagian panas digunakan untuk melakukan pekerjaan mekanis.
Selain panas spesifik, kapasitas panas tubuh biasanya ditentukan. Ini adalah jumlah panas yang diperlukan untuk menaikkan suhu tubuh itu satu derajat celcius.
Kapasitas panas c
Kapasitas panas dilambangkan dengan C huruf besar, sedangkan panas spesifik dengan C huruf kecil. Hubungan antara kedua jumlahnya adalah:
C = c⋅ m
Di mana M Itu adalah massa tubuh.
Panas spesifik molar juga digunakan, yang didefinisikan sebagai jumlah panas sensitif yang diperlukan untuk menaikkan ke suhu Celcius atau Kelvin.
Panas spesifik dalam padatan, cairan dan gas
Panas molar spesifik dari sebagian besar padatan memiliki nilai yang dekat dengan 3 waktu R, Di mana R Itu adalah konstanta gas universal. R = 8.314472 J/(mol ℃).
Misalnya, aluminium memiliki panas molar spesifik 24.2 J/(mol ℃), Tembaga 24.5 J/(mol ℃), emas 25.4 J/(mol ℃), dan besi manis 25.1 J/(mol ℃). Perhatikan bahwa nilai -nilai ini dekat 3r = 24,9 J/(mol ℃).
Di sisi lain, bagi sebagian besar gas, panas spesifik dekat N (r/2), dimana N bilangan bulat dan R Itu adalah konstanta gas universal. Bilangan bulat N terkait dengan jumlah derajat kebebasan molekul yang membentuk gas.
Misalnya, dalam gas monoatomik yang ideal, yang molekulnya hanya memiliki tiga derajat kebebasan, panas molar spesifik untuk volume konstan adalah 3 (r/2). Tetapi jika itu adalah gas diatomik yang ideal, dua derajat rotasi juga, jadi Cv = 5 (r/2).
Dapat melayani Anda: setengah lingkaran: cara menghitung perimeter, area, centroid, latihanDalam gas ideal, hubungan berikut antara panas molar panas spesifik dan volume konstan dipenuhi: CP = cv + R.
Sebutan samping layak air. Dalam keadaan cair di 25 ℃ air memiliki CP = 4.1813 J/(G ℃), Uap air pada 100 derajat yang dimiliki Celcius CP = 2.080 J/(G ℃) Dan es air hingga nol kelas yang dimiliki Celcius CP = 2.050 J/(G ℃).
Perbedaan dengan panas laten
Materi dapat ditemukan di tiga negara bagian: padat, cair dan gas. Untuk mengubah keadaan, diperlukan energi, tetapi setiap zat meresponsnya dengan cara yang berbeda sesuai dengan karakteristik molekuler dan atomnya.
Saat padat meleleh atau cairan menguap, suhu objek tetap konstan sampai semua partikel telah mengubah statusnya.
Oleh karena itu, dimungkinkan bahwa satu zat pada saat yang sama dalam kesetimbangan dalam dua fase: padatan - cair atau cairan - uap, misalnya uap, misalnya. Sejumlah zat dapat berlalu dari satu negara ke negara lain dengan menambahkan atau menghilangkan sedikit panas, sementara suhu tetap diperbaiki.
Panas yang dipasok ke suatu bahan menyebabkan partikelnya bergetar lebih cepat dan meningkatkan energi kinetiknya. Ini berarti kenaikan suhu.
Mungkin saja energi yang mereka peroleh begitu besar sehingga mereka tidak lagi kembali ke posisi keseimbangan mereka dan meningkatkan pemisahan di antara mereka. Ketika ini terjadi, suhu tidak meningkat, tetapi zat tersebut berlalu dari padatan ke cairan atau cairan gas.
Dalam panas yang diperlukan untuk ini terjadi, ia dikenal sebagai panas laten. Oleh karena itu, panas laten adalah panas yang dengannya suatu zat dapat mengubah fase.
Inilah perbedaan dengan panas sensitif. Zat yang menyerap panas sensitif meningkatkan suhunya dan tetap dalam keadaan yang sama.
Cara menghitung panas laten?
Panas laten dihitung dengan persamaan:
Q = m . L
Di mana L Ini mungkin panas spesifik penguapan atau fusi. Unit L Mereka adalah energi/massa.
Para ilmuwan telah memberikan banyak denominasi panas, tergantung pada jenis reaksi di mana ia berpartisipasi. Jadi, misalnya, ada panas reaksi, panas pembakaran, panas pemadatan, panas larutan, panas sublimasi dan banyak lainnya.
Dapat melayani Anda: energi kinetik: karakteristik, jenis, contoh, latihanNilai banyak jenis panas ini untuk zat yang berbeda ditabulasi.
Latihan terpecahkan
Contoh 1
Asumsikan satu yang memiliki 3 kg aluminium massal. Awalnya pada 20 ° C dan Anda ingin menaikkan suhunya hingga 100 ° C. Hitung panas sensitif yang diperlukan.
Larutan
Pertama kita perlu mengetahui panas spesifik aluminium
CP = 0,897 J / (G ° C)
Jadi, jumlah panas yang dibutuhkan untuk memanaskan potongan aluminium
Q = cP m (tf - ti) = 0.897 * 3000 * (100 - 20) j
Q = 215280 J
Contoh 2
Hitung jumlah panas yang dibutuhkan untuk memanaskan 1 liter air dari 25 ° C hingga 100 ° C di permukaan laut. Mengungkapkan hasilnya juga dalam kilokalori.
Larutan
Hal pertama yang harus kita ingat adalah bahwa 1 liter air memiliki berat 1 kg, yaitu 1000 gram.
Q = cP m (tf - ti) = 4.1813 j/(g ℃) * 1000 g * (100 ℃ - 25 ℃) = 313597.5 j
Kaloria adalah satuan energi yang didefinisikan sebagai panas sensitif yang diperlukan untuk menaikkan gram air ke Celcius. Oleh karena itu, 1 kalori setara dengan 4.1813 joule.
Q = 313597.5 J * (1 kal / 4,1813 j) = 75000 kapur = 75 kkal.
Contoh 3
Bahan 360,16 gram dipanaskan dari 37 ℃ hingga 140 ℃. Energi termal yang disediakan adalah 1150 kalori.
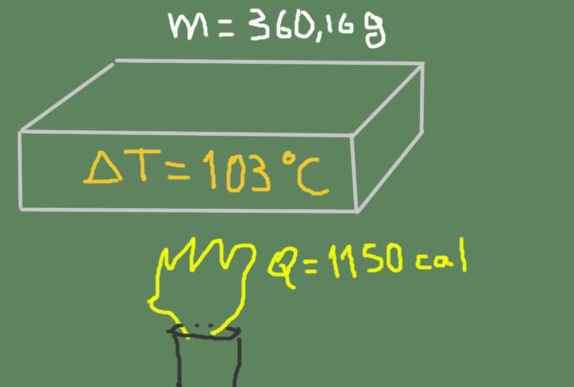 Memanaskan sampel. Sumber: Made sendiri.
Memanaskan sampel. Sumber: Made sendiri. Temukan panas material spesifik.
Larutan
Kita dapat menulis panas spesifik berdasarkan panas sensitif, massa dan variasi suhu sesuai dengan rumus:
CP = Q /(m Δt)
Mengganti data yang kami miliki sebagai berikut:
CP = 1150 kal / (360.16 g * (140 ℃ - 37 ℃)) = 0.0310 Cal / (G ℃)
Tetapi karena kalori setara dengan 4.1813 J, hasilnya juga dapat dinyatakan sebagai
CP = 0,130 J / (g ℃)
Referensi
- Giancoli, d. 2006. Fisika: Prinsip dengan aplikasi. 6th. Ed. Prentice Hall. 400 - 410.
- Kirkpatrick, l. 2007. Fisika: Pandangan Dunia. 6ta Edisi Singkat. Pembelajaran Cengage. 156 - 164.
- Tippens, hlm. 2011. Fisika: Konsep dan Aplikasi. 7. Edisi revisi. Bukit McGraw. 350 - 368.
- Rex, a. 2011. Dasar -dasar fisika. Pearson. 309 - 332.
- Sears, Zemansky. 2016. Fisika Universitas dengan Fisika Modern. 14th. Volume1. 556 - 553.
- Serway, r., Vulle, c. 2011. Dasar -dasar fisika. 9na Pembelajaran Cengage. 362 - 374.
- « Karakteristik troponin, struktur, fungsi dan tes
- Formula panas ceped, cara menghitungnya dan menyelesaikan latihan »

